Основные квантово-механические принципыРефераты >> Естествознание >> Основные квантово-механические принципы
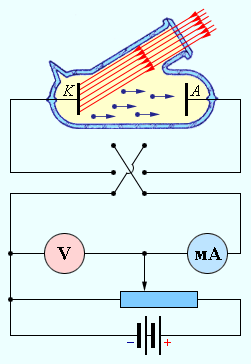
Рисунок 1.
Схема экспериментальной установки для изучения фотоэффекта.
Многочисленными экспериментаторами были установлены следующие основные закономерности фотоэффекта:
Максимальная кинетическая энергия фотоэлектронов линейно возрастает с увеличением частоты света ν и не зависит от его интенсивности.
Для каждого вещества существует так называемая красная граница фотоэффекта, т. е. наименьшая частота νmin, при которой еще возможен внешний фотоэффект.
Число фотоэлектронов, вырываемых светом из катода за 1 с, прямо пропорционально интенсивности света.
Фотоэффект практически безынерционен, фототок возникает мгновенно после начала освещения катода при условии, что частота света ν > νmin.
Все эти закономерности фотоэффекта в корне противоречили представлениям классической физики о взаимодействии света с веществом. Согласно волновым представлениям электрон при взаимодействии с электромагнитной световой волной должен был бы постепенно накапливать энергию, и потребовалось бы значительное время, зависящее от интенсивности света, чтобы электрон накопил достаточно энергии для того, чтобы вылететь из катода. Как показывают расчеты, это время должно было бы исчисляться минутами или часами. Однако, опыт показывает, что фотоэлектроны появляются немедленно после начала освещения катода. В этой модели невозможно было также понять существование красной границы фотоэффекта. Волновая теория света не могла объяснить независимость энергии фотоэлектронов от интенсивности светового потока, пропорциональность максимальной кинетической энергии частоте света.
Таким образом, электромагнитная теория света оказалась неспособной объяснить эти закономерности.
Выход был найден А. Эйнштейном в 1905 г. Теоретическое объяснение наблюдаемых закономерностей фотоэффекта было дано Эйнштейном на основе гипотезы М. Планка о том, что свет излучается и поглощается определенными порциями, причем энергия каждой такой порции определяется формулой E = hν, где h – постоянная Планка (1,05*10-27 эрг*с), а ν – частота световой волны. Эйнштейн сделал следующий шаг в развитии квантовых представлений. Он пришел к выводу, что и свет имеет прерывистую дискретную структуру. Электромагнитная волна состоит из отдельных порций – квантов, впоследствии названных фотонами. При взаимодействии с веществом фотон целиком передает всю свою энергию hν одному электрону.
2.2. Опыт Резерфорда. Ядерная модель атома.
Первая попытка создания модели атома на основе накопленных экспериментальных данных принадлежит Дж. Томсону (1903 г.). Он считал, что атом представляет собой электронейтральную систему шарообразной формы радиусом примерно равным 10–10 м. Положительный заряд атома равномерно распределен по всему объему шара, а отрицательно заряженные электроны находятся внутри него (рис. 2). Для объяснения линейчатых спектров испускания атомов Томсон пытался определить расположение электронов в атоме и рассчитать частоты их колебаний около положений равновесия. Однако эти попытки не увенчались успехом. Через несколько лет в опытах великого английского физика Э. Резерфорда было доказано, что модель Томсона неверна.
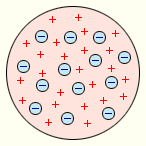
Рисунок 2.
Модель атома Дж. Томсона.
Первые прямые эксперименты по исследованию внутренней структуры атомов были выполнены Э. Резерфордом и его сотрудниками Э. Марсденом и Х. Гейгером в 1909–1911 годах. Резерфорд предложил применить зондирование атома с помощью α-частиц, которые возникают при радиоактивном распаде радия и некоторых других элементов. Масса α-частиц приблизительно в 7300 раз больше массы электрона, а положительный заряд равен удвоенному элементарному заряду.
Результат эксперимента был совершенно неожиданным даже для Резерфорда. Он находился в резком противоречии с моделью атома Томсона, согласно которой положительный заряд распределен по всему объему атома. Результаты эксперимента привели Резерфорда к выводу, что атом почти пустой, и весь его положительный заряд сосредоточен в малом объеме. Эту часть атома Резерфорд назвал атомным ядром. Так возникла ядерная модель атома.
Опираясь на классические представления о движении микрочастиц, Резерфорд предложил планетарную модель атома. Согласно этой модели, в центре атома располагается положительно заряженное ядро, в котором сосредоточена почти вся масса атома. Атом в целом нейтрален. Вокруг ядра, подобно планетам, вращаются под действием кулоновских сил со стороны ядра электроны (рис. 3).
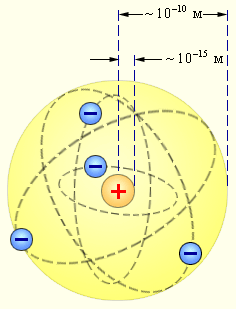
Рисунок 3.
Планетарная модель атома Резерфорда. Показаны круговые орбиты четырех электронов.
Планетарная модель атома, предложенная Резерфордом, несомненно явилась крупным шагом в развитии знаний о строении атома. Она была совершенно необходимой для объяснения опытов по рассеянию α-частиц. Однако она оказалась неспособной объяснить сам факт длительного существования атома, т. е. его устойчивость. По законам классической электродинамики, движущийся с ускорением заряд должен излучать электромагнитные волны, уносящие энергию. За короткое время (порядка 10–8 с) все электроны в атоме Резерфорда должны растратить всю свою энергию и упасть на ядро (рис. 4.) То, что этого не происходит в устойчивых состояниях атома, показывает, что внутренние процессы в атоме не подчиняются классическим законам.
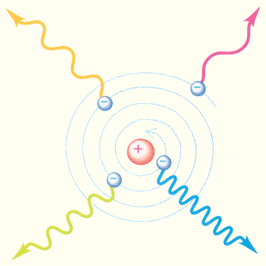
Рисунок 4.
Неустойчивость классического атома.
2.3. Квантовые постулаты Бора.
Следующий шаг в развитии представлений об устройстве атома сделал в 1913 году выдающийся датский физик Н. Бор. Проанализировав всю совокупность опытных фактов, Бор пришел к выводу, что при описании поведения атомных систем следует отказаться от многих представлений классической физики. Он сформулировал постулаты, которым должна удовлетворять новая теория о строении атомов.
Первый постулат Бора (постулат стационарных состояний) гласит: атомная система может находится только в особых стационарных или квантовых состояниях, каждому из которых соответствует определенная энергия En. В стационарных состояниях атом не излучает.
Этот постулат находится в явном противоречии с классической механикой, согласно которой энергия движущегося электрона может быть любой. Он находится в противоречии и с электродинамикой, так как допускает возможность ускоренного движения электронов без излучения электромагнитных волн. Согласно первому постулату Бора, атом характеризуется системой энергетических уровней, каждый из которых соответствует определенному стационарному состоянию
Второй постулат Бора (правило частот) формулируется следующим образом: при переходе атома из одного стационарного состояния с энергией En в другое стационарное состояние с энергией Em излучается или поглощается квант, энергия которого равна разности энергий стационарных состояний (рис. 5):
