Нильс БорРефераты >> Естествознание >> Нильс Бор
Анализируя системы, в которых вокруг положительно заряженного ядра вращается большее число электронов, Бор пришел к выводу, что устойчивой конфигурацией электронов является такая конфигурация, которая представляет собой кольцо вокруг ядра.
Бор заложил основы теории строения атомов и молекул, но решил, что подробнее остановиться на них во второй части своей статьи. Бор писал одному из друзей: "Боюсь, что мне следует торопиться с опубликованием, если я хочу представить что-то новое; эта проблема является в высшей степени актуальной".
Вторая часть статьи "Строение атомов и молекул" называлась "Системы, содержащие только одно ядро".
На основе идеализированной модели Бор предположил, что электроны вращаются вокруг ядра по коаксиальным орбитам. Но сколько электронов находятся на каждой орбите, как располагаются сами орбиты и каким образом их конфигурации определяют химические свойства элементов?
Если к единственному электрону атома водорода прибавить еще один электрон, рассуждал Бор, то оба электрона будут вращаться вокруг ядра, образовав элемент гелий. В этом случае орбита будет заполнена и тенденция к приобретению еще одного электрона исчезнет. И действительно, гелий - инертный газ, не вступающий в соединения с другими элементами.
Но если ядро с зарядом в три единицы притянет к себе третий электрон, то этот дополнительный электрон займет свою собственную орбиту, внешнюю по отношению к первоначальной орбите, занятой двумя электронами.
Предположение о ядре, окруженном кольцами с размещенными на них электронами, позволяло решить еще одну важную проблему. При переходе электрона с одной из внешних орбит сопровождающее этот процесс выделение энергии в виде излучения воспроизведет обычный линейный спектр элемента - характерные для него спектральные линии.
"По аналогии можно предположить, - продолжал Бор, - что характеристическое рентгеновское излучение возникает при переходе системы, у которой электроны внутренних орбит выбиты с помощью какой-то внешней силы, скажем воздействием катодных частиц, в равновесное состояние".
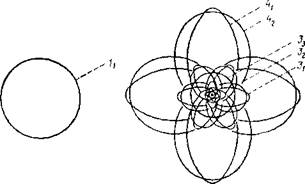
Слева - атом водорода со своим одним электроном. Справа - многочисленные орбиты атома криптона, у которого тридцать шесть электронов.
С радиоактивностью дело обстояло хуже. Это явление не могло быть объяснено излучением энергии электронами, вращающимися вокруг ядра. Бор утверждал, что в рамках атома Резерфорда допустимо только одно объяснение: источником альфа-лучей является ядро.
Кроме того, бору казалось совершенно ясным, что ядро является также источником излучения быстрых бета-частиц.
"Эта точка зрения на происхождение альфа- и бета-частиц с необычайной простотой объясняет, каким образом изменение химических свойств радиоактивных веществ связано с природой испускаемых частиц. Результаты экспериментов могут быть выражены двумя правилами:
1. Всякий раз, когда излучается альфа-частица, образующийся элемент переходит в группу, на две единицы меньшую, чем группа периодической системы, к которой принадлежал исходный элемент.
2. Всякий раз, когда излучается бета-частица, группа периодической системы, к которой принадлежит образующийся элемент, на единицу больше группы, в которой находится исходный элемент".
Именно это доказывал произведенный Бором анализ структуры атомов. Эксперимент и теория не просто согласовывались, они согласовывались с точностью, превосходящей все ожидания.
Итак, молекула является комбинацией двух или более атомов и образуется двумя отделенными друг от друга ядрами и их электронами. Бор начал свои исследования с простейшего случая - он рассмотрел два ядра, каждое из которых имело всего по одному электронному кольцу. Он доказал, что при сближении двух атомов друг с другом соприкасаются только их внешние электронные оболочки. Внутренняя часть атомов при соединении их в молекулу изменениями не подвергается.
"Основная часть электронов должна размещаться вокруг своего ядра примерно так, как если бы другое ядро отсутствовало, - говорил Бор. - Всего лишь несколько электронов будут располагаться по-новому, вращаясь по круговой орбите, охватывающей оба ядра. Новое электронное кольцо, удерживающее всю систему, и является химической связью".
Таким образом, молекула в гениальном воображении ученого превратилось в доступные объяснению организованные комбинации микроскопических солнечных систем, в которых вокруг ядер по орбитам, расположенным во многих плоскостях, вращаются электроны.
В заключении к трем статьям - трилогии, как их вскоре стали называть, - Бор суммировал основные идеи своей теории. Он использовал гипотезу Планка для объяснения атома Резерфорда и при этом выдвинул собственные гипотезы относительно испускания и поглощения излучения атомной системой. Гипотезы эти сводятся к следующему:
1. Поглощение и излучение энергии происходит непрерывно, как предполагала классическая физика прошлого, а только во время перехода систем из одного "стационарного" состояния в другое.
2. Хотя равновесие систем в их стационарном состоянии описывается обычными законами механики, эти законы неприменимы в момент перехода систем из одного стационарного состояния в другое.
3. Излучение испускается в виде одной неделимой порции - кванта Планка.
4. Стационарные состояния определяются испусканием энергии и вращением электрона.
5. Устойчивым состоянием любой атомной системы является такое состояние, при котором излучаемая энергия максимальна.
"Атом" Бора не приняли многие физики старой школы, однако игнорировать его они не могли. Хотели они того или нет, три статьи Бора изменили физику. Это изменение можно сравнить с тем, что было внесено в науку открытием ядра атома, сделанным Резерфордом двумя годами раньше.
Так родилась атомная физика, вошедшая в жизнь в наши дни. Чтобы оценить масштабы революции, произведенной Бором, потребовалось время, но независимо ни от чего революция эта произошла, и это непреложный факт.
МАНЧЕСТЕР ВОЕННОГО ВРЕМЕНИ И ОРБИТЫ.
Произошла революция в понимании физики. И хотя никто из физиков в то время не мог предположить, что она изменит политическую структуру мира и потрясет основы жизни, многие чувствовали, что изменения эти весьма глубоки и наука вступает в новую эру.
Правда, мало кто предполагал или верил и в то, что надвигается другое событие, которое перевернет мир, - война.
И тем не менее "вооруженный мир" продолжал существовать. По мере приближения весны Нильс и Маргрет Бор мирно строили планы на будущее. Нильсу было всего 29 лет, но он уже был признанным ученым; его квантовая теория атома внесла коренные изменения в физику. Бору предложили должность профессора кафедры теоретической физики Копенгагенского университета.
Бор подал заявление 4 марта 1914 года. За день до этого он написал Резерфорду, рассказав о своих планах, и попросил рекомендацию, которую то давно обещал. Восторженная и внушительная рекомендация Резерфорда прибыла следующей же почтой. Но она не понадобилась. Все отлично понимали, что квалификация Бора не вызывает сомнений, и а Копенгагенском университете впервые была создана самостоятельная кафедра теоретической физики.
