Влияние физических и химических факторов на основность алкиламинов
![]() В0Н+ + В В0 + ВН + (1)
В0Н+ + В В0 + ВН + (1)
Наличие свободной энергии этого процесса характеризует основность амина В относительно стандарта В0. Абсолютная основность (В0), равная отрицательной свободной энергии (DG0) процесса (8), может быть рассчитана, если известно соответствующее
В + Н+=ВН+ (2)
абсолютное значение для стандартного основания. Энтальпия (DH0) процесса (8), взятая с обратным знаком, характеризует сродство аминов к протону (РА) и легко рассчитывается, так как для прото-нирования аммиака, обычно принимаемого за стандарт, она определена независимыми методами [139, 143, 148, 149, 150]. Абсолютные значения 0В и РА* зависят от выбранного стандарта и абсолютной величины РА для него (например, для аммиака значение РА изменяется достаточно широко: 200,7 [139]; 201,4 [151]; 202,3 ± 2,0 [152]; 207 ± 3 [143, 148, 150, 153], 211,3 [149]; 214,4 [45]). Поэтому для выяснения количественных закономерностей влияния структуры аминов на их основность в газовой фазе лучше всего пользоваться величинами DGB (или — dRDG0 [3,7, 47]), когда за стандарт выбран аммиак**.
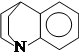
В табл.1 приведены величины DGB известного к началу 1977 г. ряда аминосоединений. Сопоставление этих данных показывает, что поведение различных аминов как оснований в газовой фазе резко отличается от такового в конденсированных средах. Например, анилин (табл. 1, № 31) в газовой фазе оказался на 6,7 ккал/моль (или почти на 5 ед. рКа) более основным, чем аммиак (№ 1), в то время как в воде, нитрометане и ацетонитриле (см. выше) наблюдается противоположная ситуация. Аналогичная картина имеет место и для пиридина, который в конденсированной фазе примерно на 4 ед. рКа менее основен, а в газовой фазе (№ 80) на 16 ккал/моль (или ~ на 12 ед. рКа) более основен, чем аммиак; для ацетамида (№ 32), который в воде ~ на 10 ед. рКа менее основен по сравнению с аммиаком, а в газовой фазе практически равен ему; для пиррола (№ 54) и некоторых других аминосоединений.
Таблица 1. Значения основностиа аминосоеденений в газовой фазеб относительно аммиака
| Номер | Амин | DGBг) | ||||
| 1 | NH3 | 0,0 | ||||
| 2 | CH3NH2 | 9,1 | ||||
| 3 | C2H5NH2 | 11,8 | ||||
| 4 | n-C3H7NH2 | 13,0 | ||||
| 5 | i-C3H7NH2 | 14,1 | ||||
| 6 | n-C4H9NH2 | 13,5 | ||||
| 7 | i-C4H9NH2 | 14,0 | ||||
| 8 | s-C4H9NH2 | 15,2 | ||||
| 9 | t-C4H9NH2 | 16,1 | ||||
| 10 | n-C5H11NH2 | 13,4д) | ||||
| 11 | t-C5H11NH2 | 17,4 | ||||
| 12 | n-C6H13NH2 | 13,5д) | ||||
| 13 | n-C7H15NH2 | 13,6д) | ||||
| 14 | c-C6H11NH2 | 16,3 | ||||
| 15 | NH2-NH2 | 3,8 | ||||
| 16 | NH2(CH2)2NH2 | 19,0д) | ||||
| 17 | NH2(CH2)3NH2 | 24,5д) | ||||
| 18 | NH2(CH2)4NH2 | 27,1д) | ||||
| 19 | NH2(CH2)5NH2 | 25,4д) | ||||
| 20 | NH2(CH2)6NH2 | 25,4д) | ||||
| 21 | NH2(CH2)7NH2 | 25,2е) | ||||
| 22 | CH3O(CH2)2NH2 | 14,7д) | ||||
| 23 | H2C=CH-CH2NH2 | 11,3 | ||||
| HCºC-CH2NH2 | 6,7 | ||||
| 25 | NCCH2CH2NH2 | 3,0 | ||||
| 26 | CF3(CH2)3NH2 | 10,1 | ||||
| 27 | FCH2CH2NH2 | 8,0 | ||||
| 28 | CF3(CH2)2NH2 | 6,7 | ||||
| 29 | F2CHCH2NH2 | 4,0 | ||||
| 30 | CF3CH2NH2 | -1,4 | ||||
| 31 |
| 6,8 | ||||
| 32 | CH3CONH2 | 0,2ж) | ||||
| 33 | HCONH2 | -7,1з) | ||||
| 34 | (CH3)2NH | 15,5 | ||||
| 35 | CH3NHC2H5 | 17,9 | ||||
| 36 | (C2H5)2NH | 20,2 | ||||
| 37 | (n-C3H7)2NH | 22,2 | ||||
| 38 | (i-C3H7)2NH | 23,9 | ||||
| 39 | (n-C4H9)2NH | 23,1 | ||||
| 40 | (i-C4H9)2NH | 23,6 | ||||
| 41 | (s-C4H9)2NH | 25,8 | ||||
| 42 |
| 11,2 | ||||
| 43 |
| 18,0 | ||||
| 44 |
| 20,1 | ||||
| 45 |
| 21,2 | ||||
| 46 |
| 19,2д) | ||||
| 47 |
| 14,4д) | ||||
| 48 | (H2C=CHCH2)2NH | 19,3 | ||||
| 49 | (HCºCCH2)2NH | 11,7 | ||||
| 50 | NCCH2NHCH3 | 2,7з) | ||||
| 51 | CF3CH2NHCH3 | 6,2з) | ||||
| 52 |
| 12,9 | ||||
| 53 |
| 15,3ж) | ||||
| 54 |
| 4,0ж) | ||||
| 55 | NHMe-C=O H | 1,7 | ||||
| 56 | (CH3)3N | 20,0 | ||||
| 57 | (CH3)2NC2H5 | 22,4 | ||||
| 58 | (C2H5)2NCH3 | 24,6 | ||||
| 59 | (C2H5)3N | 26,7 | ||||
| 60 | (C3H7)3N | 28,7 | ||||
| 61 |
| 17,1и) | ||||
| 62 |
| 8,1и) | ||||
| 63 |
| 24,3 | ||||
| 64 |
| 25,7 | ||||
| 65 |
| 27,1 | ||||
| 66 |
| 26,1к) | ||||
| 67 | (CH3)2N-NH2 | 15,2 | ||||
| 68 | ((CH3)2NCH2)2 | 30,3 | ||||
| 69 |
| 23,5 | ||||
|
| ||||||
| 70 | (H2C=CH-CH2)3N | 24,7 | ||||
| 71 | (HCºC-CH2)3N | 15,0 | ||||
| 72 | NCCH2N(CH3)2 | 7,1 | ||||
| 73 | F3CCH2N(CH3)2 | 20,9 | ||||
| 74 |
| 19,5 | ||||
| 75 |
| 21,0ж) | ||||
| 76 |
| 23,7ж) | ||||
| 77 |
| 19,3 | ||||
| 78 |
| 21,8 | ||||
| 79 |
| 26,0 | ||||
| 80 |
| 16,0 | ||||
| 81 | CH3CON(CH3)2 | 11,7 | ||||
| 82 | HCON(CH3)2 | 7,6 | ||||
| 83 | NF3 | -56л) |