Вычисление теплового эффекта реакций
число 3,14.
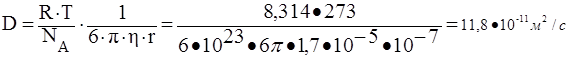
![]()
ответ на второй вопрос задания:
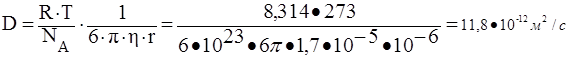
![]()
Таким образом, средний сдвиг частицы уменьшиться в 10 раз.
Ответ: ![]() , уменьшится в 10 раз.
, уменьшится в 10 раз.
80. Адсорбция ионов на твердой поверхности. Понятие об ионитах. Обратимая ионообменная адсорбция – основа ионообменной хроматографии.
Физические процессы молекулярной адсорбции на твердой поверхности описываются уравнениями Ленгмюра и Фрейндлиха.
Уравнение Ленгмюра:
![]() ,
,
где Г – величина адсорбции, кмоль/кг или кмоль/м2;
Гmax – величина предельной адсорбции, кмоль/кг (кмоль/м2);
С – концентрация раствора, кмоль/л;
а – константа равновесия адсорбции.
Это уравнение хорошо описывает адсорбцию для малых и больших концентраций растворов (или давлений газа).
Эмпирическое уравнение Фрейндлиха:
![]() ,
,
где Г – величина адсорбции, кмоль/кг (кмоль/м2);
n – количество вещества-адсорбтива, кмоль;
m – масса адсорбента, кг;
К – константа (при С = 1 моль/л К = Г);
1/а – константа (адсорбционный показатель); зависит от природы адсорбента и температуры. 1/а = 0,1–1.
Адсорбционная хроматография основана на различии сорбируемости разделяемых веществ адсорбентом (твёрдое тело с развитой поверхностью); распределительная хроматография — на разной растворимости компонентов смеси в неподвижной фазе (высококипящая жидкость, нанесённая на твёрдый макропористый носитель) и элюенте (следует иметь в виду, что при распределительном механизме разделения на перемещение зон компонентов частичное влияние оказывает и адсорбционное взаимодействие анализируемых компонентов с твёрдым сорбентом).
Ионообменная хроматография основана на различии констант ионообменного равновесия между неподвижной фазой (ионитом) и компонентами разделяемой смеси.
Если на поверхности адсорбента уже адсобирован электролит, то при контакте этого адсорбента с другим электролитом почти всегда в той или иной степени происходит ионообменная адсорбция. Она наблюдается на поверхности с достаточно выраженным двойным электрическим слоем. Подвижные противоионы электрического слоя способны обмениваться на другие ионы того же знака, находящиеся в растворе.
Количественное описание ионообменного процесса (обратимость процесса, эквивалентность обмена, порядок обмена ионов) было сделано Гедройцем уже в начале XXв. Вещества, проявляющие способность к ионному обмену и используемые для адсорбции ионов, получили название ионообменников или ионитов.
Иониты имеют каркасную структуру, «сшитую» ковалентными связями. Каркас (матрица) обладает положительным или отрицательным зарядом, который скомпенсирован противоположным зарядом подвижных ионов – противоионов, находящихся в адсорбционной и диффузной частях двойного электрического слоя. Противоионы могут заменяться на другие ионы из раствора с зарядом того же знака, а каркас выступает в роли полииона и обусловливает нерастворимость ионита в растворителе.
Иониты делятся по составу на органические и неорганические, по происхождению – на природные и синтетические, по характеру обмениваемых ионов – на катиониты, аниониты и амфолиты.
Из природных неорганических катионитов чаще используются кристаллические силикаты типа цеолитов: шабазит, глакуонит и др. их каркас состоит из сетчатой структуры алюмосиликатов, в порах которой расположены ионы щелочных или щелочноземельных металлов, являющихся противоинами. К природным ионитам относятся апатиты.
Природные органические иониты – гумусовые вещества почв, содержащие карбоксильную группу, способную к ионному обмену. составляющие почву вещества обладают амфотерными свойствами и поэтому в зависимости от условий могут обменивать как катионы, так и анионы. Однако широкого применения природные иониты не имеют ввиду химической нестойкости и небольшой обменной емкости.
Промышленное применение имеют синтетические иониты, и среди них наиболее широко используют ионообменные смолы, которые имеют сетчатую структуру и содержат ионогенные группы: - OH, COOH, SO3H, - COONa и т.п.
89. Написать формулу строения мицеллы золя, образованного в результате взаимодействия указанных веществ(избытка одного, затем другого вещества): CdCl2 + Na2S; FeCl3 + NaOH. Назвать составляющие компоненты мицеллы.
1) CdCl2 + Na2S
Избыток CdCl2 дает мицеллу:
[ (CdCl2 ) Cd2+ · Cl–]+ x Cl–
![]()
зародыш: (CdCl2 )
![]()
ядро: [ (CdCl2 ) Cd2+
![]()
гранула: [ (CdCl2 ) Cd2+ · Cl–]+
Избыток Na2S дает мицеллу:
[2 (NaCl) 2 Cl– · Na+]– x Na+
зародыш: (NaCl )
![]()
ядро: (NaCl ) 2 Cl-
![]()
гранула: [ (CdCl2 ) Cd2+ · Cl–]+
2) FeCl3 + NaOH
Избыток FeCl3 дает мицеллу:
[ (FeCl3 ) Fe3+ · 2Cl–]+ x Cl–
зародыш: (FeCl3 )
ядро: (FeCl3 ) Fe3+
гранула: [ (FeCl3 ) Fe3+ · 2Cl–]+
Избыток NaOH дает мицеллу:
[3 (NaCl) 3 Cl– · 2Na+]– x Na+
зародыш: (NaCl )
ядро: 3 (NaCl) 3 Cl–
гранула: [3 (NaCl) 3 Cl– · 2Na+]–
98. Коагуляция дисперсной системы. Скорость коагуляции. Причины, вызывающие процесс самопроизвольной коагуляции.
Коагуляция – процесс самопроизвольного укрупнения (слипания) дисперсных частиц, который может происходить при действии на дисперсную систему различных факторов: при интенсивном перемешивании или встряхивании, нагреве или охлаждении, облучении светом или пропускании электрического тока, при добавлении к системе электролитов или неэлектролитов и др. При разных способах воздействия на систему происходит уменьшение энергии связи диспергированных частиц с окружающей их дисперсионной средой. Так, добавление электролита вызывает сжатие диффузного слоя в коллоидной частице, следовательно, понижение величины электрокинетического потенциала. Это приводит к уменьшению электростатического отталкивания коллоидных частиц и, как следствие, к большей вероятности их слипания.
Минимальная концентрация электролита, добавляемого к дисперсной системе, при которой наступает явная коагуляция за определенный промежуток времени, носит название порога коагуляции ![]() . Порог коагуляции определяется температурой, природой добавленного электролита, знаком заряда добавляемого иона (действует прежде всего ион, имеющий заряд, противоположный заряду коллоидных частиц) и величиной заряда этого иона. Так, для трех-, двух- и однозарядных ионов явная коагуляция наступает при концентрации электролитов в соотношении 1:10 - 50: 500-1000 (приближенное правило Шульце-Гарди).
. Порог коагуляции определяется температурой, природой добавленного электролита, знаком заряда добавляемого иона (действует прежде всего ион, имеющий заряд, противоположный заряду коллоидных частиц) и величиной заряда этого иона. Так, для трех-, двух- и однозарядных ионов явная коагуляция наступает при концентрации электролитов в соотношении 1:10 - 50: 500-1000 (приближенное правило Шульце-Гарди).
