Дискриминация гипотез по кинетическим экспериментам
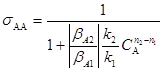 (6)
(6)
Поскольку ![]() , то из уравнения (6) следует, что sАА будет не зависеть от XA при n2 = n1, расти с увеличением XA при n2 > n1 и падать с ростом XA при n2 < n1.
, то из уравнения (6) следует, что sАА будет не зависеть от XA при n2 = n1, расти с увеличением XA при n2 > n1 и падать с ростом XA при n2 < n1.
Как видно из уравнений (5) и (6) при анализе зависимостей sik от Ck (XA) мы имеем дело с изменением отношения скоростей реакций (или сумм отношений скоростей в более сложных случаях). Отношения скоростей в многомаршрутных процессах с линейными механизмами в стационарных и квазистационарных условиях всегда существенно проще, чем выражения для Rp, поскольку многочленные полиномы, стоящие в знаменателе кинетических уравнений (![]() ) при этом сокращаются. Рассмотрим этот вопрос подробнее.
) при этом сокращаются. Рассмотрим этот вопрос подробнее.
Анализ узлов сопряжения
Все интермедиаты в реакционной сети, которые превращаются по двум и более стадиям, не считая обратной стадии образования интермедиата, образуют так называемые узлы сопряжения. Простейший узел – параллельно-последовательная реакция
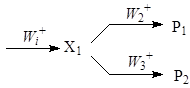
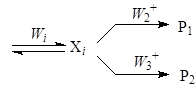
Более сложный узел включает дополнительные интермедиаты:
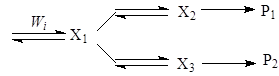
Во всех случаях отношение R1/R2 намного более информативно для целей дискриминации, чем сами скорости R1 и R2.
Рассмотрим узел сопряжения (7)
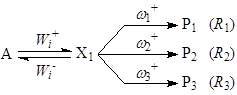 , (7)
, (7)
где wj – веса стадий j.
В стационарных условиях
![]()
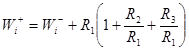
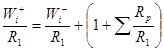
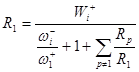 (8)
(8)
В уравнение (8) входит скорость образования X1, отношение весов ![]() при постоянных концентрациях, входящих в
при постоянных концентрациях, входящих в ![]() и переменная сумма
и переменная сумма ![]() , которая меняется в зависимости от
, которая меняется в зависимости от ![]() и
и ![]() . Выполнимость уравнения (8)
. Выполнимость уравнения (8)
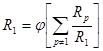
может служить подтверждением схемы (7) и позволяет найти ![]() и
и ![]() .
.
Другой вариант анализа схемы (7):
![]() (9)
(9)
Поскольку ![]()
![]() . Тогда
. Тогда
![]() , откуда
, откуда
![]() или (10)
или (10)
![]() (11)
(11)
(при сохранении концентраций, входящих в ![]() и
и ![]() постоянными).
постоянными).
Пример. Изучали реакцию
![]() (12)
(12)
в системе CuCl (3 – 9![]() ) – NH4Cl – HCl – H2O в условиях высокого катионного фона ([NH4+] = 12
) – NH4Cl – HCl – H2O в условиях высокого катионного фона ([NH4+] = 12![]() ) в безградиентом проточном реакторе при поддержании постоянными активностей Cu+ и Cl– и концентраций каталитически активных комплексов CumCln(n – m)–. При добавлении в этот раствор CuCl2 (5·10–3 – 170·10–3 М) скорость образования винилхлорида RВХ понижается, и появляются два продукта окислительного хлорирования ацетилена – 1,2-дихлорэтилен (ДХЭ) и винилиденхлорид (ВДХ):
) в безградиентом проточном реакторе при поддержании постоянными активностей Cu+ и Cl– и концентраций каталитически активных комплексов CumCln(n – m)–. При добавлении в этот раствор CuCl2 (5·10–3 – 170·10–3 М) скорость образования винилхлорида RВХ понижается, и появляются два продукта окислительного хлорирования ацетилена – 1,2-дихлорэтилен (ДХЭ) и винилиденхлорид (ВДХ):
![]() (13)
(13)
![]() , (14)
, (14)
скорости образования которых RДХЭ и RВДХ проходят через максимум по мере увеличения [CuCl2]. При малых [CuCl2] наблюдается слабый рост ВХ от [CuCl2]. Для создания стационарного режима по [CuCl2] концентрацию Cu(II) поддерживали постоянной, окисляя Cu(I) электрохимически в ходе реакции. Скорость синтеза ВХ до добавления CuCl2 описывается простым уравнением
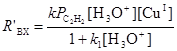 (15)
(15)
в соответствии со схемой механизма
![]() (16)
(16)
Падение RВХ при добавлении CuCl2 говорит о взаимной связи процессов (12), (13) и (14) и о наличии узла сопряжения.
Первая гипотеза о простом узле сопряжения стадий образования ВХ и ДХЭ позволяет рассмотреть отношение RДХЭ и RВХ.
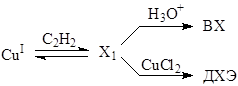
Зависимость отношения RДХЭ/RВХ от [CuCl2] при постоянных остальных параметрах системы описывается уравнением (16)
![]() . (16)
. (16)
Второй вариант узла сопряжения связывает ВДХ и ВХ.
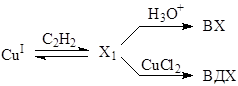
Отношение RВДХ/RВХ = f [CuCl2] описывается более сложной зависимостью, простейший вид которой подчиняется уравнению (17)
![]() . (17)
. (17)
Квадрат по концентрации CuCl2 в числителе уравнений (16) и (17) свидетельствует о последовательном участии двух молекул CuCl2 в стадиях окисления Х1 до ДХЭ и ВДХ
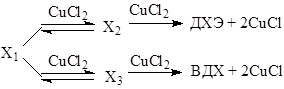 (18)
(18)
При этом стадия образования Х2 квазиравновесна (16), а стадия образования Х3 – нет (17). Чтобы найти выражение для RВХ, RДХЭ и RВДХ не хватает еще одного уравнения. Воспользуемся зависимостью (11). Эксперимент показал, что выполняется линейное соотношение (11) в форме уравнения (19) при варьировании [CuCl2]
![]() (19)
(19)
Решение системы (16), (17) и (19) дает уравнения (при [H3O+] = const)
![]() (20)
(20)
![]() (21)
(21)
![]() (22)
(22)
![]() (23)
(23)
Уравнения (20 – 23) описывают экспериментальные зависимости Rp = f([CuCl2]) и соотношение скоростей Rp.
Исследования различных модельных реакций и отклонение других гипотез образования ВДХ, например, через ClCºCH
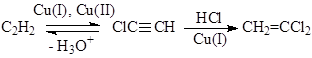
позволило предложить механизм с участием s-металлоорганических соединений Cu(I) и Cu(II)
