Исследование уравнений реакций
CH3COO - + K++H++Cl – =CH3COОН + K+ +Cl -, слабый элетролит CH3COОН
CH3COO - + H+ =CH3COОН
7. Чему равна величина ЭДС гальванического элемента, составленного из стандартных цинкового и серебряного электродов, погруженных в растворы их солей? Приведите схему гальванического элемента и реакции, и реакции протекающие на электродах при его работе
Схема гальванического элемента:
(–) Zn | Zn2+ || Ag+ | Ag (+)
На аноде протекают реакции: Zn0-2e=Zn2+
На катоде протекают реакции: Ag++e=Ag0
Т.к. потенциал Е0(Ag)> Е0(Zn)
Е0(Ag+ |Ag)= +0,80В
Е0(Zn2+ | Zn)= -0,763В
то на серебряном электроде будет протекать восстановление (будет являться катодом), а на цинковом электроде будет протекать окисление (он будет анодом);
Потенциал гальванического элемента:
Е = Е0катода – Е0анода =0,80 – (-0,763)=1,562В
Ответ: 1,562 В.
8. Изделие из алюминия склёпано медью. Какой из металлов будет подвергаться коррозии с водородной деполяризацией, если эти металлы попадут в кислую среду (HCl)? Составьте уравнения проходящих при этом процессов, приведите схему образующегося гальванического элемента. Определите продукты коррозии
В реакциях с кислотами атомы алюминия окисляются ионами водорода в ионы алюминия, которые переходят в раствор:
2Al+6H+→2Al3+ +3H2h
Медь в электрохимическом ряду напряжения металлов находится за водородом, (т.е. её стандартный потенциал положительный) и с разбавленными кислотами не реагирует (положительно заряженные ионы меди не переходят в раствор).
В кристаллической решетке меди (в отличие от алюминия) свободные электроны не накапливаются. При соприкосновении этих двух металлов свободные электроны алюминия переходят к меди и восстанавливают на её поверхность ионы водорода:
2H+ +2e→H2h
Продуктами коррозии будет являться результат взаимодействия алюминия с соляной кислотой:
2Al+6HCl→2AlCl3+3H2h
Образуется гальванический элемент:
(–) Al |AlCl3|Cu(+)
Анод катод.
9. При электролизе водных растворов каких из приведённых ниже веществ на катоде выделяется только металл: хлорид бария, хлорид меди (II), иодид калия, нитрат серебра, сульфид натрия? Приведите соответствующие уравнения электродных процессов
При электролизе водных растворов катионов металлов, у которых стандартный электродный потенциал больше чем водорода (Е0>>-0,41В) на катоде восстанавливаются только катионы металлов. В данном случае это хлорид меди (II) и нитрат серебра:
|
(–) Катод
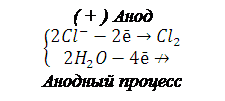
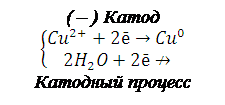
 |
Суммарный процесс электролиза:
![]()
Суммарный процесс электролиза:
![]()
Суммарное молекулярное уравнение электролиза:
![]() .
.
Библиографический список
1. Будякк Е.В. Химия: учеб. пособие Иркутск: Изд-во ИрГТУ, 2008. – 160 с.
2. Коровин Н.В. Общая химия. М. Высш. шк., 2002. 558 с.
3. Кузнецова А.А. Химия: метод. указания по освоению дисциплины для студентов заочной формы обучения. Иркутск: Изд-во ИрГТУ, 2010. 44 с.
4. Химия: метод. указания, программа, решение типовых задач и контрольные задания для студентов заочного обучения технических направлений и специальностей / сост.: В.И. Дударев, В.П. Зуева, О.В. Лебедева, Ю.Н. Пожидаев, З.Н. Топшиноева, А.Н. Шибанова. Иркутск: Изд-во ИрГТУ, 2007. 92 с.
