Несимметричные сульфиды
СОДЕРЖАНИЕ
1. Введение
2. Пространственно-затрудненные фенолы и стабилизация полимерных материалов
2.1. Старение полимеров
2.2. Пространственно-затрудненные фенолы, как ингибиторы радикальных процессов в полимерах.
3. Методы получения органических сульфидов
4. Пути синтеза несимметричных сульфидов на основе 4-(g-хлорпропил)-2-трет.-бутилфенола.
4.1. Получение 4-(g-хлорпропил)-2-трет.-бутилфенола (хлорид Ф-13)
4.2. Синтез 4-(g-меркаптопропил)-2-трет.-бутилфенола
4.3. Синтез 2,2'– метиленбис-[4-(g-меркаптопропил)-6-трет.-бутилфенола].
4.4. Синтез несимметричных сульфидов алкилированием 4-(g-меркаптопропил)-2-трет.-бутилфенола и 2,2`метиленбис-[4-(g-меркаптопропил)-6-трет.- бутилфенол] алкилгалогенидами в щелочном виде.
5. Практическая часть
5.1. Наработка 4-(g-хлорпропил)-2-трет.-бутилфенола (хлорид Ф-13)
5.2. Получение 4-(g-меркаптопропил)-2-трет.-бутилфенола
5.3. Получение 2,2'-метиленбис-[4-(g-меркаптопропил)-6-трет.-бутилфенола]
5.4. Взаимодействие 2,2'-метиленбис-[4-(g-меркаптопропил)-6-трет.-бутилфенола] бромистым бутилом (н-C4H9Br) в щелочной среде
5.5. Взаимодействие 2,2'-метиленбис-[4-(g-меркаптопропил)-6-трет.-бутилфенола] с йодистым этилом (C2H5J) в щелочной среде
5.6. Взаимодействие 4-(g-меркаптопропил)-2-трет.-бутилфенола с йодистым этилом (C2H5J) в щелочной среде.
5.7. Взаимодействие 4-(g-меркаптопропил)-2-трет.-бутилфенола с бромистым бутилом (н-C4H9Br) в щелочной среде.
6. Выводы
1. Введение
Полимерные вещества внедрились во все сферы человеческой деятельности – технику, здравоохранение, быт. Ежедневно мы сталкиваемся с различными пластмассами, резинами, синтетическими волокнами. Полимерные материалы обладают многими полезными свойствами: они высокоустойчивы в агрессивных средах, хорошие диэлектрики и теплоизоляторы. Некоторые полимеры обладают высокой стойкостью к низким температурам, другие - водоотталкивающими cвойствами и так далее.
Недостатками многих высокомолекулярных соединений является склонность к старению и, в частности, к деструкции – процессу уменьшению длины цепи и размеров молекул. Деструкция может быть вызвана механическими нагрузками, действий света, теплоты, воды и особенно кислорода и озона. Процесс уменьшения цепи идёт за счёт разрушения связей С-С и образования радикалов, которые в свою очередь, способствуют дальнейшему разрушению полимерных молекул.
Перед учёными стоит проблема продления срока службы полимерных изделий. Для предотвращения старения в полимерные материалы вводят различные добавки (стабилизаторы).
В качестве ловушек свободных радикалов, образующихся при деструкции полимерных материалов, используют фенольные стабилизаторы.
Фенольные стабилизаторы более эффективны, так как, улавливая свободные радикалы, образуют более устойчивые связи с ними, предотвращая дальнейшую деструкцию углеродной цепи. Кроме того, они обладают комплексным защитным действием (например, предотвращают разрушающее действие кислорода и высоких температур, или кислорода и радиации). Фенольные стабилизаторы выгодно отличаются от других добавок тем, что не изменяют цвет полимерных материалов, в состав которых вводятся.
В настоящее время в промышленном производстве полимеров требуются новые фенольные добавки с широким спектром стабилизирующих свойств и низкой себестоимостью. Несмотря на актуальность проблемы, исследований по разработке и получению фенольных стабилизаторов ведется мало. В связи с этим целью нашей работы был синтез новых серосодержащих пара-функционально-замещенных пространственно-затрудненных фенолов на основе 4-(g-хлорпропил)-2-трет.-бутилфенола и 2,2'-метиленбис-[4-(g-хлорпропил)-6-трет.-бутилфенола].
Основными задачами, которые требовалось решить в ходе исследования, являлись:
1. Изучить проблему старения полимеров и способов его предотвращения путем введения в материал фенольных стабилизаторов.
2. Ознакомиться с распространенными методами получения сульфидов.
3. Проверить возможности синтеза несимметричных сульфидов взаимодействием меркаптанов (4-(g-меркаптопропил)-2-трет.-бутилфенола и 2,2'-метиленбис-[4-(g-меркаптопропил)-6-трет.-бутилфенола]) с алкилгалогенидами в этиловом спирте.
2. Пространственно-затрудненные фенолы и стабилизация полимерных материалов
2.1. Старение полимеров
Полимерные материалы в значительной мере подвержены воздействию условий окружающей среды (свет, тепло, действие озона, радиация, механические нагрузки).Под влиянием этих факторов снижается эластичность, ухудшается электроизоляционные свойства и др. Эти явления, называемые в совокупности старением, приводят к необратимым изменениям свойств полимерных материалов и сокращают срок службы изделий из них. При эксплуатации большинство полимеров находится в контакте с кислородом воздуха, т.е. в окислительной среде. Реакции окислительной деструкции являются наиболее распространенными из реакций, протекающих при старении в естественных условиях, и представляют собой радикально-цепной окислительный процесс. Этот процесс активируется различными внешними воздействиями – тепловым, радиационным, механическим, химическим. Характерная особенность радикально-цепных окислительных процессов – возможность их резкого замедления путем введения небольшого количества ингибитора (стабилизатора).
Выделяют следующие типы стабилизаторов:
· антиоксиданты или антиокислители (защищающие полимерные вещества от разрушающего действия кислорода);
· антиозонаты (защищающие полимерные вещества от разрушающего действия озона);
· светостабилизаторы (защищающие полимерные вещества от разрушающего действия ультрафиолетовых лучей);
· термостабилизаторы (защищающие полимерные вещества от разрушающего действия высокой температуры);
· антирады (защищающие полимерные вещества от разрушающего действия радиационного излучения).
Как известно, основу макромолекулы большинства полимеров общего назначения составляет углеродная цепь типа:
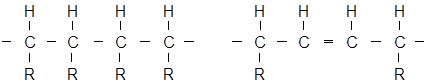
где: R = H, alk, ar.
В общем виде механизм ингибированного окисления углеводородов молекулярным кислородом может быть представлен следующей схемой:
Механизм ингибированного окисления углеводородов молекулярным кислородом
(0) RH ® R•
(1) R• + O2 ® ROO•
(2) ROO• + RH ® ROOH + R•
(3) ROOH ® RO• + HO•
(4) R• + R• ® R-R
(5) ROO• + R• ® ROOR
(6) ROO• + ROO• ® ROH + R"COR + O2
(7) ROO• + InH ® ROOH + In•
(8) In• + RH ® InH + R•
(9) In• + In• ® In-In
(10) In• + ROO• ® InOOR
В целом процесс окисления зависит от величины константы скорости реакции продолжения цепи (k2) и концентрации перекисных радикалов. Соответствующие гидроперекиси являются первичными продуктами окисления, дальнейший распад которых приводит к различным кислородсодержащим веществам и часто сопровождается разрывом углерод-углеродной цепи.
Присутствующий в окисляющейся системе ингибитор (InH), как правило, реагирует c радикалами ROO• (реакция 7), либо прерывая цепь окисления, либо уменьшая концентрацию этих радикалов, что приводит к снижению скорости окисления. Естественно, что чем менее активен получающийся из ингибитора радикал, тем меньше вероятность протекания реакции 8. Следовательно, тормозящее действие любого ингибитора окисления зависит, с одной стороны, от скорости реакции перекисных радикалов с ингибитором, а с другой – от активности получающегося из ингибиторов радикала. Малоактивные радикалы In• обычно не способны продолжать цепь (реакция 8) и рекомбинируют друг с другом (реакция 9). Таким образом, относительная активность радикала In• непосредственно в процессе окисления должна определяться отношением констант скоростей реакций k2/k7, которое характеризует максимальную возможность торможения процесса окисления при использовании данного ингибитора (сила ингибитора). Чем меньше это отношение, тем больше возможное тормозящее действие ингибитора.
