Одноосновные насыщенные карбоновые кислоты
Кислотные радикалы RCO- (ацилы) имеют следующие названия:
|
радикал муравьиной кислоты |
формил |
HCO- |
|
радикал уксусной кислоты |
ацетил |
CH3CO- |
|
радикал пропионовой кислоты |
пропионил |
CH3CH2CO- |
|
радикал масляной кислоты |
бутирил |
CH3CH2CH2CO- |
|
радикал валериановой кислоты |
валерил |
CH3CH2CH2CH2CO- |
Промышленные способы получения карбоновых кислот
1. Окисление углеводородов
Имеются два направления: окисление низших алканов С4-С8 преимущественно в уксусную кислоту и окисление твердого парафина в так называемые синтетические жирные кислоты (СЖК) с прямой цепью углеродных атомов С10-С20, являющихся сырьем для синтеза ПАВ.
Процесс протекает в жидкой фазе - термически или в присутствии катализаторов. При окислении алканов происходит деструкция по связям между вторичными углеродными атомами, поэтому из н-бутана образуется главным образом уксусная кислота, а в качестве побочных продуктов - метилэтилкетон и этилацетат.
2. Синтезы на основе оксида углерода
Карбоновые кислоты получают на основе оксида углерода реакциями карбоксилирования и карбонилирования:
CH2=CH2 + CO + H2O ® CH3CH2COOH
CH3CH2OH + CO ® CH3CH2COOH
Присоединение водорода и карбоксильной группы по двойной связи при кислотном катализе всегда протекает по правилу Марковникова, вследствие этого только из этилена получается неразветвленная кислота, а из его гомологов - a-метилзамещенные кислоты. Особый интерес данный метод представляет для синтеза третичных кислот (неокислот) из изоолефинов (реакция Коха):
(CH3)2C=CH2 + CO + H2O ® (CH3)3CCOOH
изобутилен триметилуксусная кислота
Механизм реакции состоит в предварительном протонировании алкена кислотой с образованием иона карбония, его взаимодействия с СО с получением ацилий-катиона и реакции последнего с водой с образованием карбоновой кислоты:
RCH=CH2 + H+ « RC+HCH3 + CO « RCH(CH3)C+O + H2O « RCH(CH3)COOH + H+
Неокислоты и их соли обладают очень высокой растворимостью и вязкостью, а их сложные эфиры - стабильностью к гидролизу, что обеспечивает им широкое применение в ряде отраслей.
Карбонилирование спиртов катализируется комплексами металлов (Ni, Co, Fe, Pd). Процесс реализован в промышленности для синтеза уксусной кислоты из метанола и характеризуется высокими экономическими показателями.
Кислоты также получают окислением альдегидов (продукт оксосинтеза).
Лабораторные способы получения карбоновых кислот
1. Окисление первичных спиртов см. Лекцию№21
2. Окисление альдегидов и кетонов
Альдегиды окисляются значительно легче, чем кетоны. Кроме того, окисление альдегидов приводит к образованию кислот с тем же числом углеродных атомов, в то время как окисление кетонов протекает с разрывом углерод-углеродных связей (образуются две кислоты или кислота и кетон):
CH3CHO + O2 ® CH3COOH + H2O
CH3CH2COCH2CH3 + O2 ® CH3COCH3 + CH3CH2COOH
Окислителями служат перманганат калия или бихромат. Окисление кетонов требует более жестких условий, чем альдегиды.
3. Гидролиз нитрилов
Нитрилы получают взаимодействием галогеналканов с цианистым калием, а затем подвергают их гидролизу водными растворами кислот или щелочей. В кислой среде азот выделяется в виде соли аммония:
CH3CN + 2 H2O + HCl ® CH3COOH + NH4Cl
R-CºN+H+®R-C+=NH+H2O®RC(O+H2)=NH«H+ + RC(OH)=NH « RCONH2
RCONH2 + HX + H2O ® RCOOH + NH4X;
в щелочной - в виде гидроксида аммония, кислота же получается в виде соли:
CH3CN + 2 H2O + KOH ® CH3COOK + NH4OH
RCºN + -OH ® RC(OH)=N- + H2O ® -OH + RC(OH)NH « RCONH2 + NaOH ® RCOONa + NH3
4. Синтез Гриньяра
При взаимодействии магнийорганических соединений с диоксидом углерода образуются соли карбоновых кислот:
CH3CH2MgBr + CO2 ® CH3CH2COO-Mg+Br
Под действием сильной кислоты (обычно HCl) соль превращается в кислоту:
CH3CH2COO-Mg+Br + HCl ® CH3CH2COOH + MgBrCl
5. Гидролиз жиров
Жиры и масла - сложные эфиры глицерина и высших жирных кислот. Как все сложные эфиры, жиры могут быть подвергнуты гидролизу (омылению) действием водных растворов щелочей, минеральных кислот или водяным горячим паром под давлением
химические свойства
Карбоновые кислоты, как и спирты, способны образовывать водородные связи. Если акцептором является достаточно сильное основание, образование водородной связи предшествует полному переносу протона к основанию. В этом случае донор водородной связи считают «кислотой». Будет ли данное соединение «донором водородной связи» или «кислотой», зависит от природы «акцептора водородной связи» или «основания». Чем сильнее основание, тем больше вероятность того, что данное соединение будет вести себя по отношению к нему как кислота:
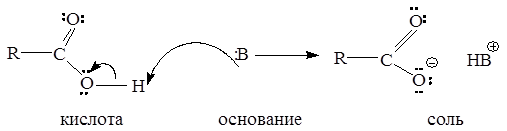
Межмолекулярные водородные связи, возникающие между молекулами карбоновых кислот, настолько прочны, что даже в газообразном состоянии значительная часть молекул существует в виде димеров:
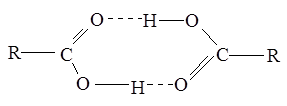
С ростом углеводородной цепи способность кислот к образованию водородных связей уменьшается.
Карбоновые кислоты обладают более выраженными кислотными свойствами, чем спирты, из-за стабилизации карбоксилат-аниона, вызванной делокализацией p-электронов. Другими словами, карбоксилат-ион стабилизирован вследствие резонанса:
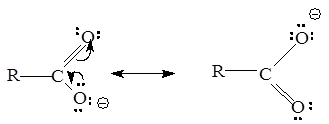
Степень делокализации изменяется в ряду RCOO- >>RCOOH >> ROH, RO-.
![]() RO- + +BH
RO- + +BH
 Энергия
Энергия
![]() RO-H + B
RO-H + B
RO-H + :B « RO- + +BH
![]() координата реакции
координата реакции
 |
![]()
 Энергия
Энергия
 | |||
 | |||
