Получение синтетических красителей реакцией азосочетания на примере синтеза 3-окси-4-карбоксиазобензола
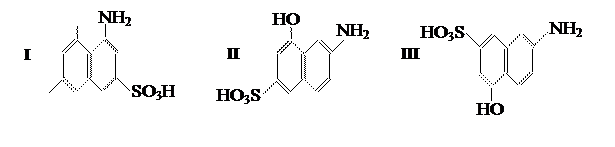

Обычно реакцию азосочетания ведут таким образом, чтобы к её концу в реакционной массе оставался незначительный избыток азосоставляющей и совершенно отсутствовало диазосоединение.
3.4. Механизм реакции азосочетания
Реакция азосочетания является классическим примером электрофильного замещения в ароматических соединениях. Эффектным электрофилом в данном случае является катион арилдиазония:
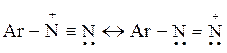
Он образуется в результате взаимодействия анилина с азотистой кислотой:
Однако, катион арилдиазония является более слабым электрофилом по сравнению с такими реагентами, как +NO2 и способен успешно атаковать только очень реакционноспособные ароматические соединения, такие как фенолы и амины.
Катионы диазония существуют только в кислой или слабощелочной среде, в сильнощелочном растворе они превращаются в кислоты. Поэтому реакция азосочетания может проводиться только в указанных условиях. Оптимальное значение pH зависит от свойств атакуемого соединения. В случае фенолов реакция лучше всего протекает в слабощелочной среде, поскольку образующийся фенолят-ион намного лучше атакуется, чем сам фенол из-за значительно более высокой электронной плотности.
Ароматические амины, как правило, атакуется несколько труднее, чем фенолы, поэтому сочетание с ними чаще всего проводят в слабокислом растворе, что обеспечивает высокую концентрацию иона.
Реакция азосочетания в общем виде:
Если X= ─![]() , ─
, ─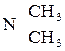 , сильно активирующие группы, азосочетание проходит успешно. Различия в поведении аминов и фенолов вызвано тем обстоятельством, что диазониевый ион эффективно атакует только свободный амин и фенолят-анион.
, сильно активирующие группы, азосочетание проходит успешно. Различия в поведении аминов и фенолов вызвано тем обстоятельством, что диазониевый ион эффективно атакует только свободный амин и фенолят-анион.
Аммониевые ионы солей аминов ─NH3, ─NH2R, ─NHR2 и свободный фенол практически не атакуются, так как вследствие слабой электрофильности диазониевого иона он может атаковать углерод ароматического кольца лишь при значительном содействии со стороны заместителя. Такое содействие выражено в случае ─O и ─N(CH3)2:
Очень медленно реакция идёт в случае фенола:
3.6. Продукты для холодного крашения
Во всех рассмотренных до сих пор примерах реакцию азосочетания вели в растворе, затем выделяли полученный краситель, фильтровали, высушивали и в готовом виде передавали на текстильные фабрики для крашения ткани. Существует и другой способ крашения ткани, при котором реакцию азосочетания проводят непосредственно на волокне. Для этого ткань пропитывают щелочным раствором азосоставляющей (например 2-нафтолом) а затем погружают в подкисленный раствор диазосоставляющей (например диазотированного п-нитроанилина). При этом краситель образуется непосредственно на волокне и полученная окраска обладает большой прочностью. Так как реакции диазотирования и азосочетания проводят при низких температурах, а в производстве это достигается охлаждением льдом, то способ этот получил название холодного или ледяного крашения.
Важнейшими азосоставляющими для холодного крашения являются производные β-оксинафтойной кислоты – азотолы. Их получают взаимодействием β-оксинафтойной кислоты с ароматическими аминами.
Азотолы легко переходят на волокно из щелочных растворов и прочно удерживаются на нём, что облегчает последующее сочетание их на волокне с диазосоединением.
Диазосоставляющие для холодного крашения выпускают в различных формах. Наиболее простая форма – азоамины – аминосоединения бензольного и нафталинового ряда. Название азоаминов включает цвет наиболее важного красителя, получаемого, из него в текстильной промышленности. Например азоамин красный Ж (п-нитроанилин), азоамин жёлтый О (о-хлоранилин).
В отличие от азотолов азоамины нельзя непосредственно применять для холодного крашения. Их сначала нужно перенести в форму диазосоединения, т.е. продиазотировать, причём обязательно на текстильной фабрике непосредственно перед крашением. Это объясняется неустойчивостью обычных форм диазосоединений и трудностью транспортировки. Поэтому большей частью диазосоединения перерабатывают сразу после диазотирования, не выделяя из раствора. Но специально для холодного крашения некоторые диазосоединения заготавливают в твёрдом виде или в виде паст, переводя их в различные стойкие формы, пригодные для хранения и транспортировки. Стойкие формы азосоединений называются диазолями.
Одна из таких форм – двойная соль диазосоединения с солями тяжёлых металлов, например хлористым цинком. Её получают добавлением хлористого цинка к раствору соли диазония. При последующем добавлении хлористого натрия двойная соль выпадает в осадок, её отфильтровывают и сушат при низкой температуре. Строение соли отвечает формуле ![]() . В некоторых случаях диазотирование ведут в среде серной кислоты; тогда двойная соль имеет строение
. В некоторых случаях диазотирование ведут в среде серной кислоты; тогда двойная соль имеет строение ![]() .
.
Таким образом, из азоамина жёлтого О получают диазоль жёлтый О:
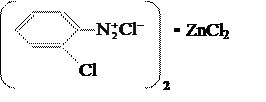

4. Экспериментальная часть
4.1. Синтез 4-окси-3-кабоксиазобензола
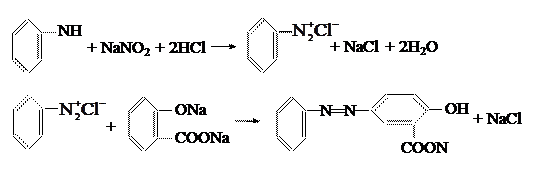

|
Анилин 9,3 г (9,1 мл) Соляная кислота (d=1,18) 22,5 мл Нитрит натрия 7 г Карбонат натрия 3 г |
Салициловая кислота 13,8 г Раствор едкого натра (36%-ный) 16,5 мл 2 фарфоровых стакана на 250 мл Мешалка |
В фарфоровом стакане на 150-200 мл растворяют 9,3 г анилина в смеси 22,5 мл концентрированной соляной кислоты и 22,5 мл воды. Раствор охлаждают до 0˚С и при перемешивании приливают к нему охлаждённый раствор 7 г нитрита натрия в 20 мл воды (при температуре не выше 2˚С). Конец реакции диазотирования контролируют по иодкрахмальной бумаге.
Через 10 мин после конца диазотирования избыток соляной кислоты удаляют осторожным внесением 2 г соды, после чего раствор должен всё же давать слабокислую реакцию на конго.
Раствор диазосоединения при перемешивании постепенно приливают к охлаждённому до 0˚С раствору 13,8 г салициловой кислоты в 16,6 мл 36%-ного едкого натра и 35 мл воды, к которому добавлено ещё 1 г соды (температура должна поддерживаться не выше 5˚С). Через 2 ч выпавший моноазокраситель отделяют фильтрованием.
Характеристика исходных реактивов
| № | Название | Формула | Мол. масса | ρ, г/см3 | Т. пл., ˚С | Т.кип., ˚С |
| Растворимость | |
| в воде | в орг. р-лях | ||||||||
| 1 | Анилин | C6H5NH2 | 93,13 | 1,02 | -6 | 184,4 | 1,585 | 3,4 | сп. э. бз. |
| 2 | Соляная кислота | HCl | 36,5 | 1,179 | - | - | - | - | - |
| 3 | Нитрит натрия | NaNO2 | 69,0 | 2,17 | 79 разл. | - | - | 84,5 | э. метанолабс. сп |
| 4 | Карбонат натрия | Na2CO3 | 105,9 | 2,53 | 851 | разл. | - | 21,5 | - |
| 5 | Салициловая кислота | HO-C6H4-COOH | 138,1 | 1,443 | 159 | возг. | - | 0,18 | сп. э. ац. хл. |
