Разработка энергосберегающих технологий процесса ректификации продуктов синтеза хлорбензола
![]() (4.6.2.)
(4.6.2.)
где ![]() – приведенная температура, Т/Тс
– приведенная температура, Т/Тс
![]() – ацентрический фактор
– ацентрический фактор
Константы в уравнении (4.6.2.) были получены из преобразования данных по паровому давлению для ограниченного числа обычных углеводородов. Эти пределы использования уравнения состояния СРК ограничены неполярными компонентами.
Уравнение состояния Соав-Редлих-Квонга – это модификация уравнения состояния Редлиха-Квонга (которое основано на уравнении Ван-дер-Ваальса). Соав заменил член ![]() более общей температурной зависимостью а(Т). Выражение получило следующий вид:
более общей температурной зависимостью а(Т). Выражение получило следующий вид:
![]() (4.6.3.)
(4.6.3.)
где ![]()
![]() (4.6.4.)
(4.6.4.)
![]() ,
, ![]() – критические температура и давление для i-го компонента
– критические температура и давление для i-го компонента
![]() (4.6.5.)
(4.6.5.)
![]() (4.6.6.)
(4.6.6.) ![]() (4.6.7.)
(4.6.7.)
![]() (4.6.8.)
(4.6.8.)
![]() (4.6.9.)
(4.6.9.)
![]() – ацентрический фактор для компонента i
– ацентрический фактор для компонента i
![]() – константа бинарного взаимодействия для компонентов i и j
– константа бинарного взаимодействия для компонентов i и j
Введение члена альфа позволило улучшить предсказание парового давления для чистых компонентов. Комбинированная формула для вычисления α(Т) с введенным членом ![]() означает улучшение предсказания свойств смеси.
означает улучшение предсказания свойств смеси.
Использование формулировки Соава для предсказания свойств смеси включает в себя два этапа. Во-первых, для каждого из компонентов подбирается ацентрический фактор компонента (wi) таким образом, чтобы точно предсказать давление паров компонента. Во-вторых, из экспериментальных данных для бинарных систем с компонентами i и j, для которых достигается фазовое равновесие, определяется параметр kij.
4.7. Модель Peng-Robinson
Уравнение состояния Пенга-Робинсона было опубликовано в 1976 году и является модификацией уравнения Редлиха-Квонга. Во многих отношениях оно похоже на уравнение SRK, но все же он разработано для улучшения предсказания плотности жидкости. Как и в случае уравнения Соава-Редлиха-Квонга, в уравнении Пенга-Робинсона присутствует температурная зависимость а(Т) и выражение имеет следующий вид:
![]() (4.7.1.)
(4.7.1.)
где: ![]() (4.7.2.)
(4.7.2.)
![]() (4.7.3.)
(4.7.3.)
![]() ,
, ![]() – критические температура и давление компонента i
– критические температура и давление компонента i
![]() (4.7.4.)
(4.7.4.)
![]() (4.7.5.)
(4.7.5.) ![]() (4.7.6.)
(4.7.6.)
![]() (4.7.7.)
(4.7.7.)
![]() (4.7.8.)
(4.7.8.)
![]() – ацентрический фактор для компонента i
– ацентрический фактор для компонента i
![]() – константа бинарного взаимодействия для компонентов i и j
– константа бинарного взаимодействия для компонентов i и j
Введением члена α было достигнуто улучшение предсказания давления пара чистых компонентов, а добавлением члена ![]()
![]() в комбинированную формулу для вычисления а(Т) означало улучшение предсказания свойств смесей.
в комбинированную формулу для вычисления а(Т) означало улучшение предсказания свойств смесей.
Использование уравнения Пенга-Робинсона включает в себя два шага, аналогичные предыдущей модели.
4.8. Групповые модели
Групповые модели основаны на предположении об аддитивности вкладов различных химических групп в термодинамические свойства компонентов и смесей. Наибольшее распространение получила модель UNIFAC. Именно её мы использовали для создания псевдоэкспериментальных данных парожидкостного равновесия. Рассмотрим модель более подробно.
4.8.1. Модель UNIFAC [44-48]
Метод UNIFAC (universal functional activity coefficient – универсальный функциональный коэффициент активности) был разработан в 1975 году Фреденслундом, Джонсом и Праузницем. Данный метод рассчитывает величины коэффициентов активности на основе концепции группового вклада. Предполагается, что взаимодействия между двумя молекулами являются функцией взаимодействий между группами. Данные межгруппового взаимодействия получаются путем обработки экспериментальных данных для пар компонентов. Число функциональных групп ограничено.
Метод UNIFAC основан на модели UNIQUAC, которая представляет избыточную энергию Гиббса (и логарифм коэффициента активности) как комбинацию двух эффектов. Таким образом, используется уравнение:
![]() (4.8.1.)
(4.8.1.)
Комбинационный член ![]() рассчитывается непосредственно по уравнению UNIQUAC с использованием параметров площади и объема Ван дер Ваальса, рассчитанных по индивидуальным структурным группам :
рассчитывается непосредственно по уравнению UNIQUAC с использованием параметров площади и объема Ван дер Ваальса, рассчитанных по индивидуальным структурным группам :
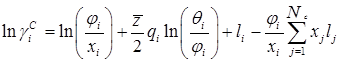 (4.8.2.)
(4.8.2.)
где:
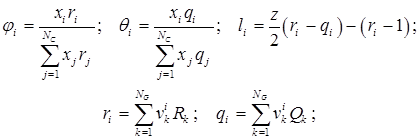 (4.8.3.)
(4.8.3.)
NC – число компонентов;
NG – число различных групп в смеси;
z – согласованное число для пространственной решетки, равное 10;
![]() – число функциональных групп типа k в молекуле i;
– число функциональных групп типа k в молекуле i;
Rk – параметр объема для функциональной группы k;
Qk – параметр площади для функциональной группы k;
xi – мольная доля компонента i в жидкой фазе.
Параметры группового объема и площади определяются из атомной и молекулярной структуры:
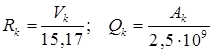 (4.8.4.)
(4.8.4.)
где : Vk, Ak = объем и площадь Ван дер Ваальса для группы k;
Остаточный член ![]() определяется как:
определяется как:
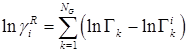 (4.8.5.)
(4.8.5.)
где: Гk = остаточный коэффициент активности группы k в смеси;
