Реакции альдегидов и кетонов присоединение углеродных нуклеофилов
Особая ценность реактивов Гриньяра заключается в их способности создавать новые связи С¾С. Разница в электроотрицательности между углеродом и магнием (2,5 - 1,2 = 1,3), обусловливает полярность связи между этими атомами и наличие частичного отрицательного заряда на атоме углерода и частичного положительно-го заряда на атоме магния. В реакциях реактивы Гриньяра ведут себя как карбанионы. Карбанионы являются хорошими нуклеофилами и легко присоединяются к карбонильной группе. Магнийорганические соединения вступают в реакции нуклеофильного присоединения к альдегидам и кетонам с образованием алкоксидов, гидролизующихся в спирты:
Присоединение к формальдегиду приводит к образованию первичных спиртов.
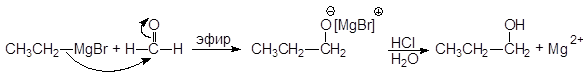 (17)
(17)
Другие альдегиды дают вторичные спирты:
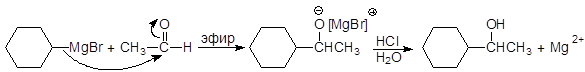 (18)
(18)
1-Циклогексилэтанол
Из кетонов получают третичные спирты:
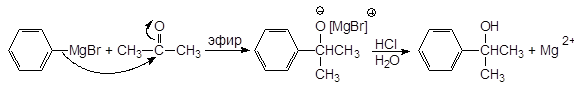
2-Фенил-2-пропанол
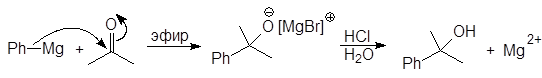 (19)
(19)
Б. Присоединение литийорганических соединений
Литийорганические соединения более реакционноспособны, чем магнийлрганичес-кие и обеспечивают больший выход целевого продукта. Онако с ними можно работать только в атмосфере инертного газа. Ниже приводится пример использования литийорганического соединения для получения стерически затрудненного третичного спирта.
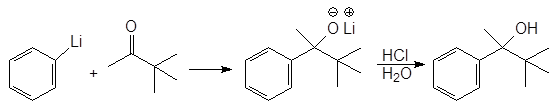 (20)
(20)
Фениллитий 3,3-Диметил-2-бутанон 3,3-Диметил-2-феил-2-бутанол
В. Присоединение ацетиленидов металлов
Этинид-анион также является нуклеофилом. Образующиеся при этом спирты содержат две функциональные группы, каждая из которых может быть далее модифицирована.
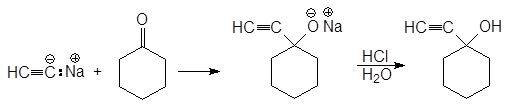 (21)
(21)
1-этинилциклогексанол
Гидратация полученного алкинола приводит к образованию a-гидроксикетона, а гидроборирование-окисление - b-гидроксиальдегида.
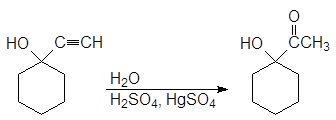 (22)
(22)
1-ацетилциклогексанол
(a-гидроксикетон)
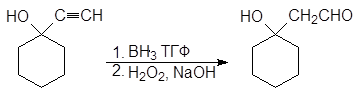 (23)
(23)
2-(1-гидроксициклогексил)этаналь
(b-гидроксикетон)
Упр. 8. Напишите реакции получения 2-фенил-2-бутанола с помощью реактивов Гриньяра (3 комбинации).
Г. Циангидринный синтез
Циановодород присоединяется к альдегидам и кетонам с образованием a-окси-нитрилов ( циангидринов). Сама синильная кислота является очень слабым нуклеофилом и поэтому реагирует очень медленно. С гораздо большей скоростью карбонильная группа реагирует с цианид-ионом.
Альдегиды легко образуют циангидрины. Кетоны с разветвленной цепью углеродных атомов, а также высшие кетоны циангидринов не образуют. Реакцию обычно проводят, прибавляя минеральную кислоту к смеси карбонильного соединения и водного раствора цианида натрия.
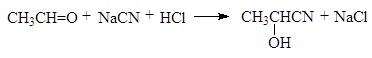 (24)
(24)
2-гидроксипропаннитрил
(ацетальдегидциангидрин)
Гидролизом циангидринов получают a-оксикислоты:
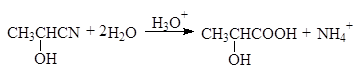 (25)
(25)
нитрил a-оксипро- молочная
пионовой кислоты кислота
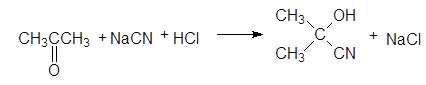 (26)
(26)
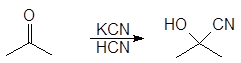
ацетонциангидрин
Реакция проходит при щелочном катализе по следующему механизму:
![]()
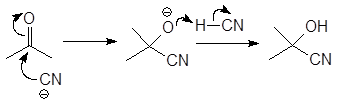 (М 5)
(М 5)
При гидролизе ацетонциангидрина в присутствии соляной кислоты образуется 2-гидрокси-2-метилпропановая кислота, а при его обработке концентрированной серной кислотой – метакриловая кислота:
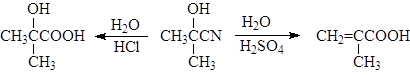 (27,28)
(27,28)
2-гидрокси-2-метилпропановая к-та метакриловая к-та
Ацетонциангидрин широко используется в лабораторной практике для получения других циангидринов, например:
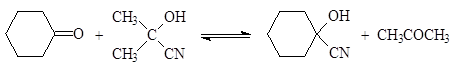 |
(29)
циклогексанонциангидрин
В этой реакции используется обратимость реакций присоединения к карбонильной группе.
Упр.9. Напишите реакции ацетона и пропионового альдегида с синильной кислотой. Каков механизм этих реакций? Какое из этих соединений и почему будет легче вступать в реакцию? Объясните, почему образование циангидринов ускоряется добавлением оснований, а не добавлением кислот?
Д. Реакция Реформатского
К действию цинкорганических соединений на альдегиды и кетоны сводится реакция Реформатского:
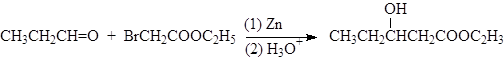 (30)
(30)
пропаналь этилбромацетат этил-3-гидроксивалероат
Упр. 10. Напишите реакции получения ниже следующих соединений из соответствующих альдегидов и кетонов по реакции Реформатского:
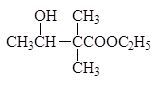
![]()
![]() (в)
(в)
