Реакции спиртов. Кислотно-основные свойства спиртов. Реакции с участием нуклеофильного центра
Спирты представляют собой соединения общей формулы ROH, в которых гидроксильная группа присоединена к насыщенному атому углерода. По номенклатуре ИЮПАК насыщенные спирты называют алканолами, нумерация в которых определяется гидроксильной группой. Гидроксильная группа при наличии двойной и тройной связей является старшей.
![]()
![]()
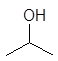
![]()
![]()
этанол 1-пропанол 2-пропанол 2-пропен-1-ол 2-пропин-1-ол
этиловый пропиловый изопропиловый аллиловый пропаргиловый спирты
![]()
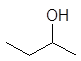
![]()
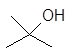
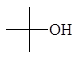
1-бутанол 2-бутанол 2-метил-1-пропанол 2-метил-2-пропанол
н-бутиловый втор-бутиловый изобутиловый трет-бутиловый спирты
При нумерации атомов главной цепи спиртов гидроксильная группа имеет преимущество перед алкильными группами, атомами галогенов и кратной связью.
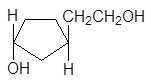
транс-3-(2’-гидроксиэтил)-1-циклопентанол
Часто спирты называют по углеводородной группе (этиловый спирт). В этой номенклатуре положение заместителя в алкильной группе спирта обозначается буквами греческого алфавита:
![]()
![]()
g-бромпропиловый спирт b-метоксиэтиловый спирт
В зависимости от того, является ли атом углерода, к которому присоединена гидроксильная группа, первичным 1о, вторичным 2о или третичным 3о спирты бывают 1о (RCH2OH), 2о (R2CHOH) или 3о (R3COH). Например, из четырех возмож-ных бутиловых спиртов два – бутиловый и изобутиловый являются первичными 1о, втор-бутиловый - вторичным 2о и трет-бутиловый – третичным 3о.
Число гидроксильных групп в молекуле определяет так называемую атомность спирта. По числу гидроксильных групп в молекуле спирты подразделяются на одноатомные, двухатомные, трехатомные и т.д. Например, этанол является одноатомным спиртом, этиленгликоль _ двухатомным, а глицерин _ трехатомным.
![]()
![]()
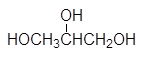
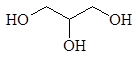
этиленгликоль глицерин
1. Реакции спиртов
Функциональная группа спиртов содержит электроотрицательный атом кислорода с двумя неподеленными парами электронов. В молекуле спиртов можно выделить следующие реакционные центры:
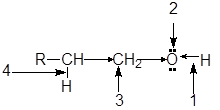
1. ОН-кислотный центр, обусловливающий возможность отщепленя протона вследствие высокой полярности связи О-Н;
2. нуклеофильный и n-основный центр - атом кислорода, имеющий неподеленные пары электронов;
3. электрофилный центр - a-атом углерода, на котором дефицит электронов вызван -I-эффектом соседней гидроксильной группы;
4. b-С-кислотный центр, в котором поляризация связи С-Н также обусловлена электроноакцепторным влиянием гидроксильной группы.
1.1. Кислотно-основные свойства спиртов
Спирты являются слабыми ОН-кислотами Бренстеда и жесткими кислотами по Пирсону. По кислотности спирты близки к воде. Кислотные свойства спиртов определяются способностью к протонизации атома водорода гидроксильной группы. Последняя обусловливается не только разницей в электроотрицательностях между атомами кислорода (3,5) и водорода (2,1), но и природой радикала. Метанол (pKa = 15,5), несколько более сильная кислота, чем вода (pKa = 15,7), но большинство спиртов являются более слабыми кислотами, чем вода. Причиной этого являются стерические препятствия, мешающие в разветвленных спиртах сольватации образующегося алкоксид-аниона. Сольватация стабилизирует алкоксид-анион и следовательно усиливает кислотные свойства.
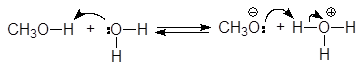 (26)
(26)
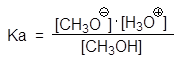
pKa = 15.5
Образование межмолекулярной водородной связи в жидкой фазе определяет различие в кислотности первичных, вторичных и третичных спиртов. В водном растворе кислотность спиртов уменьшается в ряду:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
pKa (в воде) 5.0 15,5 15,7 15,9 17,0 18,0
тогда как в газовой фазе наблюдается прямо противоположная последователь-ность
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() 30 20 10 10
30 20 10 10
В жидкой фазе определяющим фактором стабилизации алкоксид-анионов является эффект сольватации, который тем больше, чем меньше стерические препятствия для сольватации, т.е. чем меньше в молекуле углеводородных радикалов и меньше их размер. Разветвленность алкильной группы снижает кислотность спиртов, а введение в их молекулы атомов галогена, наоборот повышает ее.
Кислотные свойства спиртов проявляются во многих реакциях, например:
![]() (27)
(27)
метоксид натрия
(MeO‾Na+)
![]() (28)
(28)
этоксид натрия
(EtO‾Na+)
![]() (29)
(29)
трет-бутоксид калия
(t-BuO‾K+)
1.2. Реакции с участием нуклеофильного центра
Высокая электроотрицательность атома кислорода (3,5 по шкале Полинга), являющегося основным центром, позволяет рассматривать спирты как слабые n-основания Бренстеда и жесткие основания по Пирсону. Неудивительно, что спирты способны образовывать соли оксония только с сильными протонными кислотами и жесткими кислотами по Пирсону (фторид бора, хлорид цинка и др.).
