Синтез и анализ ХТС в производстве гидроксида натрия и хлора из водного раствора хлорида натрия
C + O2 → CO2
C + 0,5O2 → CO
- растворение хлора в электролите с образованием соляной и хлорноватистой кислот:
Cl2 + 2H2O ↔ H3O + Cl- + HOCl
- взаимодействие компонентов при диффузии щелочи в анодное пространство или смешении анодной (анолит) и катодной (католит) жидкостей с образованием гипохлорит-иона и хлорат-иона.
В результате протекания вторичных процессов раствор гидроксида натрия, полученный электролизом с железным катодом, всегда содержит примесь гипохлорита и хлората натрия. Вторичные процессы снижают выход по току и коэффициент использования энергии.
Удельный вес побочных вторичных процессов может быть снижен:
- разделением катодного и анодного пространства в электролизере с помощью фильтрующей диафрагмы (отсюда название метода диафрагменный), обеспечивающей одностороннее движение рассола в направлении, противоположном движению ионов ОН- к аноду и препятствующей обратному перемещению их;
- подачей рассола в электролизер со скоростью, превышающей скорость образования ионов ОН- и вытеснение образующегося раствора гидроксида натрия (щелока) в катодное пространство;
- применением высоких температур и концентраций рассола, что снижает растворимость хлора в электролите и вероятность протекания вторичных процессов;
- понижением концентрации выходящего из электролизера щелока, то есть уменьшением содержания гидроксида натрия в растворе, также снижающего вероятность вторичных процессов. Поэтому, процесс электролиза никогда не доводят до полного превращения хлорида натрия, останавливая егопри достижении определенной концентрации щелока.
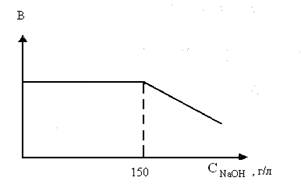
Рис. 1. Зависимость выхода по току от концентрации щелока
На рис. 1. приведена зависимость выхода гидроксида натрия от концентрации его в выходящем щелоке. Таким образом, оптимальными условиями процесса электролиза водного раствора хлорида натрия с железным катодом являются:
- температура электролита 70 - 90°С;
- концентрация щелока, выходящего из электролизера 130 - 140 г/л;
- концентрация рассола, поступающего в электролизер 305 - 315 г/л.
В этих условиях степень превращения хлорида натрия составляет 0,4-0,5 дол. ед.
Эектролизер (электролитическая, ячейка) - основной аппарат в технологическом процессе производства едкого натра и хлора электролизом водного раствора хлорида натрия с железным катодом.
Диафрагменные электролизеры могут быть двух типов: с вертикально расположенными катодами с верхним или нижним токоподводом, или с горизонтально расположенными катодами. В настоящее время повсеместно используются электролизеры первого тпа (рис 2).
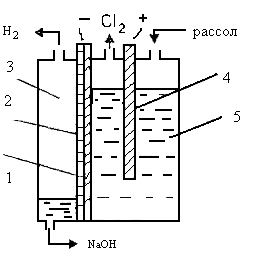
Рис. 2. Электролизер вертикального типа: 1 – перфорированный катод, 2 – диафрагма, 3 – катодное пространство, 4 – анод, 5 – анодное пространство.
Электролизер состоит из герметически закрытого корпуса, что исключает подсос воздуха и загрязнение им газообразных продуктов электролиза, анода, катода и диафрагмы. Он снабжен устройствами для подвода рассола и отвода щелока, хлора и водорода. Катод![]() электролизера изготовлен из перфорированной листовой стали или стальной сетки, натянутой на каркас. Катод может иметь различную конфигурацию. Диафрагму электролизеров изготавливают из асбеста, устойчивого к слабокислой, щелочной среде и действию хлора. Диафрагмы могут быть двух типов: листовые и осажденные. Листовые диафрагмы изготавливают из тонких листов асбестового картона, плотно прилегающих к катоду, осажденные - из специально подготовленного асбестового волокна, наносимого в виде пульпы на поверхность катода и насасываемого на него. В табл. 2. приведены характеристики наиболее распространенных современных электролизеров с металлооксидными анодами БГК-50/25 и БГК-100, различающиеся производительностью.
электролизера изготовлен из перфорированной листовой стали или стальной сетки, натянутой на каркас. Катод может иметь различную конфигурацию. Диафрагму электролизеров изготавливают из асбеста, устойчивого к слабокислой, щелочной среде и действию хлора. Диафрагмы могут быть двух типов: листовые и осажденные. Листовые диафрагмы изготавливают из тонких листов асбестового картона, плотно прилегающих к катоду, осажденные - из специально подготовленного асбестового волокна, наносимого в виде пульпы на поверхность катода и насасываемого на него. В табл. 2. приведены характеристики наиболее распространенных современных электролизеров с металлооксидными анодами БГК-50/25 и БГК-100, различающиеся производительностью.
Таблица 2
Характеристики электролизеров с железным катодом и металлооксидными анодами
|
Показатели |
Тип электролизера | |
|
БГК-50/25 |
БГК-100 | |
|
Сила тока (нагрузка на ячейку), кА |
50 |
100 |
|
Число ячеек (электролизеров) |
1 |
1 |
|
Напряжение, В |
3,40 |
3,45 |
|
Выход по току, дол. ед. |
0,96 |
0,96 |
|
Срок службы электродов, лет |
4 |
4 |
|
Концентрация NaOH в щелоке, г/л |
120-140 |
120-140 |
|
Концентрация хлора, не менее об. дол. |
0,965 |
0,975 |
|
Концентрация водорода, не менее об, дол. |
0,995 |
0,995 |
|
Производительность по 100% NaOH, т/сутки |
1,72 |
3,44 |
В цехе электролиза, отдельные ячейки (электролизеры) объединены в группы до 150 штук. Тогда суммарное напряжение электролиза составит 3,4·150 = 510 В.
Разновидность диафрагменного способа - более совершенный процесс электролиза в электролизерах с ионообменной мембраной. В таких электролизерах анодное и катодное пространства разделены полимерной мембраной, которая предотвращает попадание хлорида натрия из анодного пространства в которое подается рассол, в катодное и препятствует переносу ионов ОН- к аноду электролизера. Хлор выделяется на аноде и выводится из анодного пространства вместе с обедненным рассолом. Ионы натрия и частично молекулы воды проходят через мембрану к катоду, куда подается вода в количестве, необходимом для образования щелока заданной концентрации. Электролизеры мембранного типа различаются числом ячеек (от 40 до 80) и имеют мощность до 80 тысяч тонн в год по гидроксиду натрия. В отличие от электролизеров с асбестовой диафрагмой нагрузка на ячейку (сила тока) значительно ниже и не превышает 7,5 кА. Поэтому электролизеры с ионообменной мембраной значительно экономичнее диафрагменных.
1.3. Электролиз раствора хлорида натрия с ртутным катодом
На ртутном катоде разряд ионов гидроксония Н3О может происходить только при малых, менее 50 А/м, плотностях тока. В условиях промышленного электролиза водных растворов хлорида натрия в электролизерах с ртутным катодом плотность тока составляет 5-10 кА/м2. При такой плотности тока, вследствие перенапряжения потенциал разряда ионов Н3О составляет +2,0 В. В то же время, за счет растворения выделившегося металлического натрия в ртути, образуется амальгама Natign, представляющая качественно новый электрод, потенциал разряда натрия на котором составляет +1,2 В. Поэтому, на катоде будут разряжаться ионы натрия.
