Химизм сорбции на полистирол-азо-тиазан-дитионе-2,4
Установлено, что ртуть(I,II) в присутствии ацетатов, формиатов и некоторых органических растворителей (спирт, ацетон) в слабокислой среде взаимодействует с 5-хлор-2-гидрокси-3-[(тетра-гидро-2,4-дитиоксо-1,3-тиазин-5-ил)азо] бензолсульфокислотой (тиродином) с образованием малорастворимого интенсивно окрашенного соединения (λмакс = 600 нм, ε > 3 х 104). Обнаружено влияние состава среды на чувствительность цветной реакции ртути с тиродином. Разработана тест-методика определения ртути(I, II) на поверхности поликапроамидной мембраны с пределом обнаружения <50 мг в зоне сорбента, основанная на количественной и избирательной сорбции комплексного соединения ртути с тиродином в динамическом режиме из растворов с рН = 3-4 в присутствии ацетатов (0.5 М растворы) при объеме пробы 5-25 мл поверхностью носителя. Последующее определение ртути — по изменению окраски носителя с использованием цветовой шкалы сравнения или по изменению коэффициента диффузного отражения при 600 нм. Сорбция комплекса ртути сопровождается резким изменением окраски поверхности носителя: от слабо малиновой (реагент) до устойчивой сине-фиолетовой. Тест-методика использована при анализе промышленных образцов сложного состава с содержанием ртути менее 0.05%. Погрешность определения (sr) 0.2 . [9]
Разработан вариант проточно-инжекционного определения малых содержаний ртути в водных растворах, включающий предварительное сорбционное концентрирование и одновременный перевод ртути в аналитически-активную форму. В качестве детектора предложен тетрайодмеркуроатный жидкостной электрод, селективный к йодидным комплексам ртути. В настоящей работе изучена возможность ионометрического проточно-инжекционного определения ртути с предварительным сорбционным концентрированием. [10]
Изучена сорбция свинца из тиосульфатного раствора на твердой фазе волокнистого материала, наполненного анионообменником АВ-17 (ПАНВ-АВ-17). Свинец определяли цветной реакцией с 4-(2-пиридилазо)резорцином (ПАР) на твердой фазе методом спектроскопии диффузного отражения. Выбраны оптимальные условия сорбции (рН 4.5 ± 0.5) и определения (рН 10) свинца, изучена избирательность определения. Предложена новая система РЬ-тиосульфат-(ПАНВ-АВ-17)-ПАР для определения свинца на твердой фазе. Разработана методика определения свинца в пресных водах с пределом обнаружения 0.01 мг/л и Sr < 0.25. [11]
Разработана методика проточно-инжекционного определения малых количеств кадмия в водных растворах с использованием в качестве детектора ионоселективных электродов, чувствительных к его иодидным и хлоридным комплексам. Предварительное сорбционное концентрирование позволяет снизить предел обнаружения, повысить селективность определения и включает одновременный перевод кадмия в аналитически активную форму. [12]
Изучены цветные реакции меди(II) с ПАР и пикрамин-Е на кремнеземе, химически модифицированном группами иминодиуксусной кислоты, обменная реакция ртути(П) с диэтилдитиокарбаминатом меди в фазе кремнезема, химически модифицированного гексадецильными группами. Разработаны методики тест-определения меди и ртути. Показана возможность определения длинноцепочечных аминов в виде ионного ассоциата с восстановленной формой молибдокремневой кислоты на поверхности кремнезема, химически модифицированного гексадецильными группами. [13]
Предложен атомно-абсорбционный способ определения меди и кадмия в пламени пропан-бутан-воздух с предварительным электрохимическим и сорбционным концентрированием. Электрохимическое концентрирование проводили на металлических электродах из тантала, титана, молибдена, платины, а также на электродах из стеклоуглерода и спектрального графита. Сорбционное концентрирование осуществляли на фильтровальной бумаге с иммобилизованными дитизоном, 8-оксихнинолином и рубеановодородной кислотой. Показана возможность определения меди и кадмия в водах в диапазоне концентраций 1-10 мкг/л. [14]
Изучено комплексообразование свинца с арсеназо III в твердой фазе. Полученные данные использованы для разработки новой методики определения микроколичеств свинца. Одним из методов использованный при этом был фотометрический. Сочетание его с различными способами концентрирования, такими, как сорбционное и экстракционное, позволяет повысить чувствительность и селективность определений. [15]
Значительное внимание привлекают, наряду с другими, полимерные хелатообразующие сорбенты (ПХС), позволяющие осуществлять индивидуальное или групповое выделение микроэлементов, нивелируя влияние матрицы и обеспечивая высокий коэффициент концентрирования.
Синтезирован новый класс ПХС на основе полистирола и азозамещенных салициловой кислоты. Исследованные сорбенты представляют собой порошки коричневого цвета, нерастворимые в воде, кислотах, щелочах и органических растворителях. Сорбенты отвечают структурной формуле:
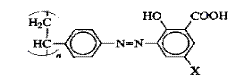
где X - мета-заместители: Н, Вr, SО3Н, АsО3Н2, N02, NH2.
Был разработан способ группового концентрирования и выделения РЬ, Zn, Cd, Мn, Сr, V новым сорбентом - полистирол-(азо-1)-2-окси-3-карбокси-5-нитробензол с последующим атомно-абсорбционным или хроматографическим определением элементов в природных и сточных водах. Сорбент извлекает микроколичества металлов (R = 95-100%) из воды в статических условиях при 30 ± 5°С, рНопт= 5.5-6.5; τ = 15-30 мин. Повышение температуры обусловлено необходимостью разрушить гидратную оболочку иона хрома [Сr(Н20)6]3+, чтобы повысить его способность к комплексообразованию. Увеличение температуры не оказывает существенного влияния на сорбцию других металлов.
На сорбцию элементов не влияют значительные количества макрокомпонентов (указаны отношения количеств мешающих элементов к количеству определяемых):
п х 105 К+ (n = 6), Nа+ (п = 8), NО-3, НРО42-, НСО3-, F-, сульфосалициловой кислоты (п = 5-7),
п X 104 - Са2+ (п = 6), |Mg2+ (п = 4),
п х 103 - Ва2+ (п = 8), Sr2+ (п = 7.5), : А13+ (п = 5), Fе3+ (n = 3),
п х 102 - Ni3+, Со2+, Сu2+.
Разработанная схема позволяет применять для определения тяжелых металлов метод пламенной атомно-абсорбционной спектроскопии или высокоэффективную жидкостную хроматографию.
Метод дает возможность выделять определяемые элементы из сложных по составу природных вод, содержащих высокие концентрации щелочных, щелочноземельных и других элементов, характеризуется экспрессностью, избирательностью, низкими пределами обнаружения и высокой воспроизводимостью результатов. Относительное стандартное отклонение составляет Sr = 0.02-0.04 для уровня содержания элементов в объекте n×10-4-m×10-5%. [16]
Найдены условия избирательного сорбционно-фотометрического определения ванадия(IV, V) и ртути(I, II) с использованием органических реагентов (ОР): сульфонитрофенола М (ванадий) и тиродина (ртуть). Определение V и Нg (визуальный тест. Sr = 0.3) с использованием цветовой шкалы сравнения или количественное (спектроскопия диффузного отражения, Sr = 0.1) проводят сразу после концентрирования в динамических условиях (при P = 10-20 мм рт. ст.) их окрашенных комплексов. Используются окрашенные комплексы ванадия(IV) с сульфонитрофенолом М (рН 3.5, 650 нм), ванадия(V) с сульфонитрофенолом М и гидроксиламином (смешанолигандный комплекс, 650 нм, рН 1.5) и ртути (I, II) с тиродином в присутствии карбоксил-ионов (580 нм, рН 3) на поверхности поликапроамидной мембраны; диаметр мембраны - 10 мм, b= 0.1 мм, m = 2.7мг. Пределы обнаружения 0.2-0.5 нг/мл (ванадий) и 4 нг/мл (ртуть). Определению ванадия(V) при рН 1.5 не мешают 20-кратные количества ванадия(IV) и значительные количества Ni, Со, Zn, Сd, Cr(III), Мn, Cu, РО43-,F; определению ртути - V, РЬ, Сd,Zn,Сu,Ni, PO43-. [17]
