Химия металлоорганических соединений
Для соединения с более полярной связью (Li, Na, Mg) предпочтительнее гетеролитические реакции:
![]() .
.
Соединения с менее полярной связью (Hg, Pb, Sn) реагируют как по гетеролитическому механизму (например, действие кислот), так и по гомолитическому (например, термическое разложение):
![]()
Образование металл - углеродной связи, например при взаимодействии галогеноалканов с металлами, может протекать через стадию ион - радикалов. Реакция начинается с переноса электрона с решетки металла на молекулу галогеноалкана с образованием анион-радикала (легко идентифицируется методом электронного парамагнитного резонанса), распадающегося на радикал и анион галогена, которые адсорбируются на поверхности металла. Далее радикал принимает второй электрон, превращаясь в карбанион, одновременно катион металла переходит в раствор, образуя металлоорганическое соединение.
1. ЭЛЕМЕНТЫ ПЕРВОЙ ГРУППЫ.
Щелочные металлы первой подгруппы имеют на внешней электронной оболочке по одному электрону и, следовательно, одновалентны.
Металлоорганические соединения построены так, что металл обычно связан поляризованной связью с атомом углерода органического остатка R—Me (где R — алкил или арил):
![]()
![]()
![]()
Названия металлоорганических соединений слагаются из названий радикалов и металла.
1.1 Органические соединения лития.
Способы получения. 1. Из галогеноалкилов (или арилов) и металлического лития (К. Циглер, 1928 г.). Способ заключается во взаимодействии лития с галогеноалкилами или арилами (обычно применяют хлористые алкилы и бромистые арилы). Успех реакции,![]()
![]()
![]() помимо строения галогенопронзводного, зависит от растворителя и температуры. Растворителями при получении литийорганических соединений — алкильных — служат петролейный эфир, гексан, бензол; арильных — этиловый эфир:
помимо строения галогенопронзводного, зависит от растворителя и температуры. Растворителями при получении литийорганических соединений — алкильных — служат петролейный эфир, гексан, бензол; арильных — этиловый эфир:
![]()
![]()
Галогенвинилы (в которых галоген обладает малой подвижностью) легко реагируют с литием, образуя литийорганические соединения винильного типа:
![]()
Неустойчивость литийорганических соединений к влаге и к кислороду заставляет проводить синтез с сухими веществами в атмосфере инертных газов (азота). Литийорганические соединения обычно не выделяются в свободном виде, а применяются в растворах так же как натрий- и магнийорганические соединения.
Основному процессу могут сопутствовать побочные реакции, например взаимодействие исходного галогеноалкила с образовавшимся литийорганическим производным:
![]() 2. Действие лития и литийалкилов на органические соединения ртути имеет значение в случае необходимости выделения литийоранических соединений в свободном виде:
2. Действие лития и литийалкилов на органические соединения ртути имеет значение в случае необходимости выделения литийоранических соединений в свободном виде:
![]()
Химические свойства. Вода, спирты, кислоты легко реагируют с литийорганическими соединениями, например:
![]()
Окисление литийорганических соединений. При регулируемом окислении литийорганические соединения превращаются в спирты:
![]()
Синтез кислот. Введение литийорганических соединений в избыток двуокиси углерода (их выливают на твердую углекислоту) приводит к литиевым солям карбоновых кислот, которые при действии соляной кислоты превращаются в карбоновые кислоты. Эта реакция широко применяется при исследовании строения литийорганических соединений и для синтеза карбоновых кислот:
![]() Взаимодействие с непредельными углеводородами — общее свойство для щелочных металлов первой группы. Первоначально считалось, что для успеха реакции двойная связь должна быть сопряжена с непредельной системой или ароматическим кольцом. Однако в 1960 г. К. Циглер показал возможность присоединения литийалкилов к изолированной двойной связи, причем третичные и вторичные литийалкилы реагируют легче первичных.
Взаимодействие с непредельными углеводородами — общее свойство для щелочных металлов первой группы. Первоначально считалось, что для успеха реакции двойная связь должна быть сопряжена с непредельной системой или ароматическим кольцом. Однако в 1960 г. К. Циглер показал возможность присоединения литийалкилов к изолированной двойной связи, причем третичные и вторичные литийалкилы реагируют легче первичных.
Бутиллитий при нагревании и повышенном давлении присоединяется к этилену с образованием литийалкилов (в которых литий сохраняет высокую реакционную способность):
![]()
Изопропиллитий реагирует с этиленом уже при -60°С, образуя 1-литий-З-метилбутан:
![]()
К 1,3-бутадиену литийалкилы присоединяются в положения 1,4 и 1,2. Повышение температуры и давления благоприятствует 1,4- присоединению:
![]() .
.
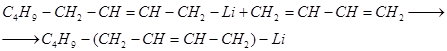
Практическое значение этой реакции заключается в том, что она привела к промышленному методу стереорегулярной полимеризации 1,3-бутадиена в синтетический каучук.
Взаимодействие алкиллития с карбонильными соединениями (альдегидами, кетонами), как и в случае натрий-, магний-, цинк-, алюминийорганических соединений, приводит к спиртам. Использование в этой реакции литийорганических соединений оправдано в тех случаях, когда взаимодействие с альдегидами и кетонами более доступных магнийорганических соединений не приводит к цели.
Так, диизопропилкетон и изопропиллитий образуют триизопропилкарбинол. Реакция протекает через стадию нестойкого комплекса, который перегруппировывается в литиевый алкоголят, гидролизуемый водой в триизопропил карбинол:
![]() Магнийорганическим синтезом подобный спирт разветвленного строения получить нельзя вследствие восстановления исходного кетона магнийорганическим соединением.
Магнийорганическим синтезом подобный спирт разветвленного строения получить нельзя вследствие восстановления исходного кетона магнийорганическим соединением.
1.2 Органические соединения натрия
Натрийорганические соединения сохраняют ряд общих черт с органическими соединениями лития, однако их специфика заключается: а) в преимущественной роли реакции металлирования при их синтезе, открытой П. П. Шорыгиным (1910 г.) и детально разработанной на примере получения органических соединений натрия; б) в большей реакционной способности, затрудняющей их синтетическое использование. Практическое значение органических соединений натрия связано с инициируемой ими реакцией полимеризации 1,3-бутадиена.
Способы получения. Металлирование (замена водорода натрием в органических соединениях). Металлирующими агентами могут быть натриевые производные предельных углеводородов, амид натрия в жидком аммиаке и металлический натрий. Металлированию подвергаются преимущественно следующие группы органических соединений: ароматические углеводороды, жирноароматические соединения, ацетиленовые углеводороды.
