рДНК-биотехнология. Способы биотрансформации клеток
Электропорация — наиболее простой, эффективный и воспроизводимый метод введения молекул ДНК в клетки. Однако до недавнего времени этот метод использовался в ограниченном числе лабораторий в связи с отсутствием серийных приборов — электропораторов. Появление и совершенствование таких приборов в ближайшие годы приведет к широкому применению данного подхода в генетической инженерии самых разных типов клеток.
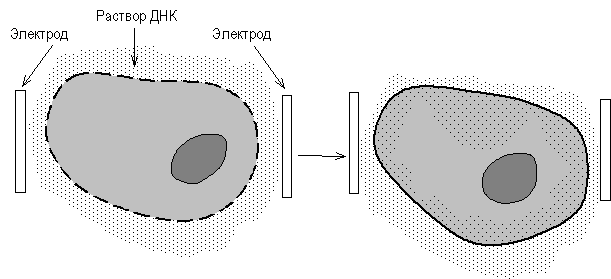
Рис. 5. Метод электропорации
«Мини-клетки» получают путем блокирования донорных клеток митозе колцемидом. При продолжительной обработке клеток колцемидом в них вокруг каждой хромосомы формируется новая ядерная мембрана. Обработка цитохалазином В и центрифугирование приводит к образованию мини-клеток, представляющих микроядра, инкапсулированные в цитоплазматическую мембрану.
Полученные мини-клетки очень чувствительны к разного рода воздействиям, поэтому для слияния подбирают специальные мягкие условия. Метод трудный, капризный, эффективность низкая – 10-6 – 10-7.
Упаковка в липосомы используется для защиты экзогенного генетического материала от разрушающего действия рестриктаз.
Липосомы - сферические оболочки, состоящие из фосфолипидов. Получают их путем резкого встряхивания смеси водного раствора и липидов, либо обрабатывая ультразвуком водные эмульсии фосфолипидов. Липосомы, состоящие из фосфатидилсерина и холестерина наиболее пригодны для введения ДНК в клетки животных и растений. Системы переноса с помощью липосом низкотоксичны по отношению к клеткам.
Метод биологической баллистики (биолистики) является одним из самых эффективных на сегодняшний день методов трансформации растений, особенно однодольных.
Суть метода заключается в том, что на мельчайшие частички вольфрама, диаметром 0,6—1,2 мкм, напыляется ДНК вектора, содержащего необходимую для трансформирования генную конструкцию. Вольфрамовые частички, несущие ДНК, наносятся на целлофановую подложку и помещаются внутрь биолистической пушки. Каллус или суспензия клеток наносится в чашку Петри с агаризированной средой и помещается под биолистическую пушку на расстоянии 10—15 см. В пушке вакуумным насосом уменьшается давление до 0,1 атм. В момент сбрасывания давления вольфрамовые частички с огромной скоростью выбрасываются из биолистической пушки и, разрывая клеточные стенки, входят в цитоплазму и ядро клеток.
Обычно клетки, располагающиеся непосредственно по центру, погибают из-за огромного количества и давления вольфрамовых частиц, в то время как в зоне 0,6—1 см от центра находятся наиболее удачно протрансформированные клетки. Далее клетки осторожно переносят на среду для дальнейшего культивирования и регенерации.
С помощью биолистической пушки были протрансформированы однодольные растения, такие, как кукуруза, рис, пшеница, ячмень. При этом были получены стабильные растения-трансформанты. Кроме успехов в получении трансгенных однодольных, биолистическая трансформация применяется для прямого переноса ДНК в эмбриогенную пыльцу и дальнейшего быстрого получения трансгенных дигаплоидных растений, которые являются важным этапом в селекционной работе. В настоящее время этим методом была проведена трансформация растений табака и после регенерации гаплоидных растений получены стабильные трансформанты.
2.3 Способы прямого введения гена в клетку
В настоящее время бактерия E. coli является самой изученной клеткой из всех существующих. У большинства наиболее полно изученных фагов клеткой - хозяином является также E. coli.
Протопласт E. coli одет в муреиновый мешок, прилегающий к внешней мембране. E. coli относится к микроорганизмам, не обладающим физиологической компетентностью к поглощению экзогенной ДНК. Поэтому необходимо создать условия, позволяющие преодолеть барьер клеточной стенки. Сначала получают сферопласты путем обработки клеток лизоцимом в изотоническом растворе.
Липополисахаридный слой внешней мембраны грамотрицательной бактерии стабилизирован двухвалентными катионами, поэтому для разрыхления внешней мембраны E. coli используется комплексообразователь этилендиаминтетрауксусная кислота (EDTA), которая связывает двухвалентные катионы. При обработке EDTA часть липополисахаридов высвобождается из внешней мембраны клетки, и лизоцим может достигнуть муреинового мешка и гидролизовать его. Это ведет к повышению проницаемости клеточной оболочки. Усовершенствование методов получения сферопластов E. coli и их трансфекции позволили достичь достаточно высокой эффективности трансформации молекулами ДНК различных фагов.
Обнаружено, что на инфекционность существенное влияние оказывает форма молекул фаговых ДНК, которую они принимают in vivo. Фаги с кольцевой или линейной, но быстро замыкающейся ДНК (лямбоидные фаги) характеризуются наибольшей эффективностью трансфекции.
Успешное проведение экспериментов на кишечной палочке стало стимулом для проведения аналогичных исследований с другими прокариотическими организмами. Наибольших успехов удалось достичь с клетками Bacillus subtilis. B. subtilis - непатогенный почвенным микроорганизм, растущий в строго аэробных условиях. Бациллы не образуют токсинов и непатогенны ни для животных, ни для человека, тогда как клеточная стенка E. coli содержит эндотоксин, который довольно трудно отделить от продуктов генной инженерии. Кроме того, клеточная стенка бацилл имеет простую структуру и бактерии могут секретировать многие белки в культуральную жидкость. 20 различных видов бацил секретируют в культуральную жидкость более 40 ферментов с внеклеточной локализацией. E. coli секретирует в среду относительно мало белков, а выделение и очистка их затруднены. В бациллах также обнаружены плазмиды и фаги, которые к настоящему моменту уже хорошо изучены.
Чужеродные гены клонируют в так называемых челночных векторах. Эти вектора с одинаковым успехом реплицируются в клетках нескольких хозяев, в данном случае, в клетках E. coli и B.subtilis. Векторы были получены комбинацией in vitro фрагментов этих плазмид.
Гены E. coli со своими регуляторными районами не функционируют в B.subtilis, поэтому были использованы собственные гомологичные районы B.subtilis.
Для конструирования рекомбинантной ДНК, содержащей в своем составе ген, который должен экспрессироваться, придерживаются следующей стратегии. Синтезируют кДНК или из клонотеки выделяют клетки, несущие фрагмент генома с нужным геном, и клонируют их в соответствующем векторе. Фрагменты геномной ДНК подвергают модификации - удаляют из них некодирующие области и участки соседних генов. Часто для проведения этой операции необходимо секвенирование данного фрагмента ДНК. Затем конструируются промежуточные рекомбинантные ДНК, в которых ген помещается под контроль бактериальных регуляторных элементов (промотор, оператор, точка связывания с рибосомами). Эти регуляторные элементы выделяют из гибридных плазмид, сконструированных специально как источники регуляторных элементов. Полученная конструкция встраивается в подходящий вектор, например, pBR 322, и ген экспрессируется в бактериальной клетке.
