Химическая кинетика и равновесие в гомогенных системах
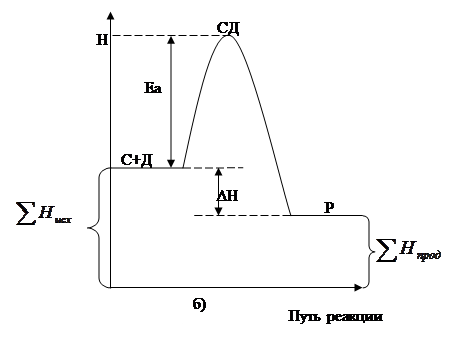
Рис. 5.4. Диаграмма изменения энтальпий для эндотермических (а)
и экзотермических (б) процессов.
На рисунке а) видно, что продукты реакции обладают большим запасом энергии, чем исходные вещества, то есть реакция А + В ® S эндотермическая. Разность между энергией продуктов реакции и исходных веществ является тепловым эффектом реакции ![]() .
.
Соответствующий график для экзотермической реакции С + Д → Р представлен на рисунке б).
Взаимосвязь между константой скорости реакции k и энергией активации Еа определяется уравнением Аррениуса:
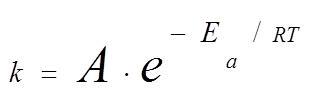 ,
,
где А – предэкспоненциальный коэффициент, связанный с вероятностью и числом столкновений.
Логарифмирование уравнения Аррениуса:
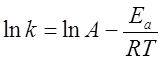 или
или 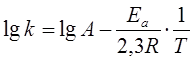
дает уравнение прямой линии. Знание констант скорости при нескольких температурах позволяет определить энергию активации данной реакции:
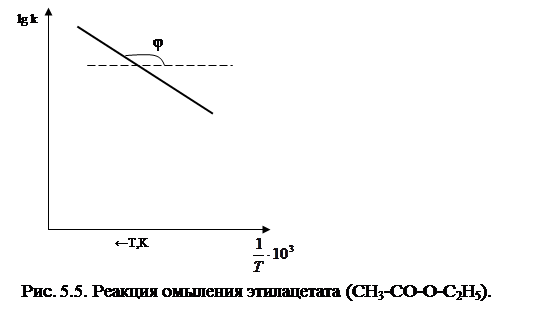
Тангенс угла наклона этой прямой к оси абсцисс равен:
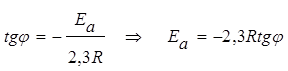 .
.
Энергия активации является тем фактором, посредством которого природа реагирующих веществ влияет на скорость химической реакции.
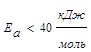 - «быстрые» реакции (ионные реакции в растворах);
- «быстрые» реакции (ионные реакции в растворах);
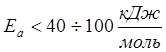 - реакции с измеряемой скоростью
- реакции с измеряемой скоростью
(Н2SO4 + Na2S2O3 = Na2SO4 + SO2 + S + H2O);
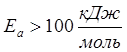 - «медленные» реакции
- «медленные» реакции
(синтез NH3 при обычных температурах).
Путь реакции может быть изменен введением в систему катализаторов.
Катализаторами называются вещества, которые влияют на скорость химической реакции, но их химический состав сохраняется после промежуточных стадий. Влияние катализаторов на скорость химических реакций называется катализом.
Катализаторы могут снижать энергию активации, направляя реакцию по новому пути. Снижение энергии активации приводит к возрастанию доли реакционноспособных частиц и, следовательно, к ускорению процесса взаимодействия. Катализаторы, ускоряющие реакцию, называются положительными. Известны также отрицательные катализаторы (ингибиторы). Они замедляют реакцию, связывая активные промежуточные молекулы или радикалы, и тем самым препятствуют протеканию реакции.
Катализаторы делятся на гомогенные и гетерогенные. Гомогенные находятся в одном и том же агрегатном состоянии хотя бы с одним из реагентов.
Гомогенный катализ осуществляется чаще всего через образование неустойчивых промежуточных продуктов. Например, реакция А + В → С требует большой энергии активации Еа. В присутствии катализатора протекают реакции А + К → АК и АК + В → С + К, где К – катализатор.
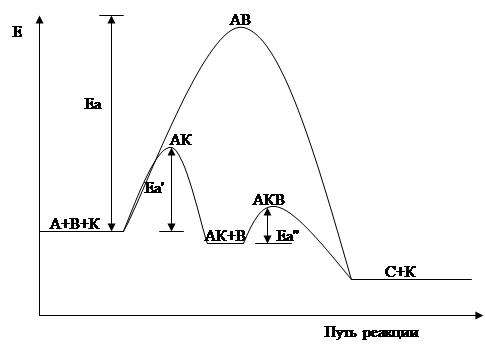
Рис. 5.6. Энергетическая диаграмма хода реакции А + В = С
без катализатора и с катализатором.
Если наибольшая из энергий активации Еа' и Еа'' для этих последовательных реакций меньше, чем энергия активации для реакции без катализатора Еа, то катализатор является положительным.
Пример гомогенного катализатора:
SO2 + O2 = SO3 - почти не идет;
2NO + O2 = NO2 - промежуточное состояние;
SO2 + NO2 = SO3 + NO – активно протекающая реакция (нитрозный способ серного ангидрида, а из него – серной кислоты) .
Цепные реакции.
Реакции протекающие с участием свободных радикалов, называются цепными. Радикал – короткоживущая валентноненасыщенная частица.
Различают два типа цепных реакций:
с неразветвленными цепями;
с разветвленными цепями.
К первому типу относится фотохимический синтез HCl. Цепь возникает в результате образования атомов – радикалов. ЕCl-Cl =58,0 ккал/моль; ЕН-Н = 104,2 ккал/моль.
Cl2 + hn = 2Cl× зарождение цепи
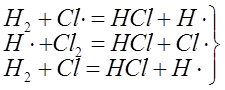 развитие цепи
развитие цепи
………………………….
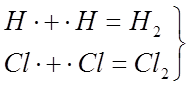 обрыв цепи
обрыв цепи
За счет внешнего источника энергии (свет, электрический разряд, нагревание, воздействие ά-, β- или γ- излучения) образуются свободные радикалы или атомы, обладающие свободными валентностями. Они взаимодействуют с молекулами. В каждом звене цепи вновь образуется новая активная частица. Путем повторения одних и тех же элементарных процессов происходит протекание цепной реакции. Ее продолжительность может быть очень большой. В приведенной выше реакции на каждый поглощенный квант образуется до 100 тыс. молекул НСl. Столкновение двух одинаковых радикалов при условии, что выделяющаяся при этом энергия может быть отдана третьему телу, приводит к обрыву цепи. Причиной обрыва может служить не только рекомбинация свободных радикалов, но и их захват стенкой реакционного сосуда, взаимодействие радикала с примесями, а также образование малоактивного радикала (обрыв в объеме). Поэтому скорость цепной реакции очень чувствительна к наличию посторонних частиц и форме сосуда.
В разветвленных цепных реакциях единичная реакция одного свободного радикала приводит к возникновению более чем одного нового свободного радикала. ![]()
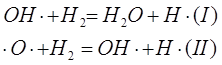
Образующиеся в реакции I радикалы обеспечивают развитие неразветвленной цепи, а атом кислорода, обладающий двумя свободными валентностями (реакция II), образует два радикала, начинающих разветвление. Возникает огромное количество свободных радикалов. «Размножение» радикалов приводит к лавинообразному течению процесса, которое может вызвать взрыв:
 Однако и в этих процессах происходят обрывы цепей. Причем бурное увеличение скорости процесса наблюдается лишь в том случае, когда темп разветвления опережает темп обрыва.
Однако и в этих процессах происходят обрывы цепей. Причем бурное увеличение скорости процесса наблюдается лишь в том случае, когда темп разветвления опережает темп обрыва.
Для таких реакций изменение концентрации активных центров во времени может быть выражено следующим соотношением:
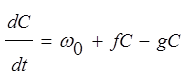 ,
,
где С – количество активных центров в зоне реакции;
![]() - скорость зарождения активных центров;
- скорость зарождения активных центров;
f – константа скорости разветвления цепей;
g – константа скорости обрыва цепей.
Химические реакции делятся на обратимые и необратимые
Химически необратимые реакции при данных условиях идут практически до конца, до полного расхода одного из реагирующих веществ (NH4NO3 → 2H2O + N2O – никакая попытка получить нитрат из Н2О и N2O не приводит к положительному результату).
Химически обратимые реакции протекают одновременно при данных условиях как в прямом, так и в обратном направлении. Необратимых реакций меньше, чем обратимых. Примером обратимой реакции служит взаимодействие водорода с иодом:
