Качественный анализ анионов
Систематический ход анализа основан на том, что сначала с помощью групповых реактивов разделяют смесь ионов на группы и подгруппы, а затем уже в пределах этих подгрупп обнаруживают каждый ион характерными реакциями. Групповыми реагентами действуют на смесь ионов последовательно и в строго определенном порядке.
В ряде случаев прибегают не к систематическому разделению ионов, а к дробному методу анализа. Этот метод основан на открытии ионов специфическими реакциями, проводимыми в отдельных порциях исследуемого раствора. Так, например, ион Fe 2+ можно открыть при помощи реактива Кз[Fе(СN)6] в присутствии любых ионов.
Так как специфических реакций немного, то в ряде случаев мешающее влияние посторонних ионов устраняют маскирующими средствами. Например, ион Zn2+ можно открыть в присутствии Fe2+ при помощи реактива (NH4)2[Hg(SCN)4], связывая мешающие ионы Fe2+ гидротартратом натрия в бесцветный комплекс.
Дробный анализ имеет ряд преимуществ перед систематическим ходом анализа: возможность обнаруживать ионы в отдельных порциях в любой последовательности, а также экономия времени и реактивов.
Но так как специфических реакций немного и мешающее влияние многих ионов нельзя устранить маскирующими средствами, в случае присутствия в растворе многих катионов из разных групп прибегают к систематическому ходу анализа, открывая лишь некоторые ионы дробным методом.
Оборудование и посуда
|
Н |
аиболее удобно в обычной практике проводить качественное исследование полумикрометодом. Этот метод не требует больших количеств веществ для анализа, дает значительную экономию времени и реактивов по сравнению с макрометодом. В то же время этот методзначительно проще микрометода, требующего специальной аппаратуры и особых навыков работы.
Для работы полумикрометодом в лаборатории необходимо иметь следующее оборудование.
1. Переносной деревянный штатив с набором капельниц с растворами солей, реактивов, кислот и щелочей и баночек с сухими солями (рис. 1).
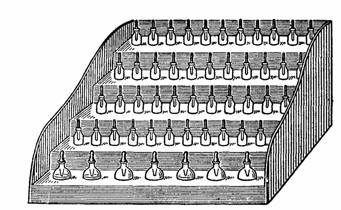
Рис. 1.
2. Штатив для пробирок.
3. Металлический штатив с кольцом, фарфоровым треугольником и асбестированной сеткой.
4. Держатели для пробирок.
5. Центрифужные пробирки (рис. 2).
![]()
Рис. 2.
6. Пробирки цилиндрические.
7. Капиллярные пипетки (рис. 3.).
![]()
Рис. 3.
8. Стеклянные палочки (рис. 4.).
![]()
Рис. 4.
9. Фарфоровые чашки диаметром 3—5 см.
10. Промывалка (рис. 5).
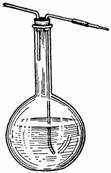
Рис. 5.
11. Предметные стекла.
12. Фарфоровая капельная пластинка (рис. 6).
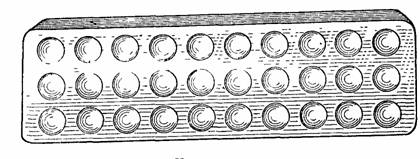
Рис. 6.
13. Предметные стекла с углублениями (рис. 7).
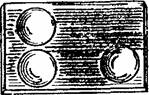
Рис. 7.
14. Ершик для мытья посуды.
15. Водяная баня (рис. 8).
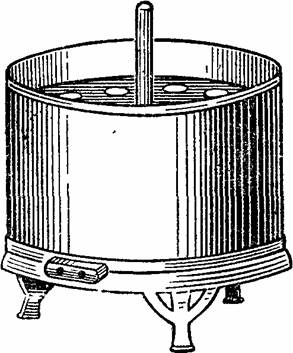
Рис. 8.
16. Центрифуга (рис. 9)
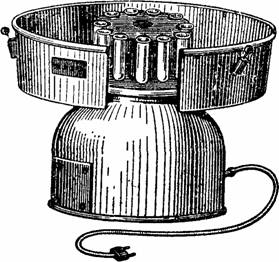
Рис. 9.
Частные реакции, а также операции разделения ионов проводят в конических пробирках для центрифугирования или в маленьких цилиндрических пробирках. В пробирку вносят несколько капель анализируемого раствора и, соблюдая необходимые условия, прибавляют по каплям реактив, помешивая реакционную смесь стеклянной палочкой.
Выполняя реакцию, необходимо следить за тем, чтобы кончик пипетки не касался стенок пробирки во избежание загрязнения реактива. Вынутую из капельницы пипетку по выполнении реакции необходимо сразу же опустить в ту же капельницу.
Вместо пробирок частные реакции можно выполнять также на фарфоровых капельных пластинках (рис. 6) или особых предметных стеклах с углублениями (рис. 7). В этом случае расход реактивов минимальный, а результат реакции хорошо заметен.
Для нагревания реакционной смеси пробирку погружают в кипящую водяную баню. Водяная баня может также служить для упаривания (выпаривания до небольшого объема) растворов. Выпаривание досуха обычно проводят в фарфоровой чашке, нагревая ее на пламени газовой горелки. Пока жидкость не выпарилась до конца, целесообразно ставить чашку на асбестированную сетку. Если остаток от выпаривания необходимо прокалить, чашку ставят на фарфоровый треугольник.
Для отделения осадка от раствора пробирку с осадком помещают в центрифугу.
Классификация анионов и групповые реагенты
|
К |
ак известно из курса неорганической химии, к анионам относятся отрицательно заряженные частицы, состоящие из отдельных" атомов или групп атомов различных элементов. Эти частицы могут нести один или несколько отрицательных зарядов. В отличие от катионов, которые в большинстве своем состоят из одного атома, анионы могут иметь сложный состав, состоящий из нескольких атомов.
Общепринятой классификации анионов не существует. Разными авторами предложены различные системы классификации их.
В настоящем руководстве принята наиболее часто применяемая классификация, по которой все анионы делятся на три аналитические группы в зависимости от растворимости их бариевых и серебряных селей.
В данном случае групповыми реагентами являются растворимые соли бария и серебра (табл. 1).
Таблица № 1
Классификация анионов
| Группа | Анионы | Групповой реагент | Характеристика группы |
| 1 |
SO4 2-, SO3 2- , СO32-, РO43-, SiO3 2- |
Хлорид бария ВаСl2 в нейтральном или слабощелочном растворе |
Соли бария практически нерастворимы в воде |
| 2 |
С1- , Вг- , I-, S2- |
Нитрат серебра AgNO3 и присутствии HNO3 |
Соли серебра практически нерастворимы в воде и разбавленной кислоте |
| 3 |
NO3-, NO2-, CH3COO- |
Группового реагента нет |
Соли бария и серебра растворимы в воде |
