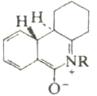
Акридон. Его получение, свойства и применение
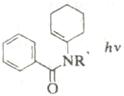
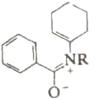
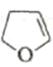
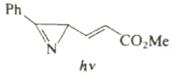
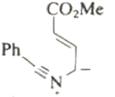
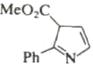
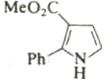
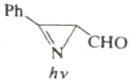
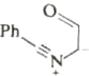
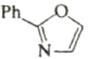
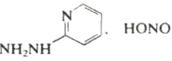
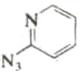
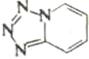
Шестиэлектронные электроциклические процессы типа (в) (рис. 10) – 1,5-биполярное замыкание цикла – более распространены. В этом случае также наблюдаются равновесные процессы замыкания и раскрытия цикла. Нестабильные 1,5-диполи обычно получают in situ и при нагревании превращают в пятичленные гетероциклы. Циклический изомер может быть выведен из равновесия при таутомерном превращении в более стабильное (часто ароматическое) соединение. Примеры 1,5-диполярного замыкания цикла приведены в табл. 5. Пример 1 демонстрирует замыкание цикла в нестабильном 1,5-диполе. В примерах 2 и 3 первоначально образующийся продукт циклизации тау-томеризуется в ароматическое соединение, что смещает равновесие в сторону циклического изомера. Реакции 4 и 5 сразу приводят к образованию ароматических гетероциклов.
Таблица 5. Примеры 1,5-диполярной циклизации.
|
Исходное соединение |
1,5-диполярный интермедиат |
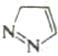
Продукт циклизации |
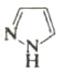
Конечный продукт (если он отличается) |
|
1. |
|
|
_ |
|
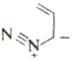
2. Винилдиазометан не может быть выделен, но циклизуется при t>250C. |
|
|
|
|
3. |
|
|
|
|
4. |
|
|
_ |
|
5. |
|
|
_ |
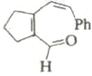
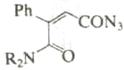
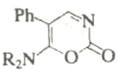
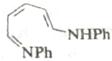
Электроциклические процессы в гетеротриенах [реакция (г), рис. 11)] могут быть применены при синтезе некоторых шестичленных гетероциклов, особенно в тех случаях, когда продукт циклизации способен к ароматизации. Для шестиэлектронных электроциклических процессов, так же как и в других случаях, возможна обратная реакция раскрытия цикла. В некоторых случаях этот обратный процесс более важен с синтетической точки зрения.
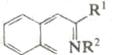
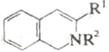
В табл. 6 приведены некоторые примеры синтеза шестичленных гетероциклов с использованием электроциклических процессов Синтез изохинолинов (реакция 4) основан на двух электроциклических реакциях: образовании орто-ксилиленового интермедиата при раскрытии бензоциклобутана и 6π-электронном электроциклическом процессе. Замыкание цикла на второй стадии идет очень легко, так как при этом восстанавливается ароматичность бензольного кольца.
В некоторых случаях электроциклические процессы в гетеротриенах приводят к образованию пятичленных гетероциклов. Вероятность протекания таких процессов увеличивается при наличии электроотрицательного гетероатома в терминальном положении гетеродиена.
Таблица 6. Образование шестичленных гетероциклов электроциклизацией.
|
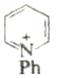
Исходное соединение |
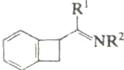
Интермедиат |
Продукт реакции |
|
1. |
_ |
|
|
2. |
|
|
|
3. |
|
|
|
4. |
|
|
|
5. |
|
|
Акридин.
Общие сведения. Акридин является дибензопиридином и относится к хинолину так же, как антрацен к нафталину. Его можно рассматривать как антрацен, в котором одна центральная группа =СН- замещена азотом.
Нумерация атомов производится следующим образом:
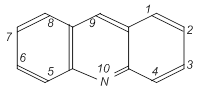
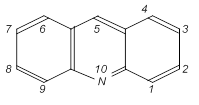
I II
В ряде стран, в том числе в России, принята нумерация I, в других странах (Англия, США) – нумерация II.
Акридин открыт в 1870г. в неочищенной антраценовой фракции каменно-угольного дегтя. Он плавится при 107οС, кипит при 345-346οС, легко возгоняется. Обладает характерным запахом, вызывает раздражение дыхательных путей, раздражает кожу, откуда и произошло название (acer – едкий). Акридин светится при трении (триболюминисценция). Разбавленные растворы имеют синюю флуоресценцию. Соли акридина в разбавленных растворах обладают зеленой флуоресценцией. При дальнейшем разбавлении, вызывающем гидролиз, флуоресценция переходит в синюю, характерную для свободного акридина. Акридиновое ядро составляет основу некоторых алкалоидов. Многие синтетические производные акридина являются ценными лекарственными препаратами и красителями.

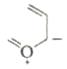
 , нагревание
, нагревание 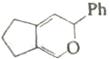
 , нагревание
, нагревание 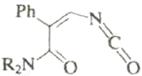
 , нагревание
, нагревание