Аспирин

2.1 Получение.
Салициловая кислота встречается в растительном мире как в свободном состоянии, так и в связанном виде во многих эфирных маслах. В промышленном масштабе ее получают синтетически карбоксилированием фенола. При действии диоксида углерода на твердые феноксиды щелочных металлов образуются фенолокислоты:
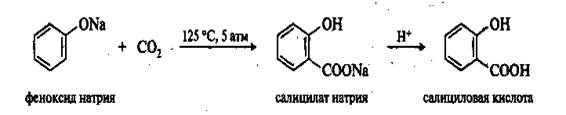
Эта реакция, называемая реакцией Кольбе-Шмитта (1860), является основным способом получения салициловой (2-гидроксибензойной) кислоты.
Механизм реакции Кольбе—Шмитта.
Реакция протекает по механизму электрофилього замещения. Согласно принципу ЖМКО, слабый электрофил - диоксид углерода, являющийся мягкой кислотой, взаимодействует с мягким основным центром амбидентного фенрксид-иона, находящимся в орто-положении. В результате обдуется σ-комплекс, стабилизированный в виде хелата с участием иона натрия. Этот σ-комплекс обычным путем (отщепление протона и возврат к ароматической системе) превращается в салицилат:
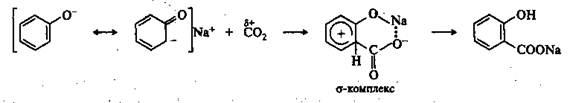
При использовании феноксида калия реакция протекает при более высокой температуре (250—360 °С) и приводит к образованию 4-гидроксибензойной кислоты. В этом случае более стабильным является σ-комплекс, возникающий при атаке пара-положения, поскольку тенденция к образованию хелата уменьшается с увеличением ионного радиуса катиона.
В реакции Кольбе—Шмитта в роли ароматических субстратов используют также фенолы с сильными электродонорными заместителями (м-аминофенол, резорцин, гидрохинон), благодаря чему реакция осуществляется в более мягких условиях: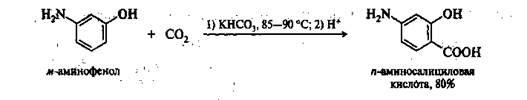
2.2. Свойства
Физические параметры салициловой кислоты:
1. Внешний вид - Салициловая кислота о-НОС6Н4СООН представляет собой кристаллическое вещество;
2. Растворимость ( в воде) -плохо растворимое в воде (1,8 г/л при 20 °С и 20,6 г/л при 80 °С);
3. Температура кипения - 1400С;
4. Температура плавления – 1590С;
5. По кислотности (рКа2,98) она превосходит почти все монозамещенные бензойные кислоты, в том числе и с электроноакцепторными заместителями.
Салициловая кислота обладает антисептическими свойствами и находит применение в медицине и как консервант некоторых пищевых продуктов. Но еще более широко используются в медицинской практике производные салициловой кислоты по обеим функциональным группам. Главным образом, это сложные эфиры по карбоксильной группе — метилсалицилат и фенилсалицилат, имеющий торговое название салол, и по фенольному гидроксилу — ацетилсалициловая кислота, для которой одно из многочисленных торговых названий — аспирин.
Названные производные получают известными способами синтеза сложных эфиров. Так, метилсалицилат образуется при этерификации салициловой кислоты метанолом:

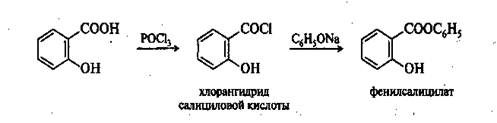
Низкая нуклеофильность фенолов не позволяет таким же способом получить фенилсалицилат. Поэтому салициловую кислоту превращают предварительно в более активный ацилирующий агент — хлорангидрид, которым затем ацилируют фенол:
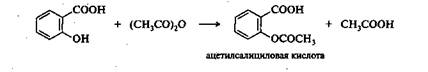
Гидроксильная группа фенола ацилируется под действием уксусного ангидрида с количественным выходом:
Салициловая кислота и ее производные со свободной гидроксильной группой дают с раствором хлорида железа(Ш) фиолетовое окрашивание, характерное для фенолов, что используется в качественном анализе.
3. Роль салициловой кислоты и её производных
в пищевой промышленности и медицине.
Молекула салициловой кислоты состоит из шести атомов углерода, соединенных в кольцо, к которому присоединены функциональные группы, например гидроксильная (комбинация кислорода и водорода: ОН).
Салициловая (о-гидроксибензойная) кислота (Acidum salicylicum) – одна из трех изомерных гидроксибензойных кислот, относящихся к группе фенолокислот. Получила свое название от латинского названия ивы – Salix. В коре ивы содержится гликозид салицин, при гидролизе которого получен фенолоспирт салигенин C6H4(OH)CH2OH. При окислении салигенина получена салициловая кислота:
C6H4(OH)CH2OH C6H4(OH)COH C6H4(OH)COOH
cалигенин салициловый салициловая
альдегид кислота
В настоящее время салициловая кислота производится в промышленности методом прямого карбоксилирования фенола диоксидом углерода (реакция Кольбе). Диоксид углерода представляет собой слабый электрофильный реагент, поэтому для осуществления реакции необходимо усиление нуклеофильных свойств субстрата. В связи с этим реакцию проводят не с самим фенолом, а с его натриевой солью, так как феноксид-ион более сильный нуклеофил, чем фенол. Реакцию осуществляют в автоклавах при нагревании под давлением. Затем реакционную смесь подкисляют и выделяют салициловую кислоту:
С6H5-ONa + CO2 = C6H5-OH С6H4-OH
фенолят натрия ê ½
COONaCOOH
салицилат салициловая
натрия кислота
При нагревании салициловая кислота легко декарбоксилируется с образованием фенола:
С6H4(OH)COOH=C6H5OH + CO2
Салициловая фенол
кислота
В салициловой кислоте имеется внутримолекулярная водородная связь, стабилизирующая карбоксилат-ион, что приводит к повышению ее кислотности (рКа 2,98) сравнительно с бензойной (рКа 4,20) и п-гидроксибензойной (рКа 4,58) кислотами.
Салициловая кислота дает с FeCl3 фиолетовое окрашивание не только в водном, но и в спиртовом растворе (в отличие от фенола).
При действии гидроксида щелочного металла салициловая кислота растворяется с образованием фенолятосоли щелочного металла, например:
C6H4-COOH + 2 NaOH = C6H4-COONa + 2 H2O
ú½
OHONa
фенолят натрия
При действии на салициловую кислоту карбонатов щелочных металлов проявляется различная степень кислотности карбоксила и фенольного гидроксила; при этом происходит образование солей. Карбоксильная группа салициловой кислоты разлагает карбонаты щелочных металлов, вытесняя слабую угольную кислоту, тогда как фенольный гидроксил, обладающий более слабыми кислотными свойствами, чем угольная кислота, неспособен разлагать эти соли и поэтому остается свободным:
2 C6H4-COOH + Na2CO3= 2 С6H4-COONa + H2O + CO2
