Действие озона на насыщенные полимеры
Следует отметить, что кинетика изменения молекулярной массы ПЭ изучена недостаточно. В частности, наряду с деструкцией следует ожидать сшивания, как это имеет место для ПС. Конкуренцию между сшиванием и распадом макромолекул при изменении условий опыта, связанную с изменением соотношения скоростей рекомбинации и распада промежуточных радикалов, наблюдали при исследовании действия озона на атактический ПП (рис. 13) [46]. Основными продуктами (свыше 80% от общего выхода) являются кетоны и кислоты в соотношении ~3: 1 [47]. Их обычно идентифицируют по поглощению в области 1700–1750 см-1 ИК-спектра. Поглощение карбоксильной группы обычно накладывается в виде длинноволнового плеча на поглощение карбонила (рис. 14). Эти полосы легко разделяются при обработке образцов растворами щелочей. Поглощение образующегося при такой обработке карбоксилат-иона лежит в области ~1580 см-1. На рис. 14 приведены характерные области ИК-спектра для озонированных кристаллов ПЭ до и после обработки щелочью [43].
По сравнению с другими методами обработки поверхности, например плазменным или коронным разрядом, действие озона сопровождается монотонным накоплением карбонильных и карбоксильных групп в образце, в то время как в остальных случаях содержание этих групп быстро запределивается [47]. В меньшей степени протекают и деструктивные процессы. При обработке озоном образец обычно прибавляет в весе, тогда как обработка в коронном разряде сопровождается потерей веса.
Накопление функциональных групп на поверхности образцов сильно изменяет физические свойства поверхности, увеличивается поверхностное натяжение, значительно возрастает адгезия. В литературе дискутируется влияние природы образовавшихся функциональных групп на величину адгезии. В частности, в работе [15] показано, что дополнительная обработка кетогрупп на поверхности ПЭ ацетилхлоридом, уксусной кислотой, бромом и другими реагентами не в силах заметно улучшить адгезию и, как правило, даже ее ухудшает. Авторы приходят к заключению, что большой вклад в адгезию вносят енолы, образующиеся из кетонов, и большинство реагентов, препятствующих енолизации или реагирующих с активным водородом оксигруппы енола, снижают адгезию.
Действие озона на ПЭ и другие полимеры сопровождается образованием перекисных радикалов [7, 20, 48]. При исследовании [29] процессов образования радикалов в реакции с озоном 0,15–0,3 г порошка полимера вносили в ампулу (d~6 мм), помещенную в резонатор ЭПР-спектрометра. и через капилляр подавали озоно-кислородную смесь, содержащую 2,2-•10–3 моль/л 03. Через 2–3 мин после начала подачи озона возникали парамагнитные частицы, концентрация которых в дальнейшем либо оставалась постоянной, либо изменялась. Результаты этого исследования приведены ниже.
![]()

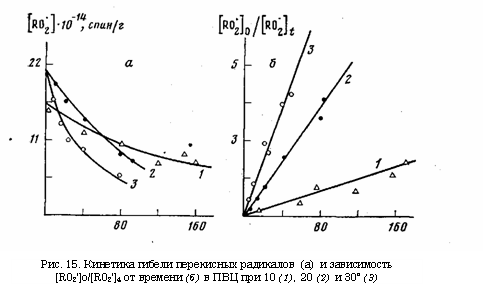
В ПС, ПВЦ и поликарбонате формы сигнала ЭПР сходны с сигналом перекисного радикала. В ПЭ возникал сигнал более сложной формы, который, возможно, представляет собой наложение сигналов двух различных радикалов. После прекращения подачи озона перекисные радикалы исчезали в течение нескольких минут; в полимерах, содержащих ароматические кольца, вместо них появлялись парамагнитные частицы, дающие узкий синглетный спектр (Д#=8,5 Э). Повторная подача озона в систему приводит к превращению этих частиц в перекисные радикалы. В отсутствие озона концентрация частиц практически не изменяется в течение месяца, а при повышении температуры они постепенно расходуются. Кинетика гибели перекисных радикалов была изучена на примере ПВЦ. Результаты опытов по изучению гибели перекисных радикалов в ПВЦ на воздухе для различных температур приведены на рис. 15. Как следует из рисунка, после прекращения подачи озона концентрация радикалов постепенно уменьшается, при этом изменения формы ЭПР-спектра не происходит. Скорость гибели перекисных радикалов подчиняется закону второго-порядка. Измеряя абсолютные начальные концентрации радикалов, удалось определить значения кинетических параметров реакции, а из температурного хода константы скорости оценить энергию активации гибели радикалов. Зависимость константы скорости от температуры можно описать уравнением
![]()
где AZ=F/sZ (V – объем полимера, s – удельная поверхность, I – средняя толщина поверхностного слоя, в котором сосредоточены радикалы).
С одной стороны, образующиеся при озонировании перекисные радикалы жестко связаны с полимерной матрицей и при температурах ниже температуры стеклования их подвижность явно недостаточна для того, чтобы объяснить наблюдаемую на опыте скорость рекомбинации. С другой стороны, при озонировании ПС и ПЭ [27, 49] отношение количества продуктов окисления к количеству поглощенного озона приближается к единице, что позволяет считать вклад эстафетной передачи в транспорт свободной валентности незначительным.
Исследование процессов накопления продуктов озонирования ПС и ПЭ [27, 49] показало, что кинетика образования перекисных соединений хорошо согласуется с предположением о преимущественном распаде первичных перекисных радикалов.
По-видимому, при низких температурах миграция свободной валентности определяется главным образом реакциями, следующими за распадом перекисных радикалов по схеме, включающей ряд элементарных стадий
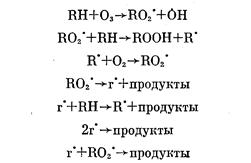
Промежуточными являются оксирадикалы, перекисные радикалы со свободной валентностью на конце цепи или низкомолекулярные радикалы, которые обладают большей подвижностью и в результате встречи с другими радикалами обусловливают гибель свободной валентности. При стационарных концентрациях R» и г» и при условии малой скорости рекомбинации г» из-за их низкой концентрации можно показать, что перекисные радикалы должны гибнуть по закону второго порядка [27, 49]. Анализ лит. данных [50, 51] показывает, что в полимерах, содержащих аморфные и кристаллические области, рекомбинация перекисных радикалов, равномерно распределенных по объему образца, не соответствует ни первому, ни второму порядку. В этом случае процесс рекомбинации можно представить суперпозицией двух реакций второго порядка с различными константами скорости для аморфной и кристаллической областей. Однако при изучении гибели радикалов, образовавшихся в ПВЦ под действием озона, отклонения от закона второго порядка не наблюдались. Видимо, вследствие высокой лабильности С–Н-связи у третичного углерода в ПВЦ, а также вследствие малого времени экспозиции в озоне перекисные радикалы при озонолизе сосредоточены лишь в поверхностном слое образца. Толщина этого слоя в аморфных областях за счет разницы в коэффициентах диффузии озона значительно больше, чем в кристаллических, и здесь находится подавляющее большинство радикалов. Поэтому кинетические кривые гибели радикалов точно описываются уравнением бимолекулярной реакции, а величина энергии активации совпадает с найденной Лебедевым [50] энергией активации гибели перекисных радикалов в аморфной фазе тефлона.
