Исследование свойств продуктов циклизации алициклического 1,5,9-трикетона
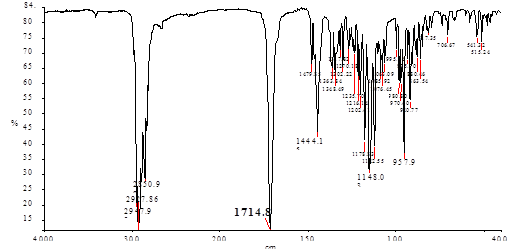
20,21-Диоксагексацикло[10.8.2.01,6.08,19.08,22.014,19]докозан-22-ол (5).
| |
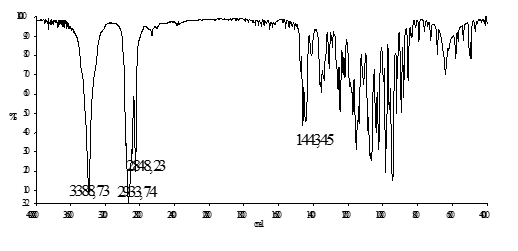
Рис. 2. ИК спектр соединения 5 в КВr.
Данные спектра ЯМР 13С (d, м.д.) (наиболее характерные сигналы) [16]: четвертичные углероды, связанные с кислородом С22, С1 и С19 при 98.2, 96.1 и 79.0, четвертичный углерод С8 при 37.8, третичные углероды С6, С12, С14 при 41.1, 39.8, 39.6.
После выделения соединения 5 мы исследовали реакционные смеси. Например, реакционную смесь, оставшуюся от синтеза соединения 5 по методу Колонжа анализировали методом ГЖХ-МС. В ней содержатся 2 изомера дикетона 1 (30 %, соотношение 1:1,), 2 изомера кетола 3 (40 %, соотношение 1:1), 2 изомера соединения 5 (9 %, соотношение 1:2), трикетон 2 (6 %) и циклогексанон (11 %).
Те же продукты содержатся в реакционной смеси после отделения соединения 5 при синтезе по методике Тиличенко.
2. Термическая дециклизация соединения 5
Тиличенко установил, что соединение 5 при температуре плавления 193 ºС, превращаясь в расплав, переходит в трикетон 2 (в чистом виде он не был выделен), а тот в свою очередь под действием щелочи количественно превращается вновь в соединение 5. Однако были неизвестны оптимальные условия превращения 5 ® 2, количество образующихся стереоизомеров трикетона (теоретически их может быть шесть), их соотношение. Ответ на эти вопросы мы получили с помощью ГЖХ-МС.
Внутримолекулярная циклизация трикетона 2, изученная ранее [14], представлена на схеме (5):
Схема 5

Мы изучили дециклизацию соединения 5 при температуре его плавления 193 0С, а также при 210 0С, оставляя расплав при указанных температурах на 5, 10, 30 и 60 минут. Опыт показал, что в самых мягких условиях (193 0С, 5 мин) образуется смесь пяти стереоизомеров с близкими временами удерживания (15.7, 15.8, 16.07, 16.48, 17.41), одинаковым распадом в масс-спектре и в соотношении (%) 23:10:11:48:2 соответственно. Примесей промежуточных продуктов дециклизации 20, 22 не обнаружено. При увеличении времени выдержки расплава до 30 мин соотношение изменяется (17:13:17:45:9), а в самых жестких условиях (210 0С, 60 мин) оно становится равным 6:19:20:34:8 соответственно. Эти данные показывают, что в первоначальный момент в смеси преобладает один стереоизомер - до 48 %, а при увеличении температуры или времени выдержки его доля падает до 34 %, изменяется доля и других стереоизомеров. Это связано, по-видимому, с взаимопревращением стереоизомеров в расплаве в результате кето-енольной таутомерии.
При обработке смеси спиртовым раствором 1н NaOH при 20 0С происходит полное превращение всех стереоизомеров в один и тот же продукт 5 с незначительной примесью его стереоизомерной формы. Выделить какой либо стереоизомер трикетона 2 в индивидуальном виде нам не удалось.
ИК спектр стереоизомерной смеси трикетона 2 содержит полосу поглощения карбонильной группы циклогексанона при 1705 см-1 (рис. 3).
Рис. 3. ИК спектр соединения 2 в СНСI3.
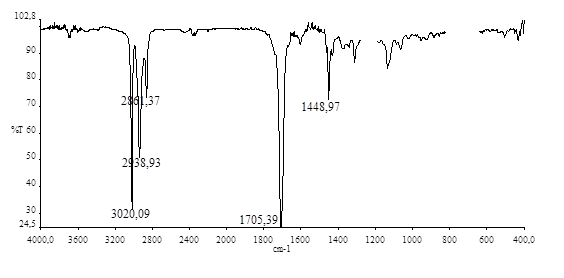
Попытка выделения индивидуального трикетона за счет предполагаемой разности в растворимости стереоизомеров к успеху не привела.
3. Дегидратация соединения 5
Рассчитывая получить соединения 20, 22, мы изучили реакцию дегидратации соединения 5 в различных растворителях (серный эфир, ТГФ, бензол, этанол) под действием кислот (p-TsOH, HCI) при 20 0С. Исходное соединение возвращалось неизменным. Однако при кипячении в уксусной кислоте (20 мин, Т=130 °С) и последующей нейтрализации раствором соды с выходом 84 % получили кетон 22. Его структура была доказана на основании ГЖХ-МС, ИК и ЯМР 1Н, 13С-спектроскопии.
Рис. 4. Хроматограмма и масс-спектр
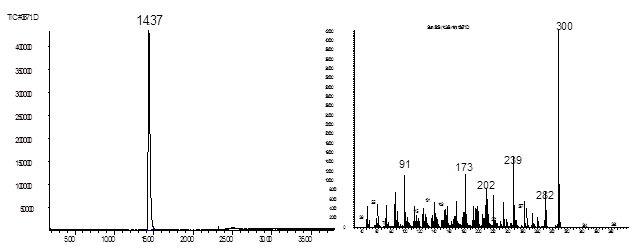
|
В ИК спектре (рис. 5) содержится полоса поглощения карбонильной группы при 1715 см-1.
В спектре ЯМР 1Н (рис. 6) содержится синглетный сигнал протонов метиленовой группы (2Н, С2-Н) в области 2.5 м.д.
 В спектре ЯМР 13С (рис. 7) содержатся сигнал углерода карбонильной группы (С21) при 217.10, четвертичных углеродов при двойной связи: С8, связанного с О-атомом при 142.60 и С3 при 103.82, четвертичного углерода (С10), связанного с О-атомом при 82.4,четвертичного углерода (С1) при 51.26, а также два сигнала третичных углеродов (С15 и С17) при 39.74, 46.38.
В спектре ЯМР 13С (рис. 7) содержатся сигнал углерода карбонильной группы (С21) при 217.10, четвертичных углеродов при двойной связи: С8, связанного с О-атомом при 142.60 и С3 при 103.82, четвертичного углерода (С10), связанного с О-атомом при 82.4,четвертичного углерода (С1) при 51.26, а также два сигнала третичных углеродов (С15 и С17) при 39.74, 46.38.
4. Реакция восстановительного гидроаминирования по Лейкарту
Соединение 5 мы ввели в реакцию гидроаминирования по Лейкарту. Как указано в литобзоре, эта реакция была проведена с трикетоном 14 при микроволновом облучении с формиатом аммония в этиленгликоле [22].
Сначала эту реакцию мы провели также с формиатом аммония в диметиловом эфире диэтиленгликоля (диглим), со смесью карбоната аммония и 85 % муравьиной кислоты в диглиме при микроволновом облучении. При этом было выделено исходное соединение в очищенном виде. В диглиме происходит перекристаллизация соединения 5. Его сложно перекристаллизовать из других растворителей, так как в этом случае образуется продукт, не дающий узкого интервала температуры плавления, что объясняется примесью продуктов дециклизации. И именно неудавшаяся реакция Лейкарта в диглиме помогла найти идеальный растворитель для перекристаллизации. В условиях классической реакции Лейкарта (HCONH2, HCOOH, при нагревании) нами были выделены три новых гетероциклических соединения.
Реакция проводилась при 160-175 °С в формамиде с 85-%-ной муравьиной кислотой. Мы учитывали, что в растворе при нагревании соединение 5 может существовать в виде смеси промежуточных продуктов циклизации (схема 5), содержащих карбонильные группы, а потому можно было ожидать образования разнообразных соединений.
После проведения реакции мы получили трехкомпонентную смесь, из которой с 60 % выходом выкристаллизовывалось соединение 23. Оставшийся фильтрат по данным ГЖХ-МС состоял из смеси соединений 24 и 25 в соотношении 1:2 и примеси соединения 23. После отгона формамида и разбавления остатка водой выпадал осадок соединения 24 (М 303), а после экстракции водного раствора выделили соединение 25 с выходом около 2 %.