Каталитический риформинг
Дегидроизомеризация пятичленных нафтенов, формула 2
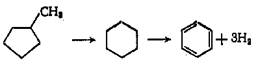 (2)
(2)
Ароматизация (дегидроциклизация) парафинов, формула 3
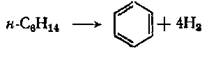 (3)
(3)
Изомеризация углеводородов - другой тип реакций, характерных для каталитического риформинга. Наряду с изомеризацией пятичленных и шестичленных нафтенов, изомеризации подвергаются как парафины, так и ароматические углеводороды.
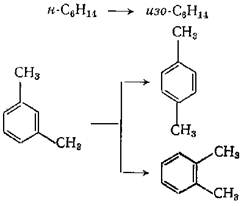
Рисунок 1 – изомеризация парафинов и ароматических углеводородов.
Существенную роль в процессе играют также реакции гидрокрекинга. Гидрокрекинг парафинов, содержащихся, в бензиновых фракциях, сопровождается газообразованием, формула 4
С8Н18 + Н2 → С5Н12 + С3Н8 (4)
что ухудшает селективность процесса. С другой стороны, аналогичная реакция гидродеалкидирования алкилбензолов позволяет увеличить выход низкомолекулярных гомологов бензола, которые представляют наибольший практический интерес, формула 5
С6Н5С3Н7 + Н2 → С6Н6 + С3Н8 (5)
Протекают также реакции, приводящие к раскрытию циклопентанового кольца и к превращению пятичленных нафтенов в парафины, формула 6
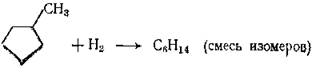 (6)
(6)
Элементарные стадии ряда приведенных реакций предопределяются бифункциональным характером катализаторов рифрминга. С одной стороны, они содержат один металл (платину) или несколько металлов (например, платину и рений, или платину и иридий), которые катализируют реакции гидрирования и дегидрирования. С другой стороны, носителем служит промотированный галогенами оксид алюминия, обладающий кислыми свойствами и катализирующий реакции, свойственные катализаторам кислотного типа. Поэтому разные элементарные стадии реакции могут протекать на различных участках поверхности катализатора: металлических или кислотных. В качестве примера можно сослаться на реакцию изомеризации нормального парафина. Сперва такой углеводород дегидрируется до нормального олефина на металлическом участке, далее нормальный олефин изомеризуется на кислотном участке в изоолефин, который затем подвергается гидрированию на металлическом участке, превращаясь в изопарафин. Не только в этой, но и в ряде других реакций каталитического риформинга, важнейшие элементарные стадии - гидрирование и дегидрирование углеводородов.
Сырье каталитического риформинга обычно подвергают гидрогенизационной очистке, после чего в нем остается крайне незначительное количество примесей, в частности серо- и азотсодержащих соединений, являющихся каталитическими ядами. В условиях каталитического риформинга они подвергаются гидрогенолизу с отщеплением сероводорода, формула 7, и аммиака, формула 8
RSR + 2Н2 → 2RH + H2S (7),
RNHR + 2H2 → 2RH + NH3 (8)
2 Превращения шестичленных нафтенов
2.1 Реакции дегидрирования
Дегидрирование шестичленных нафтенов - основное направление их превращения в условиях каталитического риформинга. Скорости дегидрирования шестичленных нафтенов на платиновых катализаторах риформинга весьма велики и намного превышают скорости их дегидрирования на других металлических и оксидных катализаторах, показанную в таблице 2.
Таблица 2 − Сравнительная активность катализаторов в реакции дегидрирования циклогексана.
|
Катализатор |
* r, моль/(г с) |
Катализатор |
* r, моль/(г с) |
|
34% Сr2O3/Al2O3 |
0,5 |
1% Pd/Al2O3 |
200 |
|
10% MoO3/Al2O3 |
3 |
5% Ni/SiO2 |
320 |
|
5% Ni/Al2O3 |
13 |
1% Rh/Al2O3 |
890 |
|
5% Co/Al2O3 |
13 |
0.5 Pt/Al2O3 |
1400-4000 |
Достаточно отметить, что скорость дегидрирования циклогексана на платиновых катализаторах в 500-1300 раз больше скорости той же реакции на алюмомолибденовом катализаторе, который сравнительно недавно еще применялся в процессе риформинга бензиновых фракций. При таких скоростях реакции степень дегидрирования шестичленных нафтенов может в значительной мере предопределяться условиями химического равновесия для той реакции.
Химическое равновесие. Реакции дегидрирования шестичленных нафтенов в ароматические углеводороды обратимы, формула 9
![]() (9)
(9)
Зная константу равновесия Кр, можно вычислить равновесные концентрации реагирующих веществ, формула 10
![]() (10)
(10)
Ниже приведены логарифмы констант равновесия для реакций дегидрирования циклогексана и некоторых его гомологов при температурах от 400 до 550 °С, таблица 3
Таблица 3 – Логарифмы констант равновесия для реакций дегидрирования циклогексана и некоторых его гомологов
|
Углеводороды |
408 °С |
450 °С |
500 °С |
550 °С |
|
Циклогексан |
3,70 |
4,88 |
5,91 |
6.82 |
|
Метилциклогексан |
4,19 |
5,36 |
6,33 |
7,28 |
|
Этилциклогексан |
4,23 |
5.36 |
6,34 |
- |
|
н – Пропилциклогексан |
4,26 |
5,39 |
6,37 |
- |
|
1, 2, 4 – Триметилциклогексан |
5,11 |
- |
- |
- |
