Качественный анализ неизвестного вещества
Комплексонометрическое титрование используют также для анализа различных сплавов, определения сульфатов, фосфатов и других анионов, для анализа органических соединений.
Физико-химические методы установления точки эквивалентности в комплексонометрии[3]
Различные физико-химические методы обычно используют для установления оптимальных условий титрования. Кроме того, с помощью физико-химических методов можно проводить определения элементов, для которых еще не найдены цветные индикаторы. Потенциометрическое титрование комплексоном выполняют с помощью ионоселективных электродов или используют инертные электроды из благородных металлов, реагирующие на изменения окислительно-восстановительного потенциала системы. С помощью биметаллической пары электродов платина-вольфрам можно титриметрически определить свинец, медь, цинк, никель, кадмий и другие элементы. Широко применяют амперометрическое титрование ЭДТА для определения никеля, цинка, кадмия, свинца. Используют кондуктометрическое, фотометрическое, термометрическое и другие виды титрования комплексоном с физико-химической индикацией точки эквивалентности.
2.3 Расчет кривой титрования методом комплексонометрии
Оценить возможность титриметрического определения и построить кривую титрования для следующих данных 0,05М ZnCl2 0,025M Na2H2Y, pH 9, концентрация аммиака 0,1 моль/л.
Запишем уравнение титриметрической реакции:
Zn2++ H2Y2-→ZnY2-+2H+
Расчет кривой титрования сводится к расчету показательной концентрации Zn2+ в зависимости от объема титранта. Устойчивость ZnY2- зависит от кислотности среды (чем выше кислотность, тем ниже устойчивость), в связи с этим для связывания ионов водорода, количественное определение ZnCl2 проводят в среде аммонийного буфера.
Рассчитаем объем титранта по закону эквивалентов:
![]() (1)
(1)
откуда
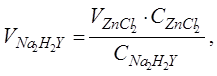 (2)
(2)
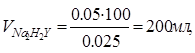
Наличие иона Н+ в среде, где присутствует трилон В, приводит к протеканию следующих конкурирующих реакций:
Y4-+H+ « HY3-, ![]() = K4;
= K4;
HY3-+H+ « H2Y2-, ![]() = K3;
= K3;
H2Y2-+H+ « H3Y-, ![]() = K2;
= K2;
H3Y-+H+ « H4Y, ![]() = K1;
= K1;
где K1, K2, K3, K4 – константы ступенчатой диссоциации H4Y (K1=1,0.10-2, K2=2,1.10-3, K3=6,9.10-7, K4=5,5.10-11)[5].
Рассчитаем условную константу устойчивости, которая выражает прочность комплексов цинка с трилоном В:
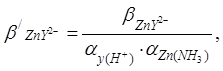 (3)
(3)
![]()
Рассчитаем коэффициенты конкурирующих реакций:
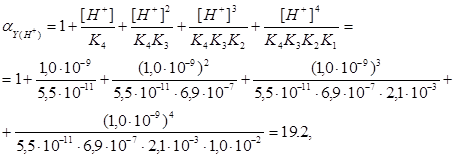 (4)
(4)
Zn2+ участвует также в конкурирующих реакциях образования комплексных соединений с аммиаком NH3 в соответствии со следующими уравнениями реакций:
n2++NH3![]() Zn(NH3)2+,
Zn(NH3)2+,
Zn2++2NH3![]() Zn(NH3)22+,
Zn(NH3)22+,
Zn2++3NH3![]() Zn(NH3)32+,
Zn(NH3)32+,
Zn2++4NH3![]() Zn(NH3)42+,
Zn(NH3)42+,
![]() (5)
(5)
По данным литературного источника[5]
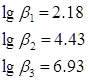
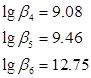
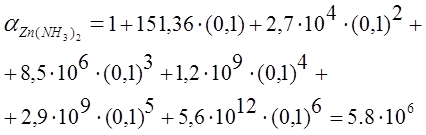
Подставив, выражения (4) и (5) в уравнение константы устойчивости (3) получим:
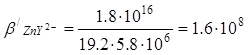
1) до начала титрования, в отсутствии конкурирующих реакций с участием цинка, концентрация ионов Zn2+ равна концентрации соли ZnCl2
ZnCl2 →Zn2++2Cl-
[Zn2+]=C![]() =0.05 моль/л
=0.05 моль/л
2)до точки эквивалентности величина pZn определяется концентрацией неоттитрованного иона цинка уравнение (а), так диссоциацией комплексоната, образующегося по уравнению(б) при избытке ионов цинка можно пренебречь.
а)Zn2++H2Y2-→ ZnY2-+2H+
б)ZnY2- ↔Zn2++Y4-.
![]() дис.
дис.
![]() (6)
(6)
Проведем расчет для точек ![]()
3) В точке эквивалентности расчет концентрации ионов Zn2+ проводится с учетом уравнения реакции диссоциации комплекса:
ZnY2-↔Zn2++Y4-
Данное равновесие количественно описывается константой:
 (7)
(7)
[Zn2+] = [Y4-] = x,
[ZnY2-] = [ZnCl2],
![]() ,
,
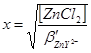 ,
,
![]() ,
,
[Zn2+] = 1,8 ∙ 10-5
pZn = 4.7
4)после точки эквивалентности концентрация комплексоната металла остается постоянной
Концентрация ионов лиганда определяется избытком добавленного титранта:
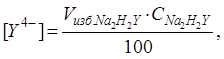 (8)
(8)
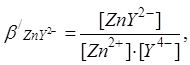 (9)
(9)
откуда :
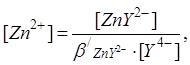
Для найденных значений [Zn2] и [Y4-] вычисляются значения pZn2+ и pY4- и строится кривая титрования в координатах pZn2+- Vтитранта. Проводится анализ кривой титрования, рассчитывается скачок титрования, выбирается индикатор.
В таблице 3 представлены данные расчета изменений концентрации ионов определяемого вещества и титранта в зависимости от объема добавляемого титранта (при условии что объем раствора в процессе титрования не изменяется).
Таблица 3-Изменение pZn при титровании трилоном Б.
|
Ŋ |
VТ,мл |
[Y4-] |
pY4- |
[Zn2] |
pZn2+ |
|
0 |
0 |
- |
- |
0.05 |
1.3 |
|
0.1 |
20 |
- |
- |
0.025 |
1.6 |
|
0.2 |
40 |
- |
- |
0.02 |
1.7 |
|
0,4 |
80 |
- |
- |
0.015 |
1,8 |
|
0.8 |
160 |
- |
- |
0.005 |
2.3 |
|
0.9 |
180 |
- |
- |
0.0025 |
2.6 |
|
0.99 |
198 |
- |
- |
0.00025 |
3.6 |
|
0.999 |
199.8 |
- |
- |
0.000025 |
4.6 |
|
1 |
200 |
- |
- |
1.8.·10-5 |
4.7 |
|
1.001 |
200.2 |
5·10-5 |
4.3 |
3.125·10-6 |
5.5 |
|
1.01 |
202 |
5·10-4 |
3.3 |
3.12·10-7 |
6.5 |
|
1.05 |
210 |
2.5·10-3 |
2.6 |
6.2·10-8 |
7.2 |
|
1.1 |
220 |
5·10-3 |
2.3 |
3.1·10-8 |
7.5 |
|
1.2 |
240 |
0.01 |
2 |
1.5·10-8 |
7.8 |
|
1.8 |
360 |
0.04 |
1.4 |
3·10-9 |
8.4 |
|
2 |
400 |
0.05 |
1.3 |
3.12·10-9 |
8.5 |
