Методы органического синтеза
О – алкилирование проводят при температурах не выше 100 С в воде или органических растворителях, например:
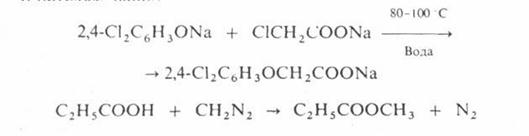
N – алкилирование аминов спиртами осуществляют в газовой фазе в присутствии кислотных катализаторов при 200–300 °С, напр.:
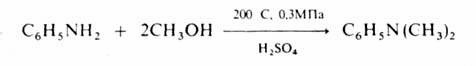
Получение алкильных производных металлов проводят в присутствии меди, например:

Алкилирование углеводородов сопровождается полиалкилированием, изомеризацией и полимеризацией. Так, при этилировании бензола по р-ции Фриделя – Крафтса, кроме этилбензола, образуются ди- и полиэтилбензолы. Полиалкилирование объясняется лучшей растворимостью в образующемся каталитическом комплексе алкилатов по сравнению с исходным в-вом. При использовании в качестве растворителя нитрометана идет преимущественное образование моноалкилпроизводных. Для увеличения выхода моноалкилпроизводных уменьшают мольное соотношение олефин: бензол, а также проводят рециркуляцию полиалкилпроизводных, в результате которой идет их деалкилирование.
Механизм алкилирования наиболее подробно изучен на примере С‑и О – алкилирования реакции с участием алкилгалогенидов, спиртов, сложных эфиров протекают следующим образом:
![]()
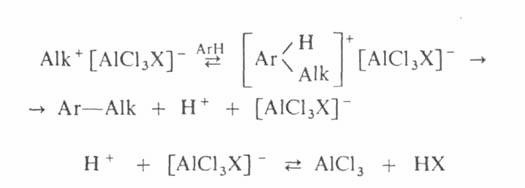
Поскольку третичные алкилгалогениды ионизируются легче всего, вторичные – труднее, а первичные практически не ионизируются, вероятность образования соответствующих карбкатионов уменьшается в том же ряду. Такое же влияние строения алкилирующего агента отмечено при О – алкилировании, которое в целом протекает как нуклеофильное замещение у насыщенного атома углерода:
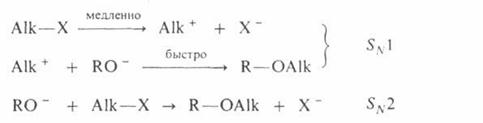
Помимо приведенных выше реакций, алкилирование применяют в лабораторной практике для получения алкильных производных карбонильных соединений, дикарбонильных соединения, при хлорметилировании ароматических углеводородов:
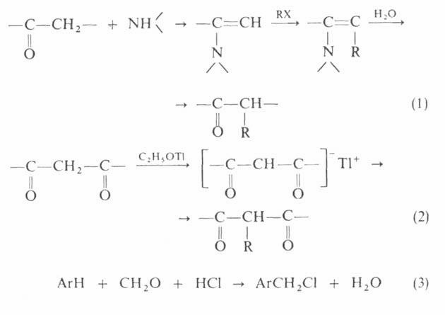
Алкилирование широко применяется в промышленности, в частности для получения алкилата, этилбензола, изопропилбензола, высших алкилбензолов.
Реакции конденсации
Исторически закрепившееся в органической химии название большой группы реакций различного характера. В более узком значении – внутри- и межмолекулярные процессы образования новой связи С–С в результате взаимодействия двух или более молекул органических соединений. Реакции конденсации можно разбить на след. группы: 1. Замещение атома или группы атомов с отщеплением простой неорганической или органической молекулы:
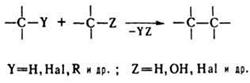
В качестве конденсирующих агентов используют в-ва, которые связывают отщепляющиеся соединения, образуют реакционноспособные промежуточные продукты или действуют как катализаторы. Реакции конденсации с отщеплением воды могут проходить по одной из след. схем:
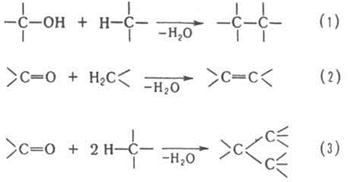
Схеме (1) соответствуют алкилирование ароматических и непредельных соединений спиртами, автоконденсация жирных спиртов, например:
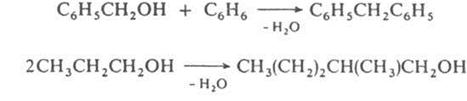
По схеме (2) протекают кротоновая конденсация и многочисленные родственные процессы, например Перкина реакция, Кнёвенагеля реакция и др.; по схеме (З) – многие синтезы ряда трифенилметана, например:
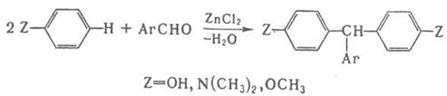
Отщепление воды катализируется обычно кислотами и основаниями, такими, как H2SO4, HCl, АlСl3, ZnCl2, NaOH, NaOR, NaNH2, NaH, RNH2. Некоторые реакции, сопровождающиеся образованием связи углерод–гетероатом или гетероатом–гетероатом, также относят к реакциям конденсации, например:
![]()
Под действием металлов реакции конденсации происходят с отщеплением атомов галогена от двух молекул орг. галогенида (Вюрца реакция, Ульмана реакция). Реакции конденсации с отщеплением водорода могут осуществляться пиролитически либо под действием окислителей, например:
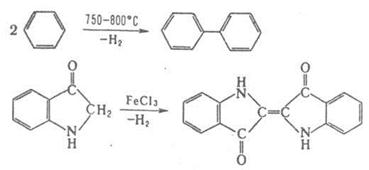
Ряд процессов реакции конденсации сопровождается отщеплением молекул орг. соединения, например спиртов. К этому типу принадлежат сложноэфирная конденсация, Клайзена конденсация, Дикмана реакция. Конденсирующие агенты – щелочные металлы, орг. и неорг. основания. Обычно к К. р. не относят этерификацию, переэтерификацию, алкилирование и ацилирование по гетероатомам, однако происходящие по этим схемам процессы образования полимеров называют поликонденсацией. 2. Присоединение молекулы органического соединения по кратной связи другой молекулы:
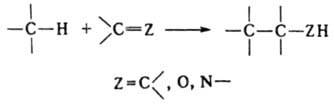
Сюда относят, например, многочисленные случаи альдольной конденсации, зачастую представляющей собой предварительную стадию кротоновой конденсации, Михаэля реакцию, бензоиновую и ацилоиновую конденсации, диеновый синтез, а также реакции гидро- и карбометаллирования олефинов и ацетиленов.
Диазотирование
Способ получения ароматических диазосоединений, заключающийся обычно в действии NaNO2 на первичные ароматические амины в присутствии минеральной к-ты НХ:
![]()
Диазотирование проводят в воде, концентрированных кислотах, реже – в неводных средах. Поскольку реакция экзотермична, а диазосоединения при нагревании легко разлагаются, реакционная смесь обычно охлаждают, поддерживая температуру в интервале 0–10 °С. При недостатке кислоты могут образовываться диазоамино- и аминоазосоединения. Производные о-аминонафтолов при диазотировании окисляются; для предотвращения этого в реакционную смесь добавляют соли Сu или Zn. Механизм диазотирования включает нитрозирование свободного амина с последующим отщеплением Н2О от катиона N‑нитрозаммония (I) или ОН – от N‑нитрозамина (II):
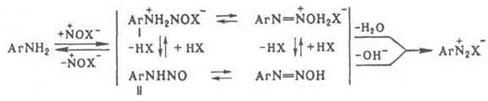
Нитрозирующий агент NOX образуется по р-ции: NO2- + + 2Н+ + Х- D NOX + Н2O, где X = ОН, ОС(О) CН3, OSO3H, NO2, Hal и др. (X расположены в порядке возрастания активности NOX). Наиболее активный агент – свободный нитрозоний – катион NO+; он образуется только в концентрированной серной или хлорной к-те. Если NOX образуется быстрее, чем катион N – нитрозаммония, скорость диазотирования зависит от концентрации амина. Чем ниже кислотность среды, тем выше концентрация NO2- и ОН-, а следовательно, и концентрация малоактивных частиц N2O3 и HNO2, в результате чего скорость диазотирования должна снижаться. Однако одновременно увеличивается концентрация свободного амина, что приводит к увеличению скорости диазотирования. С увеличением кислотности среды, как правило, увеличивается концентрация наиболее активных NOX, однако уменьшается концентрация свободного амина, что приводит к снижению скорости диазотирования. Поэтому в слабокислой среде диазотируют более основные амины, в сильнокислой – менее основные, в концентрированной H2SO4 с помощью нитрозилсерной к-ты – амины крайне низкой основности (например, полинитроанилины). Чтобы увеличить скорость последней р-ции, среду разбавляют ледяной СН3СООН, сдвигая равновесие в сторону образования свободного амина. При диазотировании обычно к р-ру или мелкодисперсной суспензии соли амина в к-те прибавляют NaNO2, взятый с небольшим избытком. При использовании плохо растворимых аминосульфокислот к слабощелочному р-ру амина, содержащему NaNO2, прибавляют соляную к-ту. Для выделения галогенидов диазония процесс ведут в абсолютном спирте или ледяной СН3СООН, используя http://www.xumuk.ru/encyklopedia/909.html водородные соли амина и в качестве диазотирующего агента – алкилнитриты. Для контроля р-ции в промышленности используют анализаторы с электро – химической индикацией избыточной HNO2. Анализатор связан с автоматическим дозиметром, регулирующим прибавление к-ты, NaNO2 и амина таким образом, чтобы не возникал избыток нитрозирующего агента. диазотирования – первая стадия синтеза азокрасителей, а также р-ций Зандмейера, Гомберга, Шимана, Гаттермана, Несмеянова, Барта, Меервейна. Диазотирование открыто П. Гриссом в 1858.
