Полимерные композиты на основе диальдегилцеллюлозы и полигуанилинметакрилата
К наиболее сильным из известных гуанидиновых антисептиков относятся «хлоргексидин» (1,6-бис-4,4-хлорфеноксибигуанидогексин) [7], низкомолекулярный полигексаметиленбигуанидин - «вантоцил» [15, 16] и «космо-цил» [17].
Так, например, хлоргексидин используется в качестве дезинфицирующего средства в виде солей (гидрохлорида, ацетата, глюконата) и широко рекомендуется за рубежом в виде растворов, мазей, присыпок как эффективное дезинфицирующее средство в хирургии для борьбы с внутрибольничными инфекциями, лечения кожных заболеваний и бытовых целей. Однако, следует отметить, что хлоргексидин, вантоцил и космоцил получают по сложной 4-х стадийной технологической схеме, кроме того при их синтезе исходным сырьем служит хлорциан, поэтому технологический процесс дорог и опасен.
В нашей стране был разработан процесс производства полимерного гуанидинового антисептика - полигексаметиленгуанидингидрохлорида (ПГМГ) («метацид», «полисепт») [18, 10], исходя из гексаметилендиамина и гидрохлорида гуанидина:
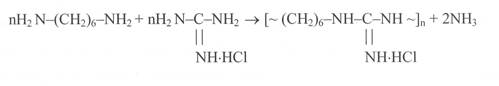
В дальнейшем было предложено объединить в одном процессе синтез гуанидингидрохлорида и получение из него ПГМГ [20].
Так как три аминогруппы гуанидингидрохлорида имеют различную реакционную способность, то молекулярную массу и структуру «полисепта» удается регулировать, изменяя условия реакции и содержание гексаметилендиамина в исходной смеси [21]. Так, при сравнительно низких температурах для процесса поликонденсации (120-130°С) в реакцию с гексаметилендиами-ном вступают преимущественно две аминогруппы гуанидингидрохлорида, образуя хорошо растворимый линейный олигомер с ММ=1,7-12,5х10 . При увеличении количества гексаметилендиамина в реакционной смеси сверх одного моля на 1 моль гуанидингидрохлорида и повышении температуры до 180-20О°С в реакцию может вступать третья аминогруппа и образуется разветвленный полимер, который имеет ММ 20-43x103.
Различные соли ПГМГ (фосфат, глюконат, дегидроцет, сорбат, фторид, сульфат, нитрат, силикат, ацетат, стеарат, олеат, фумарат, сукцинат, адипи-нат, себацинат) были получены при действии различных кислот или их солей на основание или карбонат ПГМГ [22]. Среди указанных полимерных солей наибольшее практическое значение помимо «полисепта» имеют фосфат «фо-гуцид» и глюконат. По сравнению с «полисептом», фогуцид менее токсичен и коррозионноактивен.
Поликонденсационные полимеры: «полисепт» и «фогуцид» рекомендованы Минздравом в качестве дезинфицирующего средства в лечебных учреждениях и роддомах [23], а также в ветеринарии [24].
По данным, указанным в работе [25], растворы «полисепта» в концентрации 0,1-0,05% вызывают гибель грамположительных и грамотрицатель-ных микроорганизмов: коринебактерий дифтерии (с. Duphtheretiae), золотистого стафилококка (St.aureus), а также St.aibus и St. faekalis, брюшнотифозной палочки (S.typhi), шигелл Зонне и Флекснера (Shigella Sonnae, Flexneri), кишечной палочки (E.Coli), сальмонелл Бреслау и Гертнера (Salmonella th.murum), вульгарного протея (Proteus Vulgarus), синегнойной палочки (Ps.aeruginosa) в течение 5-25 минут.
Перспективным является применение гуанидин содержащих полимеров для лечения заболеваний вирусной этиологии. Разработанные и применяемые в настоящее время противовирусные препараты проявляют свое защитное действие путем инактивации вирусов во внешней среде, предохранения восприимчивых тканей и клеток от адсорбции на них вирусных частиц, преду преждения миграции нового поколения вирусных частиц из инфицированных клеток и нарушения синтеза вирусов в восприимчивых клетках. Интерес к применению синтетических полимеров для вирусологических целей возник после того, как была установлена возможность ингибировании действия ферментов, размножения бактерий и развития опухолей под влиянием некоторых биологических и синтетических полимеров. По данным института Вирусологии им. Д.И. Ивановского АМН, защитным противовирусным эффектом обладают полимеры, содержащие гуанидиновую группировку, в частности, «полисепт» и «фогуцид». В результате проведенных исследований было установлено, что эти вещества обладают сильным вирулицидным действием по отношению к вирусам герпеса простого, вируса СПИДА, вируса гепатита А, вируса тропической лихорадки: при 15-20 мин экспозиции 2% раствора препарата с вирусосодержащими жидкостями (при комнатной температуре) инфекционный титр вирусов снижается в 1000 и более раз.
Механизм защитного противовирусного действия синтетических полимеров, возможно, связан с блокадой ими поверхностных рецепторов клеток [26].
По сравнению с другими катионными полиэлектролитами использование гуанидинсодержащих биоцидных полимеров имеет еще одно положительное преимущество.
При использовании синтетических биоцидных полимеров следует учитывать их биодеградируемость в живом организме. В случае использования небиодеградируемых синтетических полимеров существенное значение имеет их молекулярная масса, поскольку полимеры с молекулярной массой выше 50000 не могут выводиться через почки, а накапливаются в почечных канальцах, вызывая выраженные токсические эффекты. В этом отношении биоцидный эффект гуанидиновых соединений физиологичен, и в живом организме имеются ферментные системы, способные вызывать деградацию этих соединений, предотвращая их кумуляцию [28].
1.2 Биологически активные полимеры
Известно, что биологически активные полимеры должны удовлетворять ряду требований:
1) хорошо растворяться в воде и солевых растворах;
2) быть биосовместимыми, не обладать высокой токсичностью, не подавлять иммунную систему;
3) иметь небольшую скорость выведения и выводиться из организма после выполнения своей функции;
Все это накладывает определенные требования к их структуре, молекулярной массе и молекулярно - массовому распределению (ММР).
Чаще всего синтетические биологически активные полимеры представляют собой гибрид синтетического полимера-носителя с биологически активным веществом, Биологическая активность таких гибридных систем определяется в основном свойствами присоединенного к полимеру-носителю вещества.
Одним из способов получения водорастворимых биологически активных полимеров является синтез гидрофильных мономеров на основе гидрофобных биологически активных веществ (БАВ) и ионогенных ненасыщенных карбоновых кислот (акриловой, метакриловой и т.п.)
Метакриловая и акриловая кислота и их производные характеризуются значительной реакционной способностью в реакциях радикальной гомо- и сополимеризации. Производные метакриловой кислоты, содержащие химически активные функциональные группы, представляют собой перспективный ряд мономеров. Соответствующие им полимеры могут сохранять потенциал активности, являясь удобными носителями биологически активных веществ. Потребность в них применительно к самым разнообразным отраслям, начиная от техники и кончая медициной, естественно стимулирует и, несомненно, оправдывает необходимость изучения особенностей протекания процессов синтеза и механизма образования этого класса полимерных соединений [28, 29].
