Принципы определения примесей арсена в неизвестном минерале
2.2.2.2 Реактивы и приборы
Фосфат калия, однозамещенный, 2%-ный раствор. Растворяют 20 г однозамещенного фосфата калия в воде, разбавляют до 1 л и перемешивают.
Магнезиальная смесь, растворяют 55 г хлорида магния MgCl2∙6H2O и 105 г хлорида аммония NH4Cl в воде, добавляют 350 мл концентрированного раствора аммиака и разбавляют водой до 1 л. Дают раствору отстояться в течение 3 – 4 дней и фильтруют.
Стандартный раствор арсената. Навеску арсенита калия (х. ч.) 2,0853 г растворяют в 23 мл 1 н. раствора щелочи, переносят в мерную колбу емкостью 1 л, подкисляют хлористоводородной кислотой до кислой реакции, прибавляют 0,5 г хлората калия, разбавляют водой до метки и хорошо перемешивают. Такой раствор содержит 1∙10-2 моль мышьяка в 1 мл. Из этого раствора разбавлением готовят стандартные растворы с содержанием мышьяка 0, 1∙10-5, 2∙10-5, 2,5∙10-5, 3∙10-5, 3,5∙10-5 моль/л.
Хлорид олова(II), 0,5%-ный раствор в хлористоводородной кислоте, разбавленной (1 : 1).
Молибдат-гидразиновый реактив. Растворяют 1 г молибдата аммония в 100 мл 5 н. серной кислоты и 0,15 г сернокислого гидразина в 100 мл воды. Разбавляют 10 мл раствора молибдата аммония до 90 мл водой, добавляют 1 мл раствора сернокислого гидразина и водой разбавляют до 100 мл. Эта смесь неустойчива, и поэтому ее готовят ежедневно или в ходе анализа отдельно прибавляют соответствующее количество растворов молибдата аммония и сернокислого гидразина.
Прибор для отгонки хлорида мышьяка(III) (показан на рис. 2.2), спектрофотометр КФК-3, кюветы на 1см, набор колб и пипеток.
2.2.2.3 Ход анализа
Навеску 1 г растертого в агатовой ступке металла (или 0,2 – 0,5 г при содержании мышьяка выше 0,0005%) помещают в стакан емкостью 100 мл, добавляют 5 мл азотной кислоты (пл. 1,4), накрывают стеклом и нагревают на плитке, осторожно покачивая стакан, избегая бурного кипения и излишнего испарения кислоты. Нагревают до превращения металла в белую массу. Охлаждают, снимают стекло, дают улетучиться окислам азота, насыпают 6 г тартрата аммония (при навеске 0,5 г сурьмы достаточно 5 г тартрата), приливают воды до 80 мл и нагревают при помешивании до растворения сурьмяной кислоты. Раствор переливают в стакан емкостью 300 мл и разбавляют водой до 150 мл. Охлаждают, добавляют 10 мл раствора однозамещенного фосфата калия, 10 мл магнезиальной смеси и при помешивании – раствор аммиака до слабого запаха и начала образования осадка. Затем приливают еще 10 мл раствора аммиака, перемешивают и оставляют на 7 – 12 ч. Осадок отфильтровывают через бумажный фильтр (7 см) и 15 – 16 раз промывают малыми порциями 1%-ного раствора аммиака. Осадок на фильтре и стенках стакана растворяют в горячей серной кислоте, разбавленной (1: 10), собирая раствор в колбу прибора для отгонки хлорида мышьяка(III) (рис.2.2), прибавляют 0,3 г сернокислого гидразина (если необходимо, берут больше) и 10 мл концентрированной хлористоводородной кислоты.
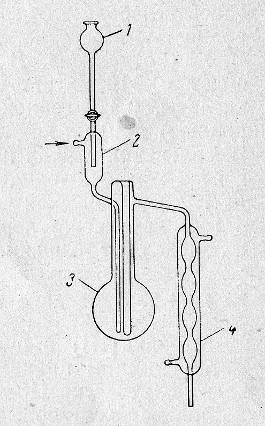
Рисунок 2.2 Прибор для отгонки хлорида мышьяка(III): 1 – капельная воронка; 2 – предохранительная склянка; 3 – реакционная колба; 4 – холодильник.
В маленький стакан наливают 10 мл холодной воды и погружают в него конец холодильника. Раствор в колбе медленно нагревают до 107 °С [7]. Собирают 100 – 110 мл отгона и определяют мышьяк с помощью спектрофотометра КФК-3.
2.3 Анализ полученных результатов
Расшифровка результатов предварительных испытаний и качественного анализа:
Таблица 1 Предварительное испытание вещества нагреванием в тугоплавкой пробирке
|
Видимые изменения |
Причини |
Возможный состав |
|
Вещество частично улетучивается. При этом есть возгон белого цвета |
NH4Г HgCl2, HgBr2 As2O3, As2O5 |
Галогениды аммония Соединения ртути Окислы мышьяка |
Таблица 2 Предварительное испытание вещества с перлом буры
|
Цвет перла |
Элементы, вызывающие окраску при перлах из Na2B4O7 | |||
|
в окислительном пламени |
в восстановительном пламени | |||
|
в горячем состоянии |
в холодном состоянии |
в горячем состоянии |
в холодном состоянии | |
|
Бесцветный |
Pb, Bi, Sb, Cd |
Pb, Bi, Sb, Cd, Fe |
Mn, Cu |
Mn, Cu |
|
Серый |
Ag, Pb, Bi, Sb, Cd, Zn, Ni |
Ag, Pb, Bi, Sb, Cd, Zn, Ni | ||
Таблица 3 Предварительное испытание вещества действием кислоты
|
Кислота |
Видимые изменения |
Причини |
Возможный состав |
|
3 М H2SO4 на холоду Последующее кипячение с 3 М H2SO4 |
Выделяется газ с запахом тухлых яиц |
H2S |
Сульфиды |
|
Отличий не зафиксировано | |||
|
Последующее кипячение с 18 М H2SO4 |
Выделяется бесцветный газ: с резким запахом, дымит на воздухе |
HCl |
Хлориди |
Таблиця 4 Перевод вещества в раствор
|
№ опыта |
Растворитель |
Видимые изменения растворения | |
|
на холоду |
при нагревании | ||
|
1 |
H2O |
– |
– |
|
2 |
3 М HCl |
– |
– |
|
3 |
12 М HCl |
– |
частично (остался белый с желтым оттенком осадок) |
|
4 |
3 М HNO3 |
– |
– |
|
5 |
15 М HNO3 |
– |
частично (остался белый с желтым оттенком осадок) |
|
6 |
3 HCl: 1 HNO3 |
– |
частично (остался белый с желтым оттенком осадок) |
