Процессы адгезии и когезии
![]() Al(OH)3 . . Al(OH)2Cl . Al(OH)2+ Cl-
Al(OH)3 . . Al(OH)2Cl . Al(OH)2+ Cl-
Al(OH)3 . +HCl . Al(OH)2Cl . Al(OH)2+ Cl-
![]()
![]() Al(OH)3 . . Al(OH)2Cl . Al(OH)2+ Cl-
Al(OH)3 . . Al(OH)2Cl . Al(OH)2+ Cl-
Al(OH)3 . . Al(OH)2Cl . Al(OH)2+ Cl-
Al(OH)3 . . Al(OH)2Cl . Al(OH)2+ Cl-

В пределах двойного электрического слоя (ДЭС) действует электрическое поле, интенсивность которого характеризуется значением потенциала. На рис. 2.5.1.1 показано изменение потенциала двойного электрического слоя (ДЭС) на кристалле AgCl с увеличением расстояния от поверхности. Потенциал на поверхности частицы называется термодинамическим потенциалом. Он характеризует скачок потенциала на границе раздела между фазами. Ионы в слое противоионов (плотного слоя) приближаются к поверхности на расстояние, определяемое собственными размерами. Воображаемая поверхность, проведенная через их центры, называется плоскостью максимального приближения и расположена на расстоянии порядка молекулярных размеров, а потенциал плоскости равен . Смещение фаз в дисперсной системе относительно друг друга вызванное внешними силами (электрическое поле) происходит по поверхности скольжения, которая не всегда совпадает с плоскостью максимального приближения и обычно расположена на бόльшем расстоянии от поверхности. Потенциал на поверхности скольжения называется электрокинетическим потенциалом или zпотенциалом. Его можно рассчитать из электрокинетических экспериментов. Его значение зависит от числа не скомпенсированных на поверхности скольжения зарядов адсорбционного слоя, т.е. числа ионов в диффузионном слое. Падение потенциалов в плотной части двойного электрического слоя (ДЭС) имеет линейный характер. В диффузной части двойного электрического слоя (ДЭС) для слабо заряженных поверхностей изменение потенциалов с расстоянием подчиняется экспоненциальной зависимости
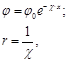
где j0- потенциал поверхности;
c- параметр Дебая;
r - характеристическая величина атмосферы, расстояние, на котором действуют адсорбционные силы;
х - расстояние от поверхности, толщина двойного электрического слоя (ДЭС).
![]() ,
,
где z – заряд.
Существует несколько правил для составления мицелл:
1. Основа мицеллы – агрегат, нерастворимый в данной дисперсионной среде, состоящий из множества (m) молекул (атомов) простого вещества (осадка).
![]()
![]() mAg3AsO3 × nAsO33- × 3(n-x)Na+ -3x×3xNa+
mAg3AsO3 × nAsO33- × 3(n-x)Na+ -3x×3xNa+
Агрегат Потенциал- Противо- Ионы
определяю- ионы диффузионного
![]() щие ионы адсорбции- слоя
щие ионы адсорбции- слоя
онного слоя
![]()
![]() Ядро мицеллы
Ядро мицеллы
Адсорбционный слой Диффузион-
![]() ный слой
ный слой
Коллоидная частица
Здесь m, n, x – натуральные числа;
m – число молекул в агрегате;
n – число потенциалопределяющих ионов;
(n – x) – число противоионов адсорбционного слоя;
x – число противоионов диффузного слоя.
Численный коэффициент 3 перед (n – x) и х поставлен ввиду трехос-новности аниона AsO33-.
2. Согласно правилу Пескова-Фаянса-Панета, на поверхности агрегата адсорбируются ионы электролита-стабилизатора, входящие в состав агрегата, либо имеющие общую природу с ним, либо специфически взаимодействующие с ним и находящиеся в избытке. Ионы, сообщающие агрегату поверхностный заряд, называются потенциалопределяющими. Агрегат + потенциалопределяющие ионы = ядро мицеллы.
3. Заряд ядра компенсируется эквивалентным количеством противоположно заряженных ионов электролита-стабилизатора – противоионов. Часть противоионов, прочно связанных с ядром, входит в адсорбционный слой. Агрегат + адсорбционный слой = коллоидная частица (имеет заряд).
4. Остальная часть противоионов образует диффузионный слой.
5. Суммы электрических зарядов коллоидной частицы и диффузионного слоя равны друг другу по абсолютной величине и противоположны по знаку.
6. Электрический заряд коллоидной частицы равен алгебраической сумме электрических зарядов потенциалопределяющих ионов и противоионов адсорбционного слоя.
7. Мицелла гидрофобного золя является электронейтральной, т.е. алгебраическая сумма электрических зарядов ионов всех слоев равна нулю
Для любого типа реакции одно из исходных веществ берут в избытке по сравнению со стехиометрически необходимым соотношением:
Na3AsO3 + 3AgNO3 → ↓Ag3AsO3 + 3NaNO3
избыток осадок
Электролитическая диссоциация электролита, взятого в избытке:
Na3AsO3 « 3Na+ + AsO33-
Заряд коллоидной частицы определяется так (правило 6):
n(-3) + 3(n – x)(+1) = -3x
Для проверки правильности записи формулы мицеллы подсчитывают алгебраическую сумму зарядов всех ионов (правило 7):
n(-3) + 3(n – x)(+1) + 3х(+1) = 0
Коллоидная частица имеет отрицательный заряд, мицелла в целом электронейтральна.
