Роль свободных радикалов в природной среде
ОГЛАВЛЕНИЕ
ВВЕДЕНИЕ
1. ОБЩАЯ ХАРАКТЕРИСТИКА И НОМЕНКЛАТУРА СВОБОДНЫХ РАДИКАЛОВ
1.1 Что такое свободные радикалы
1.2 Номенклатура радикалов
1.3 Классификация радикалов
1.3.1 Первичные радикалы и реактивные молекулы
1.3.2 Вторичные и третичные радикалы
2. РЕАКЦИИ С УЧАСТИЕМ СВОБОДНЫХ РАДИКАЛОВ В РЕЧНЫХ СИСТЕМАХ
2.1 Наблюдения и эксперименты
2.2 Результаты исследования
2.3 Анализ результатов
3. СВОБОДНОРАДИКАЛЬНЫЕ РЕАКЦИИ В АТМОСФЕРЕ
3.1 Реакции в стратосфере
3.2 Химические процессы в тропосфере
3.2.1 Роль углеводородов в тропосферных фотохимических процессах
4. СВОБОДНОРАДИКАЛЬНЫЕ РЕАКЦИИ В БИОЛОГИЧЕСКИХ СИСТЕМАХ
ЗАКЛЮЧЕНИЕ
СПИСОК ЛИТЕРАТУРЫ
ВВЕДЕНИЕ
Вся природа, окружающая нас, состоит из химических веществ и их соединений различной структуры. Их все можно разделить на различные группы по самым разнообразным признакам: состав, строение, роль в биологических системах и так далее. В своей работе я рассматриваю такую группу веществ, как свободные радикалы. Мой интерес вызван их широчайшей дифференциацией и повсеместным нахождением во всех компонентах биосферы.
Высокая реакционная способность свободных радикалов обуславливает большое количество химических реакций, которые происходят с различными элементами окружающей среды. Все они играют определенную роль в природных процессах.
В этой работе рассматриваются химические реакции с участием свободных радикалов и их участие в антропогенных и биологических циклах отдельные компонентов окружающей среды.
1. ОБЩАЯ ХАРАКТЕРИСТИКА И НОМЕНКЛАТУРА СВОБОДНЫХ РАДИКАЛОВ
1.1 Что такое свободные радикалы
Хорошо известно, что в органических молекулах (включая те, из которых состоит наш организм) электроны на внешней электронной оболочке располагаются парами: одна пара на каждой орбитали (рис. 1)
Свободные радикалы отличаются от обычных молекул тем, что у них на внешней электронной оболочке имеется неспаренный (одиночный) электрон (рис. 2 и 3).
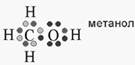
Рисунок 1.1. Электронная структура молекулы метанол
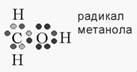
Рисунок 1.2. Электронная структура радикала метанола
Неспаренный электрон в радикалах принято обозначать точкой. Например, радикал гидроксила обозначают как HO·, радикал перекиси водорода как HOO·, радикал супероксида как ·OO- или O2·-. Ниже даны формулы трех радикалов этилового спирта: CH3CH2O·; CH3·CHOH; CH3CH2O·
Итак:
· Свободным радикалом называется частица - атом или молекула, имеющая на внешней оболочке один или несколько неспаренных электронов.
· Это делает радикалы химически активными, поскольку радикал стремится либо вернуть себе недостающий электрон, отняв его от окружающих молекул, либо избавиться от "лишнего" электрона, отдавая его другим молекулам.
· В особом положении оказалась молекула кислорода (диоксигена), которая содержит на внешней оболочке целых два неспаренных электрона. Таким образом, диоксиген - это бирадикал и, подобно другим радикалам, обладает высокой реакционной способностью.

Рисунок 1.3. Электронная структура некоторых молекул и радикалов
Важно подчеркнуть, что неспаренные электроны должны находиться на внешней оболочке атома или молекулы. В понятие свободного радикала не включаются ионы металлов переменной валентности, неспаренные электроны в которых находятся на внутренних оболочках. Поскольку и радикалы и ионы таких металлов как железо, медь или марганец (так же как комплексы этих металлов) дают сигналы электронного парамагнитного резонанса (ЭПР), эти частицы в совокаупности часто называют парамагнитными центрами.
Образование радикалов из устойчивых молекул обусловлено, таким образом, появлением на свободной, валентной орбитали нового электрона или наоборот - удалением одного электрона из электронной пары. Эти процессы обычно происходят в результате реакций одноэлектронного окисления или восстановления. В таких реакциях обычно участвует, наряду с молекулой, из которой радиукал образуется, ион металла переменной валентности, который ка раз и служит донором или акцептором одного электрона (а не двух сразу, как это бывает в реакиях между двумя органическими молекулами или между органической молекулой и кислородом). Типичный пример реакции, в которой образуется радикал - это реакция Фентон: взаимодействие пероксида водорода с ионом двухвалентного железа:
Fe2+ + H2O2 => Fe3+ + OH- + ·OH (радикал гидроксила)
При высоких температурах или под действием ультрафиолетового излучения радикалы могут образовываться также в результате разрыва химической связи (гомолитическое расщепление). В обычных условиях такие реакции в нормальных живых клетках практически не имеют места.
1.2 Номенклатура радикалов
Относительно недавно Комиссия по Номенклатуре Неорганической химии сформулировала основные правила номенклатуры радикалов [1] (табл. 1).
Таблица 1. Названия некоторых радикалов и молекул согласно рекомендациям Комиссии по Номенклатуре Неорганической Химии (1990).
|
Формула |
Структурная формула |
Название радикала |
|
O·- |
·O- |
Оксид (1-), [оксид] |
|
О2 |
·ОО· |
[Диоксиген] |
|
О2·- |
·ОО- |
Диоксид (1-), супероксид, [диоксид] |
|
O3 |
|
Триоксиген, [озон] |
|
°O3·- |
·OOO- |
Триоксид (1-), озонид |
|
HO· |
HO· или ·OH |
[Гидроксил] |
|
HO2· |
HOO· |
Гидродиоксид, [гидродиоксил] |
|
Н202 |
HOOH |
[Перекись водорода] |
|
RO· |
RO· |
[Алкоксил] |
|
C2H5O· |
CH3CH2O· |
[Этоксил] |
|
R02· |
ROO· |
[Алкилдиоксил] |
|
RO2H |
ROOH |
[Апкилгидропероксид] |
