Технология получения и свойства мочевино-формальдегидных смол
СН2О + Н2О ![]() HOCH2OH
HOCH2OH
Этот вывод основан на том, что водные растворы формальдегида кипят при 100 °С, и что дистиллат при перегонке содержит формальдегида меньше, чем кубовый остаток. Если бы растворенный формальдегид не был в виде гидрата, он должен был бы отгоняться даже при слабом нагревании.
Формальдегид в водных растворах любой концентрации склонен к уплотнению с образованием полиоксиметиленгликолей.При этом происходят следующие реакции:
1) Образование димера:
НОСН2ОН + НОСН2ОН ![]() HOCH2OCH2OH + Н2О
HOCH2OCH2OH + Н2О
2) Удлинение цепи:
НОСН2ОСН2ОН + nНОСН2ОН ![]() HO(CH
HO(CH![]() O)n+1CH
O)n+1CH![]() OH + nH2O,
OH + nH2O,
где n = 3 - 4.
Таким образом, водные растворы формальдегида, называемые формалином, всегда содержат растворимые полиоксиметиленгликоли.
Формалин всегда содержит немного муравьиной кислоты, количество которой увеличивается при длительном хранении вследствие окисления формальдегида:
2СН2О + О2 ![]() 2НСООН
2НСООН
Из других свойств этого простейшего альдегида отмечаются те, которые необходимы для понимания закономерностей образования смол:
1) одновременное самоокисление и самовосстановление альдегидной группы в присутствии водного раствора щелочи, сопровождающееся образованием метилового спирта и муравьиной кислоты;
2) образование ацеталей при нагревании формальдегида сo спиртами (например, бутиловым):
СН2О + 2С4Н9ОН ![]() С4Н9ОCН2ОC4Н9 + Н2О;
С4Н9ОCН2ОC4Н9 + Н2О;
3) образование гексаметилентетрамина (уротропина) при действии аммиака на формальдегид:
6CH2O + 4NH3 ![]() (CH2)6N4 + 6H2O;
(CH2)6N4 + 6H2O;
Основным промышленным способом получения формальдегида является окисление метилового спирта кислородом воздуха при400—600 °С в присутствии катализатора. Одновременно протекают две реакции — окисление и дегидрирование:
СН3ОН + ![]() О2
О2 ![]() СН2О + Н2О + 36,8 ккал/моль;
СН2О + Н2О + 36,8 ккал/моль;
СН3ОН ![]() СН2О + Н2 - 28,8 ккал/моль;
СН2О + Н2 - 28,8 ккал/моль;
Катализаторами процесса служат серебро, медь, окись молибдена (промотированная железом), фосфат марганца (промотированный молибденом) и др.
В последние годы формальдегид получают также окислением метана кислородом воздуха в присутствии окислов азота при 400—600 °С. Окисление протекает по схеме:
CН4 + O2 ![]() CH2O + H2O (основная реакция)
CH2O + H2O (основная реакция)
2СН4 + О2![]() 2СН3ОН (побочная реакция)
2СН3ОН (побочная реакция)
Разработаны способы получения формальдегида в смеси с другими продуктами реакции окислением кислородом воздуха некоторых углеводородов (пропана, н-бутана, изобутана при 400-500 °С).
2 Получение МФС
Механизм образования мочевино-формальдегидных смол детально не выяснен. Однако установлено, что при поликонденсации мочевины с формальдегидом в водном растворе в зависимости от рН среды, соотношения исходных компонентов, продолжительности реакции и температуры могут быть получены различные продукты. Так, в щелочной среде (рН 11–13) даже в разбавленных растворах образуется монометилолмочевина H2N-CO-NH-CH2-OH; в нейтральных и слабощелочных средах (рН 7–8) в зависимости от соотношения исходных компонентов – моно- и диметилолмочевины OC(NHCH2OH)2. Последняя образуется также при взаимодействии монометилолмочевины с формальдегидом. Положение равновесия этих реакций не зависит от рН среды, а определяется концентрацией реагирующих веществ и температурой.
При взаимодействии мочевины с формальдегидом в сильнокислой среде (рН<3) образующиеся метилолмочевины сразу же подвергаются дегидратации, давая метиленмочевины, например,
![]()
которые в условиях реакции быстро превращаются в полиметиленмочевины общей формулы (С2Н4N2O)n - неплавкие и нерастворимые аморфные продукты, не имеющие практического значения. Поэтому для получения мочевино-формальдегидных смол процесс следует проводить в условиях, способствующих образованию метилольных производных мочевины.
Моно- и диметилолмочевины – белые кристаллические продукты, растворимые в воде и метаноле; первый плавится при 111 °С (из этанола), второй – при 121 – 126 °С (из 80%-ного этанола); диметилолмочевина при нагревании растворяется также в этаноле. При нагревании безводные моно- и диметилолмочевины превращаются в полиметиленмочевины; первая полностью переходит в нерастворимый продукт при 100 °С, вторая – выше 140 °С. В водных кислых растворах (рН 4.5–6.0) метилолмочевина способна к дальнейшим превращениям с образованием, вероятно, метилен-бис-амида (I), метилолметилен-бис-амида (II) или простого эфира (III) и азометилена (IV), который сразу же тримеризуется:
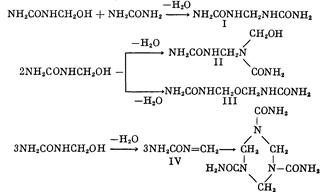
В аналогичных условиях скорость гомополиконденсации диметилолмочевины очень низка. Она также взаимодействует с мочевиной и монометилолмочевиной.
Предполагается, что основная реакция, приводящая к мочевино-формальдегидным смолам, – бимолекулярная, и скорость её пропорциональна концентрации водородных ионов. Далее приведены вероятные схемы образования мочевино-формальдегидных смол.
По-видимому, наиболее вероятна последняя схема, предусматривающая наличие в структуре полимера кислородных мостиков, присутствием которых можно объяснить выделение формальдегида при хранении и эксплуатации изделий из мочевино-формальдегидных смол.
Направление реакции мочевины с формальдегидом зависит также от температуры. Повышение её выше 40![]() (оптимальная температура для получения метилол-мочевины) способствует образованию нежелательных продуктов – метиленмочевин. Вероятность получения последних существует и в том случае, когда процесс начинают в условиях, благоприятных для синтеза метилолмочевин; это связано с изменением рН среды в ходе реакции. Так, мочевина, способная образовывать с кислотами нестойкие соли, связывает муравьиную кислоту, всегда содержащуюся в формалине. В результате этого при добавлении мочевины в раствор формалина рН реакционной смеси повышается. Однако по мере расходования мочевины кислота высвобождается и рН понижается. Кроме того, в условиях реакции муравьиная кислота образуется из формальдегида (реакция Канниццаро – Тищенко):
(оптимальная температура для получения метилол-мочевины) способствует образованию нежелательных продуктов – метиленмочевин. Вероятность получения последних существует и в том случае, когда процесс начинают в условиях, благоприятных для синтеза метилолмочевин; это связано с изменением рН среды в ходе реакции. Так, мочевина, способная образовывать с кислотами нестойкие соли, связывает муравьиную кислоту, всегда содержащуюся в формалине. В результате этого при добавлении мочевины в раствор формалина рН реакционной смеси повышается. Однако по мере расходования мочевины кислота высвобождается и рН понижается. Кроме того, в условиях реакции муравьиная кислота образуется из формальдегида (реакция Канниццаро – Тищенко):
