Химические процессы в биологическом организме
Относительное содержание a -спиральных участков и b-структур может широко варьироваться в разных белках. Существуют белки с преобладанием a-спиралей (около 75% аминокислот в миоглобине и гемоглобине), а основным типом укладки цепи во многих фибриллярных белках (в том числе фиброин шелка, b-кератин) является b-структура. Участки полипептидной цепи, которые нельзя отнести ни к одной из вышеописанных конформаций, называют соединительными петлями. Их структура определяется главным образом взаимодействиями между боковыми цепями аминокислот, и в молекуле любого белка она укладывается строго определенным образом.
Третичной структурой называют пространственное строение глобулярных белков. Но часто это понятие относят к характерному для каждого конкретного белка способу сворачивания полипептидной цепи в пространстве. Третичная структура формируется полипептидной цепью белка самопроизвольно, по-видимому, по определенному пути (путям) свертывания с предварительным образованием элементов вторичной структуры. Если стабильность вторичной структуры обусловлена водородными связями, то третичная структура фиксируется разнообразной системой нековалентных взаимодействий: водородными, ионными, межмолекулярными взаимодействиями, а также гидрофобными контактами между боковыми цепями неполярных аминокислотных остатков. В некоторых белках третичная структура дополнительно стабилизируется за счет образования дисульфидных связей (—S—S связей) между остатками цистеина. Как правило, внутри белковой глобулы расположены боковые цепи гидрофобных аминокислот, собранные в ядро (их перенос внутрь глобулы белка выгоден термодинамически), а на периферии находятся гидрофильные остатки и часть гидрофобных. Белковую глобулу окружает несколько сотен молекул гидратной воды, необходимой для стабильности молекулы белка и нередко участвующей в его функционировании. Третичная структура подвижна, отдельные ее участки могут смещаться, что приводит к конформационным переходам, которые играют значительную роль во взаимодействии белка с другими молекулами. Третичная структура является основой функциональных свойств белка. Она определяет образование в белке ансамблей функциональных групп — активных центров и зон связывания, придает им необходимую геометрию, позволяет создать внутреннюю среду, являющуюся предпосылкой протекания многих реакций, обеспечивает взаимодействие с другими белками.
Третичная структура белков однозначно соответствует его первичной структуре; вероятно, существует еще нерасшифрованный стереохимический код, определяющий характер свертывания белка. Однако один и тот же способ укладки в пространстве обычно соответствует не единственной первичной структуре, а целому семейству структур, в которых совпадать может лишь небольшая доля (до 20-30%) аминокислотных остатков, но при этом в определенных местах цепи сходство аминокислотных остатков сохраняется. Результатом является образование обширных семейств белков, характеризующихся близкой третичной и более или менее сходной первичной структурой и, как правило, общностью функции. Таковы, например, белки организмов разных видов, несущие одинаковую функцию и эволюционно родственные: миоглобины и гемоглобины, трипсин, химотрипсин, эластаза и другие протеиназы животных.
Нередко, особенно в крупных белках, сворачивание полипептидной цепи проходит через формирование отдельными участками цепи более или менее автономных элементов пространственной структуры — доменов, которые могут обладать функциональной автономией, будучи ответственными за ту или иную биологическую активность белка. Так, N-концевые домены белков системы свертывания крови обеспечивают их присоединение к клеточной мембране.
Существует много белков, молекулы которых представляют собой ансамбль из глобул (субъединиц), удерживаемых вместе за счет гидрофобных взаимодействий, водородных или ионных связей. Такие комплексы называют олигомерными, мультимерными или субъединичными белками. Укладку субъединиц в функционально активном белковом комплексе называют четвертичной структурой белка. Некоторые белки способны образовывать структуры более высоких порядков, например, полиферментные комплексы, протяженные структуры (белки оболочек бактериофагов), надмолекулярные комплексы, функционирующие как единое целое (например, рибосомы или компоненты дыхательной цепи митохондрий). Четвертичная структура позволяет создать молекулы необычной геометрии. Так, у ферритина, образованного 24 субъединицами, имеется внутренняя полость, благодаря которой белку удается связать до 3000 ионов железа. Кроме того, четвертичная структура позволяет в одной молекуле выполнять несколько различных функций. В триптофансинтетазе совмещены ферменты, ответственные за несколько последовательных стадий синтеза аминокислоты триптофана.
3. Покажите специфику строения и состава структурных белков биологической мембраны
Первичная структура белков определяет все остальные уровни организации белковой молекулы. Поэтому при изучении биологической функции различных белков важно знание этой структуры. Первым белком, для которого была установлена аминокислотная последовательность, был гормон поджелудочной железы — инсулин. Эта работа, потребовавшая 11 лет, была выполнена английским биохимиком Ф. Сенгером (1954). Он определил расположение 51 аминокислоты в молекуле гормона и показал, что она состоит из 2-х цепей, соединенных дисульфидными связями. Позже большая часть работ по установлению первичной структуры белков была автоматизирована. С развитием методов генетической инженерии появилась возможность еще более ускорить этот процесс, определяя первичную структуру белков в соответствии с результатами анализа нуклеотидной последовательности в генах, кодирующих эти белки. Вторичную и третичную структуру белков исследуют с помощью достаточно сложных физических методов, например, кругового дихроизма или рентгеноструктурного анализа белковых кристаллов. Третичная структура была впервые установлена английским биохимиком Дж. К. Кендрю (1957) для белка мышц — миоглобина.
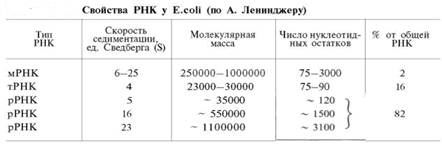
4. Дайте сравнительную характеристику всех видов РНК. Оформите ответ в виде таблицы, указав молярную массу, минорные основания, углеводы, структуру, место локализации, функции
синтез белок аминокислота
О количестве РНК нет точных данных, поскольку содержание ее в разных клетках в значительной степени определяется интенсивностью синтеза белка. На долю РНК приходится около 5–10% от общей массы клетки. Современная классификация различных типов клеточной РНК основывается на данных топографии, функции и молекулярной массы. Выделяют три главных вида РНК: матричную (информационную) – мРНК, которая составляет 2–3% от всей клеточной РНК; рибосомную – рРНК, составляющую 80–85% и транспортную – тРНК, которой около 16%. Эти 3 вида различаются нуклеотидным составом и функциями (табл. 1).
Таблица 1.
5. Фермент лактатдегидрогенеза окисляет молочную кислоту в пировиноградную. Покажите с помощью уравнения данной реакции механизм действия кофермента НАД
