Изоморфизм уравнений диссипативных свойств растворов электролитов
![]() (25)
(25)
теоретически радиусы иона и сольватированного иона можно оценить по формулам [1-6]:
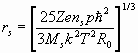 , (26) где
, (26) где
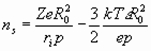 , (27) где
, (27) где
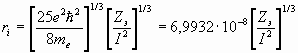 (28)
(28)
rs – радиус сольватированного иона,
ns – число молекул растворителя окружающих ион,
ri – радиус иона,
Zэ – экранированный заряд ядра,
Z – заряд иона,
I – энергия ионизации,
R0 – радиус молекулы растворителя,
р – дипольный момент молекулы растворителя,
- диэлектрическая проницаемость среды,
Мs – молекулярная масса растворителя.
Zэ – экранированный заряд ядра находится используя константы экранирования Слейтера определяемые по стандартным правилам приводимым в различных учебниках по теоретической основе неорганической химии, в частности [9].
Таблица 1
Радиусы ионов, сольватные числа и радиусы сольватированных ионов рассчитанные по уравнениям 26 – 28
|
Ион |
I, эв |
Zэ |
|
ns |
|
|
Li+ |
75,62 |
2,7 |
0,5446 |
7,3873 |
4,4246 |
|
Na+ |
47,29 |
6,55 |
1,0004 |
3,2301 |
3,3583 |
|
K+ |
31,81 |
7,75 |
1,3785 |
1,8682 |
2,7980 |
|
Cl- |
3,82 |
4,875 |
1,8100 |
1,0090 |
2,2786 |
Таблица 2
Приведенные радиусы молекул рассчитанные по формуле 25
|
Молекула |
|
|
LiCl |
1,5040 |
|
NaCl |
1,3575 |
|
KCl |
1,2559 |
Выражая из уравнения (17) вязкость и коэффициент диффузии через электропроводность (Т = 298К), получим отдельно для каждого i-го иона:
![]() (29)
(29)
![]() (30)
(30)
Переходя к вязкости и диффузии, как свойствам раствора, необходимо учитывать взаимную корреляцию движения ионов противоположного знака, поэтому вязкости и коэффициенты диффузии отдельных ионов одной молекулы, объединяем в приведенное значение.
Например, для 1-1 электролита
![]() (31)
(31)
![]() (32)
(32)
Соответственно при бесконечном разбавлении
![]() (33)
(33)
![]() (34)
(34)
Неренст и Хартли для определения коэффициента диффузии одного единственного электролита предложили уравнение (23)
![]() (35)
(35)
где D0 – предельное значение коэффициента диффузии по Нернсту (33)
Сравнивая теоретические уравнения электропроводности (1) и диффузии по Неренсту – Хартли (35), учтя в последнем максвеловское распределение по скоростям и параметр экранирования, можно показать, что
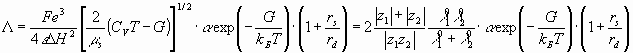 (36, 37)
(36, 37)
Электропроводности экспериментально найденные, и рассчитанные по уравнениям (36, 37), приведены в таб. 4.3 – 4.5.
Из полученных данных можно сделать вывод, что электропроводность найденная по уравнению (36) хорошо согласуется с экспериментально найденной в случаях хлоридов натрия и калия, хуже для хлорида лития, но электропроводность рассчитанная по уравнению (37) для хлорида лития практически совпадает с данными полученными по уравнению (36), в остальных случаях уравнение (37) дает небольшое расхождение с опытом.
Роль среднего значения кинетической энергии ионов в уравнении (1), которая, согласно теореме вариала, равна по модулю среднему значению полной энергии, играет функция 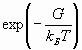 , причем
, причем 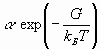 - есть максвелловское распределение по скоростям.
- есть максвелловское распределение по скоростям.
В уравнении (35) выражение ![]() равно
равно ![]() , а это есть –полная энергия молекулы при данной концентрации.
, а это есть –полная энергия молекулы при данной концентрации.
Роль распределения для коэффициента диффузии играет функция ![]() , которую, если учесть при средне молярном коэффициенте активности, можно представить в виде
, которую, если учесть при средне молярном коэффициенте активности, можно представить в виде 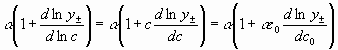 .
.
Применив поправку 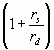 , окончательно получим
, окончательно получим
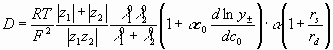 (38)
(38)
С другой стороны, учитывая уравнение (37) получим:
![]() (39)
(39)
Здесь - электропроводность экспериментальная, либо рассчитанная по уравнениям (36, 37). Нернст и Хартли получили уравнение (39) без учета вероятностного распределения, поэтому должно быть
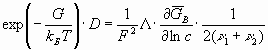
или
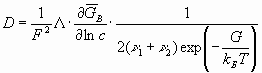 (40)
(40)
Используя уравнение Стокса – Эйнштейна (16)
![]()
выразим вязкость, через коэффициент диффузии найденный по уравнению (38) получим
![]() (41)
(41)
или по (40)
![]() (41а)
(41а)
Так же вязкость можно определить через подвижность найденную по уравнению (21)
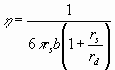 (42)
(42)
Используя значения эквивалентных электропроводностей (рис. 4.1), данные таблицы 2, уравнений 30, 35, 38, 40 и уравнений 29, 41, 41а, 42, где вместо i также табличное значение электропроводностей, были подсчитаны значения вязкости и коэффициента диффузии выбранных солей см. таб. 4 – 12.
