Структура и свойства мембранных липидов
Кроме метода дифракции рентгеновских лучей для характеристики свойств липидных фаз использовали и другие методы. Один из них, оказавшийся особенно полезным, — это электронная микроскопия замороженных сколов. Второй метод, 31Р-ЯМР, был введен в исследовательскую практику несколько позже и нашел применение для обнаружения небислойных структур, которые, как полагают, играют особую роль в биологических мембранах.
1. Электронная микроскопия липидных фаз с применением метода замораживания—травления. Этот метод оказался очень полезным при изучении структурной организации различных липидных фаз. Примеры получаемых при этом электронных микрофотографий приведены на рис. 2.7. Жидкокристаллическая фаза на этих микрофотографиях всегда выглядит как гладкая поверхность, а Р^.-фаза — как рифленая. Геле-вая фаза выглядит как гладкая поверхность, но при определенных условиях приготовления препарата имеет спиральную текстуру из-за возникновения случайных дефектов в плотной упаковке. Гексагональная фаза, образуемая такими лип идами, как ненасыщенный фосфатидилхолин, выяляется на микрофотографиях после замораживания—травления как стопка цилиндров. При приготовлении образцов липиды уравновешивают в условиях, подходящих для формирования нужных структур, а затем быстро замораживают, чтобы организация этих структур не успела измениться.
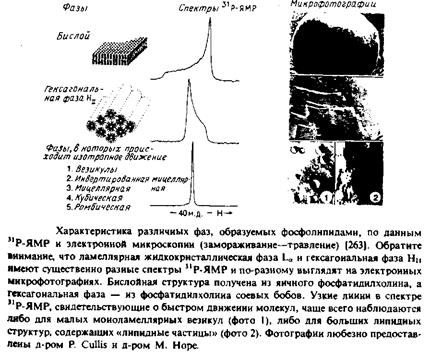

Электронно-микроскопические методы использовались также для изучения «липидных частиц». Эти частицы нередко наблюдаются в бинарных смесях, если один из липидов склонен образовывать фазу Ни, а другой — бислойные структуры. Липидные частицы образуются в чисто липидных образцах и потому отличаются от «белковых частиц», которые наблюдаются в биологических мембранах и в реконструированных белково-липид-ных системах. Было высказано предположение, что липидные частицы представляют собой вывернутые мицеллы, расположенные внутри бислоя, и что они играют определенную роль в биологических процессах, облегчая слияние мембран или стабилизируя их на сильно искривленных участках, как, например, в мем^ бране тилакоидов. Однако четких доказательств биологической роли липидных частиц пока не получено.
2. Исследование бислоев методом пР-ЯМР. Этот метод также используется для структурной характеристики гидратирован-ных липидов. Например, фосфолипиды в гексагональной фазе Ни дают спектры 31Р-ЯМР, резко отличающиеся от спектров фосфолипидов в ламеллярной фазе. С помощью этого метода исследовался переход ламеллярной фазы в гексагональную в липидах и липидных смесях. Недостатком метода является некоторая неопределенность при интерпретации спектров в случае изотропного усреднения за счет относительно быстрых движений. Полагают, что такой спектр отвечает структурам типа «липидных частиц», однако это объяснение не является единственно возможным. Как было показано, метод 31Р-ЯМР позволяет надежно установить наличие гексагональной Ни-фазы в чисто липидных дисперсиях, но в случае биологических мембран к подобным выводам следует относиться с осторожностью, особенно если они не подтверждены другими методами.
Метод 31Р-ЯМР оказался весьма полезным при определении ориентации и динамического поведения полярных головок фосфолипидов, а также структурных возмущений, вносимых в бислой мембранными белками.
2.4. ОРИЕНТАЦИЯ ПОЛЯРНЫХ ГОЛОВОК ЛИПИДОВ В БИСЛОЕ
Данные ряда методов свидетельствуют о том, что в ламелляр-ных водно-фосфолипидных дисперсиях, как и в липидных кристаллах, полярные головки липидов в целом ориентированы параллельно плоскости бислоя. В случае фосфатидилхолинов такая ориентация присуща как гелевой, так и жидкокристаллической фазам, судя по результатам исследований методами дифракции нейтронов и рентгеновских лучей. Об этом же свидетельствуют и данные, полученные методом 2Н-ЯМР, хотя при этом не исключаются и другие интерпретации. Имеющиеся данные указывают на то, что пространственное расположение полярных головок фосфа-тидилглицерина, сфингомиелина и фосфатидилсерина сходно. Исследования методом 2Н-ЯМР интактных фибробластов мыши и выделенных из них мембран также показали, что полярные головки как фосфатидилхолина, так и фосфатидилэтаноламина ориентированы параллельно поверхности мембран. Однако по данным дифракции нейтронов у фосфатидилглицерола, выделенного из Е. coli, полярная головка ориентирована примерно под углом 30° к поверхности мембраны, что облегчает связывание отрицательно заряженных фосфатных групп с катионами.
На ориентацию и динамику полярных головок липидных молекул может влиять образование межмолекулярных водородных связей на поверхности мембраны. Донорами и акцепторами при Образовании этих связей могут служить такие липиды, как фосфатидилсерин, фосфатидилэтаноламин и различные гликолипиды. Исследования, проведенные на модельных мембранных системах, показывают, что водородные связи между полярными головками сохраняются даже в условиях гидратации мембранной поверхности, однако пока неизвестно, как образование этих связей может сказаться на структуре биологических мембран.
2.5. КОНФИГУРАЦИЯ И УПАКОВКА АЦИЛЬНЫХ ЦЕПЕЙ В БИСЛОЕ
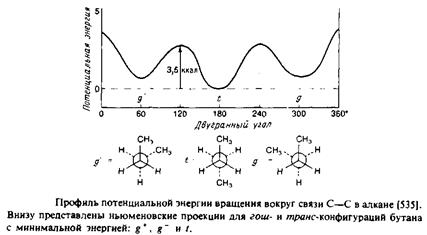
Рассмотрим сначала насыщенные углеводородные цепи. В них возможно свободное вращение вокруг каждой С—С-связи, характеризующееся энергетическим минимумом, особенно четким в случае ньюменовской проекции. Наиболее стабильна транс-конфигурация, при этом высота энергетического барьера для перехода через заслоненную конфигурацию в гош-форму составляет по оценкам 3,5 ккал/моль. В полностью m/wwc-конфигурации цепь максимально вытянута и не меняет своего направления, тогда как в гош-конформации ее направление меняется. Последовательность гош-транс-гош для трех смежных С—С-связей приводит к появлению в цепи излома, в результате чего участки цепи выше и ниже места излома оказываются значительно смещенными друг относительно друга. /ош-конфигурация в зависимости от направления вращения при переходе от Q к С4 обозначается как g+ или g". Кинки типа g + tg~ или g~ tg+ приводят к минимальному сдвигу цепи. Почти все двойные связи в мембранных липидах находятся в J/ис-конфигурации. Как и в случае гош-конфигурации, это приводит к изменению общего направления цепи. Наличие в углеводородных цепях кинков, двойных ^ыс-связей,
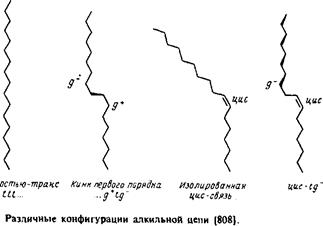
циклопропановых групп и других особенностей приводит к увеличению площади поперечного сечения цепи; это может иметь важные последствия для упаковки липидов в бислое. При этом стерические требования к упаковке углеводородных цепей и полярных головок такие же, как и в липидных крастал-лах. Эти принципы будут обсуждаться в разд. 2.3 при анализе формы мицелл.
Многие методы, включая дифракцию рентгеновских лучей и нейтронов, спектроскопию КР и ИК-спектрометрию, указывают, что в фазе геля насыщенные углеводородные цепи фосфолипидов находятся преимущественно в полностью-гпрднс-конфигурации. Минимальная площадь поперечного сечения молекулы диа-цильного фосфолипида равна около 38 A2. Примерно такую площадь занимает полярная головка фосфатидилэтанола-мина, поэтому насыщенные фосфатидилэтаноламины в гелевой фазе упаковываются так, что ацильные цепи располагаются перпендикулярно плоскости бислоя, как и в липидных кристаллах. В случае же кристаллов фосфатидилхолина минимальная площадь, приходящаяся на одну полярную головку, составляет примерно 50 А2. Поэтому дипальмитоилфосфатидилхолин в гелевой фазе не может упаковываться так, как фосфатидилэтаноламин. В этом случае ацильные цепи дипальмитоилфосфатидилхолина отклоняются на 30° от нормали к бислою, благодаря чему их поперечное сечение увеличивается и достигается соответствие размеру полярной головки. При этом углеводородные цепи сохраняют полнос-тью-транс-конфигурацию. В жидкокристаллической фазе появление в цепи гош-конформеров увеличивает эффективное поперечное сече-
