Капельный анализ
На мой взгляд, каждому химику-аналитику полезно знать основы капельного метода и уметь пользоваться им на практике.
Список литературы
1. Тананаев Н.А. Капельный метод. Качественный анализ неорганических веществ капельным методом: учебник/ Н.А. Тананаев.-6-е изд., перераб. и испр.-М.:Госхимиздат,1954.-274с.
2. Файгль Ф.Капельный анализ неорганических веществ: пер. с англ./Ф. Файгль, В. Ангер.-М.: Мир ,1976.- 394с.1 т.
3. Файгль Ф.Капельный анализ неорганических веществ: пер. с англ./Ф. Файгль, В. Ангер.-М.: Мир ,1976.- 322с.2 т.
ПРИЛОЖЕНИЕ
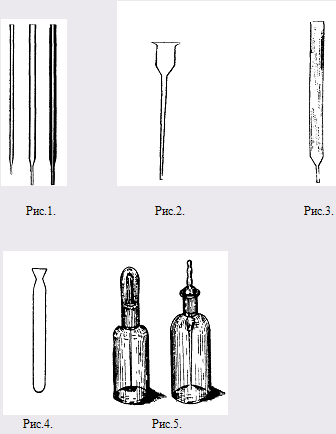
Рис.1. капиллярные трубочки
Рис.2. капилляр
Рис.3. стеклянная палочка
Рис.4. капельная пробирка
Рис.5. капиллярные склянки
Таблица 1 .Капельные реакции на катионы
|
Ион |
Реагент |
Уравнение реакции |
Окраска полученного соединения |
Условия проведения реакции |
|
Ag+ |
Соляная кислота |
AgNO3 + HCl→ AgCl + HNO3, AgCl + 2NH4OH→[Ag(NH3)2]Cl +2H2O, [Ag(NH3)2]Cl + 2HNO3 →AgCl + 2NH4NO3 |
Белый осадок, растворимый с образованием комплексных соединений, при подкислении которого снова выпадает осадок | |
|
Hg22+ |
Нитрит натрия |
Hg2(NO3)2 + 2NaNO2→ Hg + Hg(NO2)2 +2NaNO3 |
Черный или серый осадок |
Отсутствие избытка азотной кислоты |
|
Pb2+ |
Иодид калия |
Pb(NO3)2 + 2KI →PbI2 + KNO3 |
Желтый осадок |
Отсутствие избытка реагента |
|
Ca2+ |
Оксалат аммония |
CaCl2 + (NH4)2C2O4 → CaC2O4 + 2NH4Cl |
Белый осадок |
Нейтральная или среда |
|
Ba2+ |
Дихромат калия |
2BaCl2 + K2Cr2O7 +2CH3COONa + H2O → 2 BaCr2O7 + 2KCl + 2CH3COOH + 2NaCl |
Желтый осадок |
Присутствие ацетата натрия |
|
Zn2+ |
Дитизон |
ZnCl2 + 2C13H12N4S→ Zn(C13H11N4S)2 + 2HCl |
Малиново-красная окраска |
Присутствие органического растворителя |
|
Al3+ |
Ализарин |
3C14H6O2(OH)2 +Al(OH)3 → Al(C14H6O2(OH)O)3 + 3H2O |
Ярко-красная окраска |
Аммиачная среда, отсутствие Fe3+, Cr3+,SnII, Mn2+ |
|
SnII |
Иодид калия |
SnCl2 + KI→SnI2 +2KCl |
Красный осадок |
Избыток реагента |
|
SnIV |
Сероводород |
SnCl4 +2HCl → H2[Sn(Cl)6], H2[Sn(Cl)6] + 2H2S → SnS2 + 6 HCl |
Золотисто-желтый осадок |
Сначала перевести в комплекс |
|
Cr3+ |
Перманганат калия, перекись водорода |
Cr2(SO4)3+2KMnO4+ 5H2O→K2Cr2O7 + 2H2MnO3 + H2SO4; K2Cr2O7 + 4 H2O2 + H2SO4→2H2CrO6 + K2SO4 +3H2O |
Оранжевая окраска раствора переходит в синий цвет |
Наличие органического растворителя |
|
Mg2+ |
8-оксихинолин |
MgCl +2C9H6NOH + 2NH4OH→ Mg(C9H6NO)2 + 2NH4Cl |
Зеленовато-желтый осадок |
Аммиачная среда, pH=9,5-12,7 |
|
Fe2+ |
Красная кровяная соль |
3 FeCl2 + 2K3[Fe(CN)6] → Fe3[Fe(CN)6]2 + 6KCl |
Турнбулева синь |
pH=2-3, отсутствие окислителей и восстановителей |
|
Fe3+ |
Желтая кровяная соль |
4FeCl3 + 3K4[Fe(CN)6] → Fe4[Fe(CN)6]3 + 12KCl |
Берлинская лазурь |
pH=2,отсутствие оксалат-ионов, избытка реактива, окислителей и восстановителей |
|
Mn2+ |
Висмутат натрия |
2Mn(NO3)2 + 5NaBiO3 + 16HNO3 → 5 Bi(NO3)3 + 5NaNO3 + 2 HMnO4 + 7 H2O |
Розово-фиолетовая окраска |
Кислая реакция среды, отсутствие восстановителей, избытка ионов марганца |
|
Cd2+ |
Сероводород |
Cd(NO3)2 + H2S → CdS + 2HNO3 |
Желтый осадок |
Отсутствие ионов, образующих черные сульфиды |
|
Cu2+ |
Глицерин |
CuSO4 + CH2OH-CHOH- CH2OH + 2NaOH → CH2O(Cu)OCH-CH2OH + 2NaNO3 +2H2O |
Темно-синяя окраска |
Сильнощелочная среда |
|
Hg2+ |
Хлорид олова(II) |
SnCl2 + 2HgCl2 → Hg2Cl2 + SnCl4 ; Hg2Cl2 + SnCl2 → 2Hg + SnCl4 |
Белый осадок переходит в черный |
Избыток реактива |
|
Ni2+ |
Диметилглиоксим |
NiCl2 +2NH4OH+ +C4H8N2O2 → Ni(C4H7O2N2)2 + 2NH4Cl + 2H2О |
Ало-красная |
pH=8, отсутствие ионов железа(II) |
|
Co2+ |
Тиоцианат аммония |
CoCl2 + NH4SCN → (NH4)2[Co(SCN)4] + 2NH4Cl |
В водном растворе – розовая, в органической - синяя |
pH=4-5, насыщенный раствор реагента, отсутствие ионов железа(III) |
|
K+ |
Гексанитрокобальтат натрия |
2KCl + Na3[Co(NO2)6] → K2Na[Co(NO2)6] + 2NaCl |
Желтый осадок |
Нейтральная реакция среды, отсутствие катиона аммония |
|
Na+ |
Дигидростильбат калия |
NaCl + KH2SbO4 → NaH2SbO4 + KCl |
Белый осадок |
Нейтральная реакция среды, отсутствие катиона аммония |
|
NH4+ |
Реактив Несслера |
2NH4Cl + 2K2[Hg I4] + 4KOH →[ (Hg-O-Hg)NH2] + KCl + 7KI + 3H2O |
Красно-бурый осадок |
Реакция проводится в "газовой камере" |
