Масс-спектрометрический метод анализа
Буферы, такие, как Na+, K+, фосфат и соли представляют проблему для ESI из-за снижения давления пара капель, ведущего к ослаблению сигнала из-за увеличения поверхностного натяжения капель, ведущего к уменьшению летучести. Поэтому летучие буферы, такие, как ацетат аммония, могут быть использованы более эффективно.[6]
|
Таблица 1.3. Преимущества и недостатки ионизации электроспрея (ESI) | ||||
|
Устройство прибора ионизации электроспрея
Неосевая конфигурация ESI, которая сейчас используется во многих приборах для введения ионов в анализатор (как показано на рис. 1.10), показала себя очень эффективной при использовании с большим потоком жидкости. Основное преимущество такой конфигурации состоит в том, что скорость потока может быть увеличена без засорения или закупоривания входного отверстия. Неосевое распыление важно, потому что вход в анализатор более не насыщается растворителем, тем самым предохраняя капли от попадания во входное отверстие и его загрязнения. Наоборот, только ионы направляются ко входу. Это делает ESI ещё более совместимым с ЖХ при скоростях до мл/мин.
Ионизация наноэлектроспрея (nanoESI)
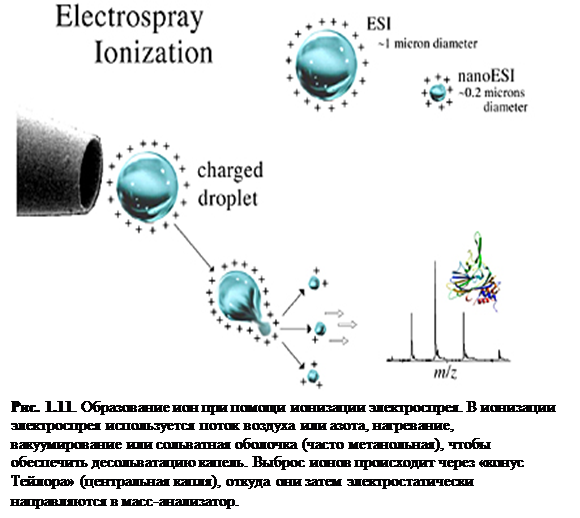 |
маленькой и расположена близко ко входу в масс-анализатор (рис. 1.11). Конечным результатом такой простой корректировки становится увеличение эффективности, которое включает уменьшение необходимого количества образца.
Скорости потока для nanoESI обычно составляют ль десятков до сотен нанолитров в минуту. Чтобы получить такие малые скорости потока, nanoESI использует источники из вытянутого и, в некоторых случаях, металлизированного стекла или плавленого кварца с малым входным отверстием (~ 5 мкм). Растворённый образец вносится в источник и к его концу прикладывается давление порядка 2 атм. Вытекание образца с очень малой скоростью позволяет достигать высокой чувствительности. Также, источники расположены очень близко ко входу в масс-анализатор, поэтому перенос ионов в масс-анализатор намного более эффективен. Например, анализ 5 mM раствора пептида при помощи nanoESI займёт одну минуту, употребив ~50 фемтомоль образца. Такой же эксперимент с обычным ESI за то же время израсходует 5 пикомоль, т.е. в 100 раз больше, чем nanoESI. К тому же, так как капли для nanoESI обычно меньше, чем для обычного ESI (рис. 1.11.), необходимое для образования ионов испарение намного меньше. Следовательно, nanoESI менее чувствительно к солям и другим примесям, т.к. меньшее испарение означает, что примеси не будут концентрироваться так сильно, как при ESI.[7]
Химическая ионизация при атмосферном давлении (APCI)
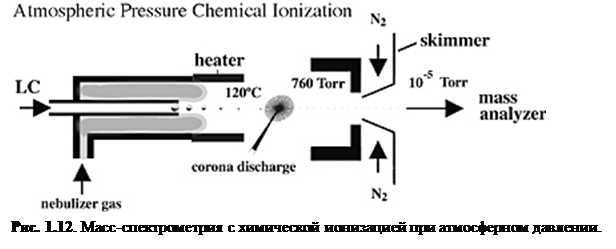 APCI также стала важным способом ионизации, потому что она генерирует ионы непосредственно из раствора и способна к анализу относительно неполярных соединений. Так же, как и в электроспрее, поток жидкости для APCI (рис. 1.12) вытекает непосредственно в устройство ионизации.
APCI также стала важным способом ионизации, потому что она генерирует ионы непосредственно из раствора и способна к анализу относительно неполярных соединений. Так же, как и в электроспрее, поток жидкости для APCI (рис. 1.12) вытекает непосредственно в устройство ионизации.
Однако сходство здесь заканчивается. Капли не заряжаются и APCI устройство содержите нагретый испаритель, который обеспечивает быстрое разделение/испарение капель. Молекулы образца в паре проходят через зону ионно-молекулярной реакции при атмосферном давлении.
В APCI ионизация возникает из-за возбуждения/ионизации растворителя коронным разрядом. Т.к. ионы растворителя существуют при атмосферном давлении, химическая ионизация молекул аналита очень эффективна; при атмосферном давлении молекулы аналита сталкиваются с ионами реагента очень часто. Перенос протона (для реакций протонирования MH+) образует положительные ионы, а перенос электрона или отщепление протона ([M-H]-) даёт отрицательные. Сглаживающее влияние сольватных оболочек на ионах реагента и высокое давление газа уменьшают фрагментацию во время ионизации и ведут к образованию практически только нетронутых молекулярных ионов. Многократная зарядка обычно не наблюдается, скорее всего, потому что процесс ионизации более энергичен, чем при ESI.[8]
Фотоионизация при атмосферном давлении (APPI)
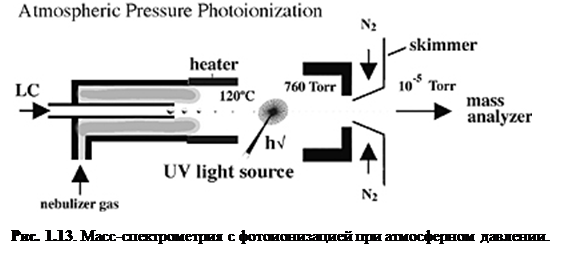
Фотоионизация при атмосферном давлении (APPI) стала сейчас важным способом ионизации, потому что она генерирует ионы непосредственно из раствора с относительно малым фоновым сигналом и способна к анализу относительно неполярных соединений. Так же, как и APCI, поток жидкости для APPI (рис. 1.13) вводится прямо в устройство ионизации.
Основное различие между APCI и APPI состоит в том, что в APPI парообразный образец проходит через ультрафиолетовый свет (обычная криптоновая лампа испускает от 10.0 эВ до 10.6 эВ). Часто APPI является намного более чувствительным, нежели ESI или APCI и показывает более высокое соотношение сигнал/шум из-за более низкой ионизации фона. Низкий сигнал фона во многом обусловлен высоким потенциалом ионизации стандартных растворителей, таких, как метанол и вода (10.85 и 12.62 эВ, соответственно), которые не ионизируются криптоновой лампой.
Недостатком ESI и APCI является то, что они образуют фоновые ионы растворителей. В дополнение к этому, ESI особенно подвержен эффектам подавления ионов, а APCI требует испарения при температурах 350-500°C, что может вызвать термическое разложение.
