Масс-спектрометрический метод анализа
Обычно тандемная масс-спектрометрия проводится столкновением выбранного иона с молекулами инертного газа, такого как аргон или гелий, и последующим анализом образовавшихся фрагментов. Тандемный анализ масс используется для определения последовательности пептидов, структурных характеристик углеводов, малых олигонуклеотидов и липидов.
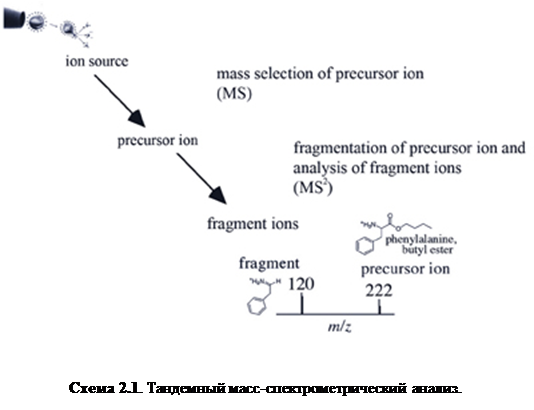
Термин «тандемный» анализ масс применяется для событий, последовательных в пространстве или во времени. Тандемный анализ масс в пространстве проводится последовательно расположенными анализаторами, тогда как тандемный во времени анализ масс осуществляется в одном и том же анализаторе, который отделяет нужный ион, фрагментирует его и анализирует фрагментарные ионы. Характеристики тандемного анализа для различных анализаторов приведены в таблице 2.2.
Скорость сканирования
Эта характеристика показывает скорость, с которой анализатор сканирует конкретный диапазон масс. Большинству приборов необходимо несколько секунд для полного сканирования, однако это время может сильно разниться в зависимости от анализатора. Времяпролётные анализаторы, например, совершают анализ в миллисекунды и даже быстрее. [12]
Конкретные виды анализаторов
Как известно, ESI и MALDI, например, генерируют ионы довольно различными способами. ESI Создаёт ионы в непрерывном потоке заряженных капель при атмосферном давлении, и ионы также создаются непрерывным потоком, по этим причинам квадрупольные анализаторы являются наиболее подходящими для ESI, так как они оба устойчивы к довольно высоким давлениям (~10-5 Торр) а и способны к непрерывному сканированию потока ионов из ESI. MALDI, с другой стороны, образует ионы посредством коротких, наносекундных, импульсов и хорошо совместимо с времяпролётным анализатором, который измеряет точно синхронизированные пакеты ионов, такие, как, например, полученные при помощи лазерного импульса.
Квадрупольный анализатор
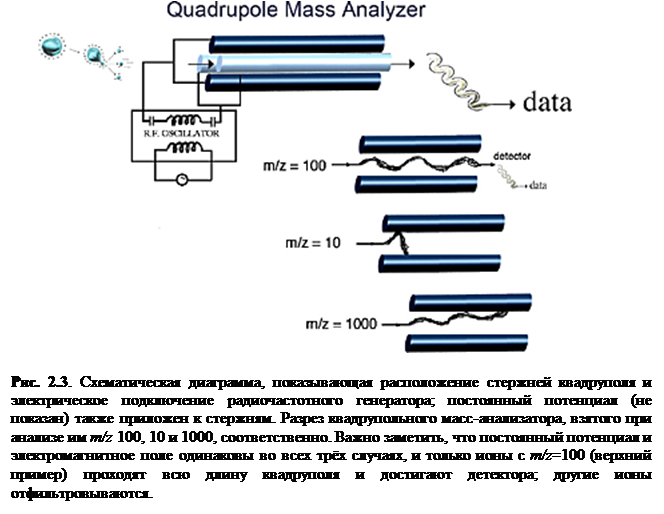 Квадрупольный анализатор масс (рис. 2.3) используется с EI-устройствами с 1950-х и до сих пор является самым распространённым анализатором. Интересно, что квадрупольные анализаторы оказались очень удобными для совмещения с ESI и APCI. Квадруполи имеют три основных достоинства. Они устойчивы к относительно высоким давлениям.
Квадрупольный анализатор масс (рис. 2.3) используется с EI-устройствами с 1950-х и до сих пор является самым распространённым анализатором. Интересно, что квадрупольные анализаторы оказались очень удобными для совмещения с ESI и APCI. Квадруполи имеют три основных достоинства. Они устойчивы к относительно высоким давлениям.
Во-вторых, квадруполи имеют значительный диапазон масс – они способны к анализу до m/z порядка 4000, что удобно, так как ионизация электроспрея белков и других биомолекул обычно дают такое распределение заряда, что m/z лежит в пределах от 1000 до 3500. Наконец, квадрупольные масс-спектрометры являются относительно дешёвыми приборами. Учитывая взаимно дополняющие особенности ESI и квадруполей, неудивительно, что первый успешный коммерческий прибор электроспрея был оснащён квадрупольным анализатором масс.
Квадрупольные анализаторы параллельно соединены с радиочастотным (RF) генератором и постоянной разностью потенциалов (DC). При определённой частоте RF, только ионы с соответствующим m/z могут пройти через квадруполь, как показано на рис. 2.3, где только ионы с m/z 100 детектируются. Во всех трёх случаях на рис. 2.3 DC и RF поля одинаковы. Поэтому сканированием RF поля может быть анализирован широкий m/z - диапазон (обычно от 100 до 4000) приблизительно за одну секунду.
Для проведения тандемного анализа масс с квадрупольным прибором,
необходимо разместить три квадруполя в ряд. Каждый квадруполь иг
рает отдельную роль: первый квадруполь (Q1) используется для сканирова
ния определённого m/z диапазона и выбора нужного иона; второй квадруполь
(Q2), также известный как ячейка столкновения, фокусирует и пропускает
ионы через подаваемый на путь пролёта вспомогательный газ (аргон или ге
лий); третий квадруполь (Q3) служит для анализа фрагментарных ионов, ге
нерированных в ячейке столкновения (Q2) (рис. 2.4). Последовательная схе
ма вызванной столк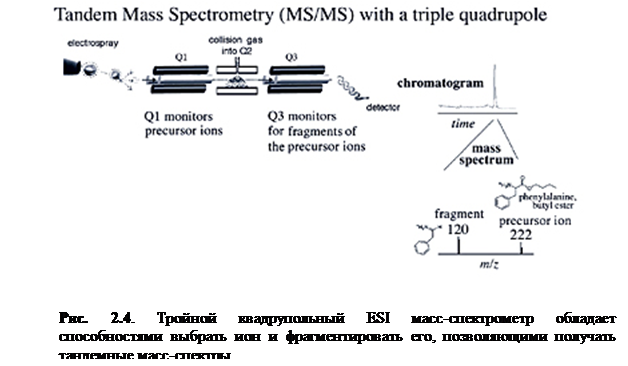 новением ионизации (CID) показана на схеме 2.1.
новением ионизации (CID) показана на схеме 2.1.
Квадрупольная ионная ловушка
Анализатор ионной ловушки показан на рис. 2.5 (реальным размером примерно с теннисный мяч) был придуман в то же время, что и квадрупольный анализатор масс, тем же человеком, Вольфгангом Паулом. Кстати, физика в основе обоих этих анализаторов сходна. Однако в ионной ловушке, вместо того, чтобы проходить через квадрупольный анализатор с наложенным радиочастотным полем, ионы ловятся в такое квадрупольное поле. Один из методов использования ионной ловушки для масс-спектрометрии включает в себя генерацию ионов непосредственно внутри при помощи EI, с последующим анализом масс. Другой, более популярный, метод использования ионной ловушки для масс-спектрометрии включает в себя генерацию ионов во внешнем устройстве при помощи ESI или MALDI и использование ионной оптики для введения образца в объём ловушки. Квадрупольная ионная ловушка обычно состоит из кольцевого электрода и двух гиперболических закрывающих электродов (рис. 2.5). Движение ионов, вызванное электрическим полем этих электродов, позволяет поймать или выпустить ионы из ловушки. В нормальном состоянии, радиочастота сканируется, чтобы резонансно возбудить и, вследствие этого, выпустить ионы через маленькие отверстия в «крышках» детектора. По мере того, как сканирование RF достигает более высоких частот, ионы с более высоким m/z возбуждаются, выпускаются и детектируются.
Очень полезной особенностью ионных ловушек является то, что они способны изолировать один вид ионов, выпустив все остальные из ловушки. Изолированные ионы могут быть, затем фрагментированы посредством столкновений, а фрагменты проанализированы. Основное преимущество квадрупольных ионных ловушек – то, что эксперимент с диссоциацией, вызванной многократными столкновениями, может быть проведён быстро без использования дополнительных анализаторов, так, что LC-MS/MS в реальном времени сейчас является обычным делом. Другими важными преимуществами квадрупольных ионных ловушек являются малые размеры и их способность ловить и накапливать ионы для обеспечения лучшего ионного сигнала. Квадрупольные ионные ловушки были приспособлены для ряда различных целей: от EI-MSn (рис. 2.5) биомолекул до их более современных совмещений с MALDI. MSn позволяет многократным MS/MS экспериментам проводиться с последовательными фрагментарными ионами, давая дополнительную фрагментарную информацию. Но главнейшим применением ионных ловушек является определение белков. LC-MS/MS эксперименты проводятся для белковых гидролизатов, давая информацию одновременно по MS и MS/MS. Эта информация позволяет идентифицировать белки и характеризовать пост-трансляционную модификацию. Диапазон масс (~4000 m/z) коммерческих LC-ловушек хорошо соответствует значениям m/z, генерируемым ионизацией электроспрея пептидов, а разрешение позволяет идентифицировать зарядное состояние многозарядных ионов пептидов. Масс-спектрометры квадрупольной ионной ловушки могут анализировать пептиды из трипсинового гидролизата при их содержании порядка 20-100 фмоль. Другим ценным качеством техники ионной ловушки для анализа пептидов является её способность проводить несколько стадий масс-спектрометрии, которые значительно увеличивают количество структурной информации. [13]
