Получение аллилового спирта гидролизом хлористого аллила
1.3.2 Электронная структура реагентов и продуктов реакции
Химическое поведение, реакционная способность молекулы зависит от природы составляющих ее атомов и от их взаимного расположения. Образуя молекулы, атомы изменяют свое состояние, влияют друг на друга. Наиболее сильно взаимодействуют между собой атомы, образующие химические связи.
Реагенты и продукты изучаемой реакции имеют неполярные (С - С, С = С) и полярные (С - Н, С - О, О - Н) ковалентные связи, возникающие в результате обобщения не спаренных валентных электронов с противоположными спинами. Зная число электронов во внешней оболочке атомов для любого органического и неорганического соединения легко написать октетные формулы. В них учитываются только внешние электроны атомов, как образующих так и не образующих химические связи.
Электронное строение аллилового спирта
Атом кислорода гидроксильной группы имеет sp3 гибридизацию. Средние длины связей 0,143 нм (С - О) и 0,091 нм (О - Н). Обе связи полярны. Однако некоторые ученые считают их в значительной мере поляризованными электроотрицательным атомом кислорода [12, 24, 26, 31].
Относительно высокие значения температуры кипения и диэлектрической проницаемости аллилового спирта объясняют полярностью группы ОН- и ее способностью образовывать водородные связи. Кислород является более электроотрицательным элементом, по сравнению с углеродом, и поэтому электронная плотность смещена в сторону кислорода. Дипольный момент ОН- группы равен 5,5·1028 Кл·м [4].
Функциональная группа спиртов содержит электроотрицательный атом кислорода с двумя неподеленными парами электронов. Его конфигурация близка к тетраэдрической и показана на рис. 1[4, 33].
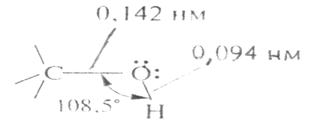
Рис. 1. Конфигурация функциональной группы спиртов
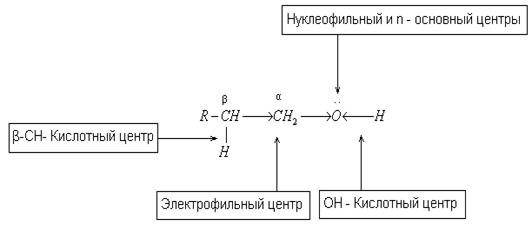
В молекуле спиртов можно выделить следующие реакционные центры, показанные ниже на рис. 2 [4, 12, 13, 33]:
• ОН - кислотный центр, обусловливающий возможность отщепления протона вследствие высокой полярности связи О - Н;
• нуклеофильный и n-основный центр — атом кислорода, имеющий не -поделенные пары электронов;
• электрофильный центр — α-атом углерода, на котором дефицит электронов вызван — I-эффектом соседней гидроксильной группы;
• β – СН - кислотный центр, в котором поляризация связи С - H также обусловлена электроноакцепторным влиянием гидроксильной группы.
![]()
Рис. 2. Реакционные центры спиртов
Большинство реакций спиртов протекают с разрывом связей О - Н или
С - О.
Для спиртов также характерны реакции, в которых участвуют
α – Н - атом (окисление), β – Н - атом (дегидратация) или δ – Н – атом
(окислительная циклизация) [2].
Гидроксильная группа в молекуле аллилового спирта отдалена от двойной связи, поэтому в данном соединении не наблюдается сопряжения связи с заместителем и поляризующее влияние на его π - связь проявляется в значительно меньшей степени, чем в молекулах винильных соединений. Эти особенности химического строения аллилового спирта обуславливают его малую реакционную способность в процессах полимеризации. Еще менее активен его радикал [3].
Электронное строение воды
Молекула воды полярна. Угол НОН составляет 104,5˚. Связь О - Н является ковалентной полярной. Между молекулами воды возникает водородная связь, которая изображается точками [12].
![]() …Нσ+
…Нσ+![]() Оα-… Нσ+
Оα-… Нσ+ ![]() Оα-…
Оα-…
![]() Нσ+…
Нσ+…
Нσ+…
Связи О - Н в молекулах воды имеют заметный полярный характер с избытком отрицательного заряда σ- на атоме кислорода. Атом водорода, наоборот, приобретает небольшой положительный заряд σ+ и может взаимодействовать с неподеленными парами электронов атома кислорода соседней молекулы воды.
Взаимодействие между молекулами воды оказывается достаточно сильным, таким, что даже в парах воды присутствуют димеры и тримеры состава (Н2О)2, (Н2О)3 и т. д. В растворах же могут возникать длинные цепи ассоциатов, поскольку атом кислорода имеет две неподеленные пары электронов.
Дипольный момент воды равен 6,1·1028 Кл·м
1.3.3 Химические свойства реагентов и продуктов реакции
Рассмотрим наиболее типичные реакции, в которые могут вступать реагенты и продукты реакции.
1.3.3.1 Химические свойства аллилового спирта
Аллиловый спирт, имея в молекуле кратную связь и гидроксильную группу, проявляет свойства спиртов и непредельных соединений:
1. Взаимодействие с галогенами с образованием β - дигалоидгидринов глицерина
Совершенно иначе, чем этиловый спирт, относится аллиловый спирт к хлору и брому; тогда как обыкновенный спирт дает с ними продукты замещения и окисления (напр. хлораль), аллиловый спирт прямо присоединяет два атома хлора, брома или йода, образуя β-дигалоидгидрины глицерина C3H6Cl2O, C3H6Br2O и C3H6J2O [2]:
![]() ,
,
2,3-дибромпропанол-1
![]() .
.
2,3-дихлорпропанол-1
2. Реакция гидрирования [10]:
![]() .
.
пропанол-1
3. Реакция гидратации в присутствии кислорода с образованием глицерина [24]:
![]() .
.
глицерин
4. Окисление с образованием альдегида [24]
Окислителями переводится в альдегид - акролеин, дальнейшее окисление дает акриловую кислоту:
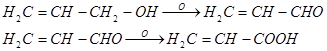 .
.
5. Взаимодействие со щелочными металлами с образованием алкоголятов [10]
Со щелочными металлами получаются алкоголяты, которые при действии хлористого аллила дают соответствующий этиловому эфиру аллиловый эфир (С3Н5)2О:
![]() ,
,
алкоголят
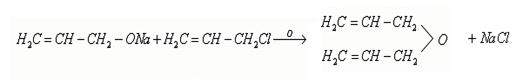
6. Межмолекулярная дегидратация спиртов с образование простых эфиров [27]:
![]() .
.
этилаллиловый эфир
7. Взаимодействие с минеральными и органическими кислотами с образованием сложных эфиров
Образование сложных эфиров происходит при взаимодействии с минеральными и органическими кислотами [26]:
![]() ,
,
аллилацетат
![]() .
.
