Проектирование производства фосфорсодержащего вещества
Несимметричные фосфиты можно применять для получения разнообразных несимметричных эфиров фосфорной и фосфиновых кислот отдельные представители которых обладают физиологической активностью.
Большой интерес представляет переэтерификация диалкилфосфитов гликолями. В результате переэтерификации диалкилфосфитов гликолями, главным образом этиленгликолем (в сходных условиях), получаются полимерные продукты.
Например, при переэтерификации диэтилфосфита диэтиленгликолем, тетраэтиленгликолем, гексаэтиленгликолем, пропиленгликолем-1,2; бутиленгликолем-1,3; бутиленгликолем-1,4; 2-бутиндиолом-1,4 и диэтаноламином образуются полиэфиры, состоящие из 2—3 остатков исходных веществ [5].
Высокомолекулярные полифосфиты легко образуются при реакции диэтилфосфита и других простейших диалкилфосфитов с гликолями, обладающими пространственно-разобщенными гидроксилами или неустойчивыми в конформациях со сближенными гидроксилами:
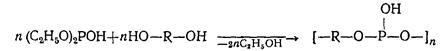
Механизм реакции переэтерификации эфиров кислот трехвалентного фосфора
Механизм реакции переэтерификации эфиров кислот трехвалентного фосфора подробно не изучен. Предполагается, что механизм этой реакции состоит в чередующихся процессах присоединения протона к атому фосфора, алкоксил-аниона — к фосфоний-катиону и отщепления спирта от промежуточного продукта с пятивалентным фосфором с образованием исходного или другого фосфита или фосфинита:
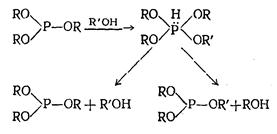
Косвенным подтверждением образования промежуточного продукта присоединения являются данные по изучению механизма реакции Арбузова и ее различных вариантов, а также экспериментальные материалы по алкоголизу зфиров кислот трехвалентного фосфора.
Первый акт реакции является необходимым, но недостаточным для осуществления переэтерификации фосфита (фосфинита). Образовавшийся аддукт, как показано выше, может расщепляться по двум направлениям. При алкоголизе любого фосфита любым спиртом устанавливается равновесие:
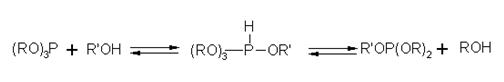
Переэтерификация произойдет в том случае, если равновесие сдвинуто вправо, т. е. если отщепится от аддукта алкоксил (или остаток фенола) исходного фосфита, а не алкоксил спирта, взятого для переэтерификации. Таким образом, решающее влияние на процесс переэтерификации оказывает второй акт реакции — расщепление продукта присоединения, который, по-видимому, определяет не только направление реакции, но и ее скорость.
Решение вопроса о том, какая молекула спирта будет отщепляться от промежуточного продукта, находится в прямой зависимости от электрофильности алкокси(фенокси)-групп, входящих в его состав. Очевидно, чем электрофильнее алкоксил, тем предпочтительнее он будет отщепляться вместе с протоном в виде «более кислого» спирта. Следовательно, при получении фосфитов методом переэтерификации желательно брать исходный фосфит с алкоксигруппами более электрофильными, чем алкоксил спирта, используемый в реакции.
Равновесие реакции переэтерификации можно сдвинуть вправо и путем отгонки выделяющегося спирта. Этим приемом широко пользуются при получении разнообразных фосфитов, когда выделяющийся спирт кипит ниже исходного.
Другой возможный механизм [5] заключается в атаке атома кислорода алкилкатионом (образующимся в результате гетеролитического расщепления спирта) и одновременного выделения алкилкатиона исходного эфира:

Однако это направление реакции имеет второстепенное значение, как при переэтерификации l- и d-бутанолами-2 и оптически активным пентанолом получаются фосфиты, дающие при гидролизе спирты, в первом случае — с 75% оптической активности от первоначальной, и во втором,— 100%. В том случае, если бы реакция протекала только по второму направлению, при гидролизе продуктов переэтерификации должны были бы образоваться оптически неактивные спирты.
Представляется перспективным использование в этих синтезах микроволнового излучения, значительно снижающего время протекания реакции (в десятки и сотни раз) по сравнению с традиционно используемым нагреванием.
Нормативно-техническая документация на сырьё, вспомогательные материалы и готовую продукцию
Гидрохинон
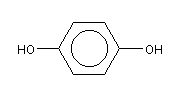
Химическая формула:
C6H4(OH)2
Квалификация «ч», ГОСТ 19627-74;
Внешний вид: кристаллы от белого до беловато-серого цвета (возможен желтоватый оттенок). При продолжительном воздействии света кристаллы гидрохинона темнеют и теряют блеск.
Фасовка: мешки по 0,5 или 25 кг.
Метакриловый эфир этиленгликоля (МЭГ) C6H10O3
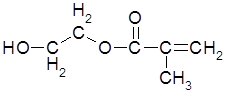
Величина ПДК рабочей зоны 20 мг/м3 (согласно ГОСТ 12.1.005-88), класс опасности IV.
Плотность (20 °C) 1.069 - 1.072 г/см3, массовая доля основного вещества 97%.
Поставляется наливом (ж/д цистерны, автоцистерны, кубы 1000 л, бочки 200л, 100 л).
Нормативно-технических документов (ГОСТ, ТУ) на диметиловый эфир β-циано-этилфосфоновой кислоты, а также конечный продукт нет, поскольку эти вещества не производятся промышленно.
Физико-химические и теплофизические свойства исходных, промежуточных, побочных, целевых продуктов и отходов производства
Гидрохинон
При нормальных условиях представляет собой кристаллы от белого до беловато-серого цвета. При продолжительном воздействии света кристаллы гидрохинона темнеют и теряют блеск.
Хорошо растворим в воде, спирте, МЭГ, эфире.
Температура плавления равна 172 °С;
Температура кипения составляет 285 °С;
Метакриловый эфир этиленгликоля (МЭГ) C6H10O3
Бесцветная прозрачная жидкость.
Величина pH 4.0 (500 г/л, H2O, 20 °C);
Температура плавления -12°C;
Температура воспламенения 101 °C;
Температура кипения: 250 °C (760 мм.рт.ст.); 95°C ( 9 мм.рт.ст.);
Плотность (20 °C) 1,069 – 1,072 г/см3;
Содержание основного вещества 97%;
Хорошо растворим в воде, спирте.
Диметиловый эфир β-цианоэтилфосфоновой кислоты [26]:
Бесцветная жидкость.
Температура кипения составляет 127-129 °С при давлении 4 гПа;
Плотность (20 °С) составляет 1,1970 г/см3;
Продукт переэтерификации (ди(2-метакрилоил β-оксиэтиловый) эфир 2-цианоэтилфосфоновой кислоты)
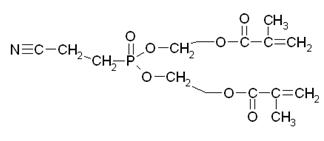
Представляет собой бесцветную, прозрачную, подвижную жидкость склонную к самопроизвольной полимеризации. Для ее предотвращения необходима стабилизация продукта гидрохиноном (около 1% масс.).
Метанол (карбинол) СH3ОН:
Бесцветная легкоподвижная жидкость с характерным запахом этилового спирта.
Молекулярная масса 32,04;
Плотность 0,7923;
Температура плавления -97,8 °С;
Температура кипения 64,7 °С;
Неограниченно растворим в воде, этиловом спирте и эфире.
