Синтез и анализ ХТС в производстве ацетона
Перед подачей реагентов в контактный аппарат (рис. 2) изопропиловый спирт испаряют в испарителе-сатураторе, насыщают парами воздуха и перегревают полученную паровоздушную смесь. Реакция протекает вадиабатических условиях, т. е. тепло, выделяющееся в процессе окисления, воспринимается самой реакционной смесью.
При окислении, «роме ацетона, образуется также некоторое количество побочных продуктов, в том числе уксусной кислоты и ацетальдегида. Поэтому контактные газы после прохождения ими металлического катализатора пропускают через насадку в виде слоя мела, на которой уксусная кислота и ацетальдегид почти количественно превращаются в ацетон. Оптимальной для этой реакции является температура 450 °С, достигаемая охлаждением контактных газов во встроенном в реактор змеевике.
Из контактного аппарата газы поступают в котел-утилизатор, а затем последовательно на «парциальную» конденсацию и водную абсорбцию. Несконденсировавшиеся газы после абсорбции ацетона водой сбрасывают в атмосферу. Промывные воды из скруббера объединяют с конденсатом и направляют на ректификацию.
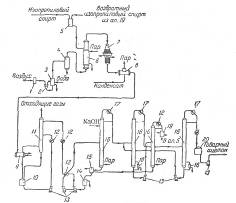
Рис. 2. Принципиальная схема производства ацетона неполным окислением изопропилового спирта в паровой фазе:
1 – висциновый фильтр; 2 – ротационный компрессор; 3, 9, 12, 19 – холодильники; 4 – ресивер; 5 – сборник изопропилового спирта; 6 – испаритель-сатуратор; 7 – контактный аппарат; 8 – котел-утилизатор; 9 – сборник конденсата; 10 – скруббер; 11 – насосы; 12 – сборник сточной воды; 15 – сепаратор; 16 – ректификационные колонны; 17 – дефлегматоры; 18 – кипятильники; 20 – сборник ацетона.
В первой по ходу процесса ректификационной колонне из водного раствора отгоняют ацетон и изопропиловый спирт. В верхнюю часть колонны для очистки от осмоляющихся примесей подают 15%-ный раствор NaOH. Вода из куба колонны после осаждения органических веществ и утилизации ее тепла подается в скруббер на абсорбцию ацетона.
В следующей колонне происходит разделение продуктов на ацетон-сырец и раствор изопропилового спирта. Ацетон-сырец поступает на ректификацию для выделения товарного ацетона; изопропиловый спирт выделяют перегонкой из водного раствора и возвращают на окисление.
Неполное окисление изопропилового спирта в жидкой фазе.
Интересным методом получения ацетона из изопропилового спирта является его неполное окисление и жидкой фазе. Этот метод, применяемый для производства перекиси водорода, осуществляется с 1957 г. на заводе фирмы «Shell Chemical Со.» в США [2].
Процесс протекает по схеме
СН3СН(ОН)СН3 + О2 → СН3СОСН3 + Н2О2
и проводится автокаталитически при 90 – 140°С под давлением, позволяющем удерживать смесь в жидкой фазе. В качестве окислителя можно применять как воздух, так и кислород.
Реактор должен быть изготовлен из материалов, не разлагающих перекись водорода. На окисление подают 89%-ный раствор изопропилового спирта; по достижении концентрации перекиси водорода 15 – 25% продукт выводится из реактора, разбавляется водой и стабилизируется. Ацетон и не прореагировавший спирт отгоняют и очищают, перекись водорода концентрируют быстрым испарением и вакуум-перегонкой.
Выход ацетона составляет 95% от теоретического, выход перекиси водорода – около 87 %25.
Другие методы получения ацетона
Ацетон получается также в качестве побочного продукта в синтезе аллилового спирта из изопропилового спирта и акролеина:
СН3–СН(ОН) –СН3 + СН2=СН–СНО → СH2=СН–СН2ОН + СН3–СО–СН3
Эта реакция проводится в паровой фазе при 350–450 °С и атмосферном давлении в присутствии катализатора – смеси окиси магния и окиси цинка.
Данный процесс, так же как и процесс получения ацетона и перекиси водорода из изопропилового спирта, является составной частью синтеза глицерина по методу американской фирмы «Shell Chemical Со.»:
|
| ||||
а) пропилен → изопропиловый спирт → ацетон + перекись водорода
|
б) пропилен → акролеин
в) акролеин + изопропиловый спирт → аллиловый спирт + ацетон
г) аллиловый спирт + перекись водорода → глицерин.
Значительные количества ацетона производят из этилового спирта, ацетилена и уксусной кислоты. Все три процесса по механизму, вероятно, сходны между собой.
Реакция
2С2Н5ОН + Н2О--- → СН3СОСН3 + СО2 + 4Н2
протекает при взаимодействии паров этилового спирта и воды в присутствии катализатора — окиси железа, активированной известью; температура процесса 470 °С. Водной промывкой из контактных газов выделяют ацетон в виде 5%-ного водного раствора. Выход ацетона по этиловому спирту составляет 86% [2]. Катализатор нуждается в периодической регенерации, общий срок его службы — 6 месяцев. Реакцию
2СН=СН + ЗН2О → СН3СОСН3 + СО2 + 2Н2
проводят пропусканием ацетилена в смеси с избытком водяного пара над катализатором, состоящим из окисей цинка ижелеза. Процесс протекает при той же температуре (470 °С), что и синтез ацетона из этилового спирта. Катализатор периодически регенерируют. При промывке контактных газов водой получают 10%-ный водный раствор ацетона, который подвергают ректификации. Выход ацетона равен 85% от теоретического. Эта реакция успешно осуществлялась даже при применении газа, содержащего 8% ацетилена («разбавленный» ацетилен).
В обоих описанных процессах ацетон получается, по-видимому, в результате декарбоксилирования промежуточно образующейся уксусной кислоты, способность которой превращаться в (СН3)2СО при нагревании с солями металлов (например, с ацетатом кальция) известна уже давно.
Это обстоятельство использовано для оформления в промышленном масштабе процесса производства ацетона пропусканием паров уксусной кислоты над окисью церия (осажденной на пемзе) при 400—450 0С и атмосферном давлении:
2СН3СООН → СН3СОСН3 + СО2 + Н2О
Выход ацетона достигает 95% от теоретического.
Одним из путей получения ацетона в промышленности является каталитическое окисление пропан-бутановых смесей при низкой температуре и высоком давлении, осуществленное вСША фирмами «Gelanese Corporation of America» и «Warren Petroleum Co.».
Наряду с ацетоном в этом процессе образуются также уксусная кислота (главный продукт), метилэтилкетон, ацетальдегид, метанол, муравьиная, пропионовая и масляная кислоты и различные лактоны.
