Химическая термодинамика
Ответ: а) ![]() = -808,97 кДж
= -808,97 кДж
б) ![]() = -539,72 кДж
= -539,72 кДж
в) ![]() = -343,18 кДж
= -343,18 кДж
г) ![]() = 238,5 кДж
= 238,5 кДж
д) ![]() = 298,4
= 298,4
е) ![]() = 3350,9 кДж
= 3350,9 кДж
Задание № 6.
Уменьшается или увеличивается энтропия при переходах: а) воды в пар; б) графита в алмаз? Почему?
Решение:
В 1911 г. Макс Планк предложил следующий постулат: энтропия правильно сформированного кристалла чистого вещества при абсолютном нуле равна нулю. Этот постулат может быть объяснен статистической термодинамикой, согласно которой энтропия есть мера беспорядочности системы на микроуровне:
S = RlnW , (8.9)
где W – число различных состояний системы, доступное ей при данных условиях, или термодинамическая вероятность макросостояния системы;
R = 1,38.10-16 эрг/град, постоянная Больцмана.
Это "уравнение Больцмана", выведено М.Планком в 1900 г,
Очевидно, что энтропия жидкости существенно превышает энтропию твердого тела, а энтропия газа – энтропию жидкости.
Sгаз>>Sж>>Sтв
 Чем сложнее молекула газа, тем больше ее энтропия.
Чем сложнее молекула газа, тем больше ее энтропия.
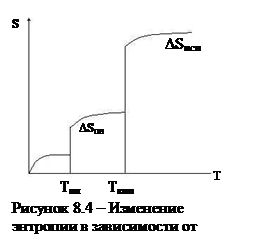
При Т=0 S=0. При повышении Т начинаются колебания атомов и S растет до Тпл.
Далее следует фазовый переход и скачок энтропии DSпл.С повышением Т S плавно и незначительно растет до Тисп, где опять наблюдается резкий скачок DSисп и опять плавное увеличение.
Знак изменения энтропии часто можно предсказать, исходя их уравнения реакций. Уменьшение количества газовых молей означат уменьшение энтропии и наоборот.
Ответ:
а) Переход жидкости в газообразное состояние ведёт к повышению энтропии.
Sгаз>>Sж
б) Переход графита в алмаз ведёт к понижению энтропии.
Список используемой литературы: 1)Глинка Н. Л., Общая химия, Ленинград,1980; 2)Берсукер И. Б., Аблов А. В., Химическая связь в комплексных соединениях, Кишинев, 1962; 3)Тучков Р. В., Лекции по общей химии, Бийск, 2004; 4)Головня В. А., Федоров И. А., Основные понятия химии комплексных соединений, М., 1961; 5)Коттон Ф., Уилкинсон Дж., Современная неорганическая химия, пер. с англ., ч. 1-3, М., 1969; 6)Коровин Н. В., Общая химия, М.:Высшая школа, 2002.
