Электрофильное ароматическое замещение
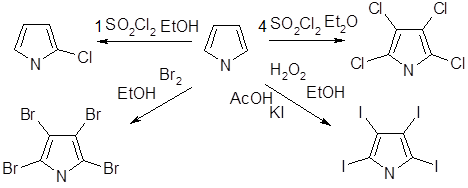
2-Бром - и 2-хлорпирролы — нестабильные соединения, которые можно получить прямым галогенированием пиррола. Использование 1,3-дибром-5,5-диметилгидантоина в качестве бромирующего агента приводит к образованию 2-бром - и 2,5-дибромпирролов; продукты бромирования стабилизируют немедленным превращением в N-трет-бутилоксикарбонильные производные. Бромирование N-трет-бутилоксикарбонилпиррола с использованием N-бромсукцинимида приводит к 2,5-дибромпроизводному
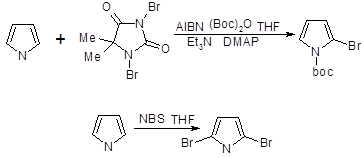
При монобромировании и моноиодировании N-триизопропилсилилпиррола образуются практически исключительно 3-галогенозамещенные пирролы, а использование двух эквивалентов N-бромсукцинимида позволяет получить 3,4-дибромпроизводное
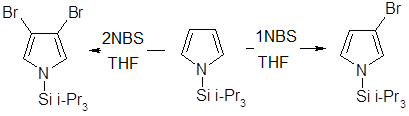
Ацилирование
Прямое ацетилирование пиррола уксусным ангидридом при 200 °С приводит к образованию 2-ацетилпиррола с примесью небольшого количества 3-ацетилпирола; N-ацетилпиррол в этих условиях вовсе не образуется N-Ацетилпиррол можно получить с высоким выходом при нагревании пиррола с N-ацетилимидазолом.
Алкильные заместители облегчают процесс ацилирования по атому углерода: так, 2,3,4-триметилпиррол превращается в 5-ацетилпроизводное даже при кипячении в уксусной кислоте. Более реакционноспособные трифторуксусный ангидрид и трихлорацетилхлорид реагируют с пирролом даже при комнатной температуре с образованием продуктов 2-ацилирования, которые в результате гидролиза или алкоголиза обеспечивают удобный синтетический подход к пиррол-2-карбоновым кислотам или их эфирам.
Сильные электроноакцепторные заместители (мета-ориентирующие группы) в α -положении пиррольного кольца склонны изменять присущую пирролу региоселективность в реакциях электрофильного замещения — последующее замещение протекает по положению 4, а не по свободному α-положению.
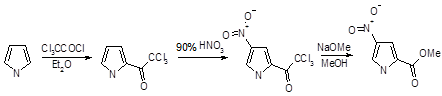
Алкилирование
Моноалкилпроизводные пиррола (по атому углерода) не удается получить прямой реакцией пиррола с алкилгалогенидами как в результате катализируемого кислотой Льюиса алкилирования, так и в отсутствие катализатора. Пиррол не вступает в реакцию с метилиодидом при температурах ниже 100˚С, однако при температурах выше 150˚С в результате серии превращений образуется сложная смесь, состоящая главным образом из продуктов полимеризации и некоторого количества полиметилированных производных пиррола. Более реакционноспособный аллилбромид реагирует с пирролом при комнатной температуре, однако в результате этого взаимодействия образуется смесь различных аллилпирролов (от моно - до тетразамещенных) одновременно с продуктами олигомеризации и полимеризации. Наиболее гладко пиррол моноалкилируется сопряженными енонами, содержащими уходящую группу в β-положении.
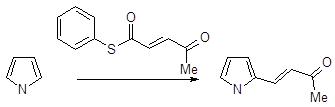
1.2.2 Электрофильное замещение тиофена
Как и следовало ожидать, для тиофена характерны реакции, свойственные ароматическим соединениям типа бензола. Тиофен галогенируется, нитруется, сульфируется и ацилируется аналогично фурану и пирролу, но в более жестких условиях.
Протонирование. Реакции протонированных тиофенов
Вследствие высокой стабильности тиофенов в их реакциях электрофильного замещения могут быть успешно использованы комбинации ряда реагентов с сильными кислотами, обычно приводящие к кислотно-катализируемому разложению и полимеризации фуранов и пирролов. Изучение катализируемого кислотами обмена на атом водорода других групп, например кремния или ртути , показало, что скорость атаки по положению 2 примерно в 1000 раз выше, чем по положению 3. Так, для 2,5-ди-трет-бутилтиофена рКа при образовании соли за счет протонирования по положению 2 составляет —10,2.При обработке тиофена горячей фосфорной кислотой получается тример, строение которого предполагает, что на первой стадии образование связи С—С вдет через α-протонированный катион.
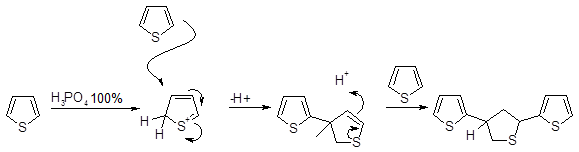
Нитрование
Нитрование тиофена следует проводить в отсутствие азотистой кислоты, которая может привести к взрыву; наиболее удобно использование ацетилнитрата или тетрафторбората нитрония. Наряду с преимущественным образованием 2-нитросоединения получают и 3-изомер с выходом -10%. Дальнейшее нитрование как 2-, так и 3-нитротио-фенов также приводит к образованию смесей: из 2-нитротиофена образуются эквивалентные количества 2,4- и 2,5-динитротиофенов, а из 3-изомера — в основном 2,4-динитротиофен. Аналогично, предсказуемая смесь изомеров образуется при нитровании замещенных тиофенов: например, 2-метилтиофен дает смесь 2-метил-5- и 2-метил-З-нитротиофенов, а 3-метилтиофен -4-метил-2- нитро- и 3-метил-2-нитротиофены в соотношении 4:1 в каждом случае.
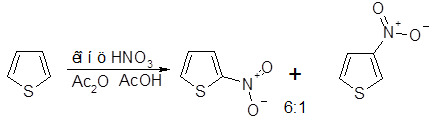
Сульфирование
Получение тиофен-2-сульфокислоты при сульфировании серной кислотой уже давно известно, однако использование комплекса пиридинсульфотриоксид, возможно, более удобный метод. 2-Хлорсульфонилирование и 2- тиоцианирование также достаточно эффективны.
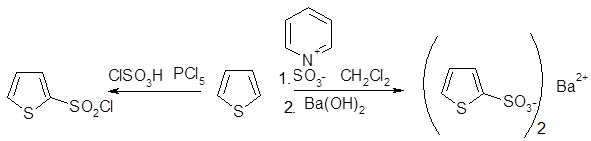
Галогенирование
Галогенирование тиофена происходит очень быстро и как при комнатной температуре, так и при -30 °С в темноте легко проходит тетразамещение . Скорость галогенирования тиофена при 25 °С примерно в 108 раз больше, чем бензола. Образование как 2,5-дибром - и 2,5-дихлортиофенов, так и 2-бром- и 2-иодтиофенов гладко происходит в различных контролируемых условиях. Контролируемое бромирование 3-бромтиофена дает 2,3-ди-бромтиофен.

Трибромирование тиофена гладко протекает в 48%-ном растворе НВг. Давно известно, что при обработке полигалогенотиофенов цинком и кислотой удается селективно удалять α-галоген, что делает доступным получение 3-бромтиофена, а 3,4-дибромтиофен аналогично образуется при восстановлении тетрабромида. При использовании боргидрида натрия из 2,3,5-трибромтиофена получают 2,3-дибромтиофен (в присутствии катализатора Pd(0))или 2,4-дибромтиофен (без катализатора).
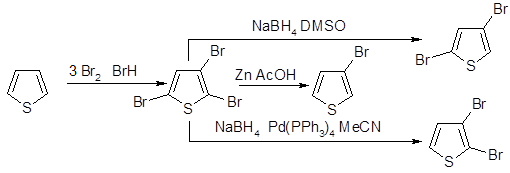
Моноиодирование α-замещеиных тиофенов, независимо оттого, оказывают ли эти заместители активирующее или дезактивирующее влияние, идет по второму α-положению при действии иода и иодбензолдиацетата. 3-Алкилтио-фены можно монобромировать или моноиодировать по положению 2 при использовании N-бромсукцинимида или иода в присутствии оксида ртути(II) соответственно.
Ацилирование
Ацилирование по Фриделю-Крафтсу наиболее часто используется для тиофенов и обычно дает хорошие выходы в контролируемых условиях. Несмотря на то, что при взаимодействии тиофена с AlCl3 получаются смолы, их образования можно избежать, если добавлять катализатор к тиофену и ацилирующему агенту. Наиболее часто в качестве катализатора используют хлорид олова. Эффективный метод — ацилирование ангидридами, катализируемое фосфорной кислотой. В реакциях с ацетил-п-толуолсульфонатами в отсутствие катализаторов с высоким выходом образуется 2-ацетилтиофен. При формилировании тиофена по Вильсмейеру получают 2-формилтиофен. 2-Формилпроизводное образуется также из 3-фенилтиофена в условиях реакции Вильсмейера.
