Электрофильное ароматическое замещение
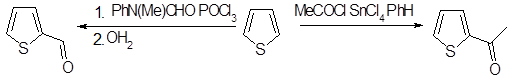
Алкилирование
Алкилирование проходит достаточно легко, однако редко используется в препаративной химии. Одним из примеров может служить эффективное 2,5-бис-трет-бутилирование тиофена.
Конденсация с альдегидами и кетонами
Кислотно-катализируемые реакции тиофена с альдегидами и кетонами неприменимы для получения гидроксиалкилтиофенов, так как они нестабильны в условиях реакции. Однако можно осуществить хлоралкилирование, а при использовании хлорида цинка даже тиофены, имеющие электроноакцепторные заместители, вступают в эту реакцию. Необходимо тщательно подбирать условия, так как возможно образование как ди-2-тиенилметанов, так и 2,5-бис(хлорметил)тиофена.
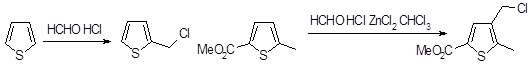
1.2.3 Электрофильное замещение фурана
Среди трех пятичленных систем с одним гетероатомом, фуран представляет собой «наименее ароматическое» соединение и, как таковой, проявляет наибольшую склонность к реакциям присоединения.
Это верно в отношении как взаимодействия с обычными электрофильными реагентами, используемыми в реакциях замещения, так и процессов типа реакции Дильса-Альдера.
Нитрование
Чувствительность фуранов не позволяет использовать концентрированную кислотную нитрующую смесь. При взаимодействии фурана или замещенных фуранов с ацетилнитратом первоначально образуются неароматические аддукты, в которых образованию продуктов замещения препятствует процесс нуклеофильного присоединения ацетата к катионному интермедиату, обычно по положению 5. Ароматизация с потерей уксусной кислоты, приводящая к образованию нитропроизводного, происходит под действием растворителя; наилучшие результаты достигаются при использовании слабого основания, такого, как пиридин.
Дальнейшее нитрование 2-нитрофурана дает 2,5-ди-нитрофуран в качестве основного продукта реакции.
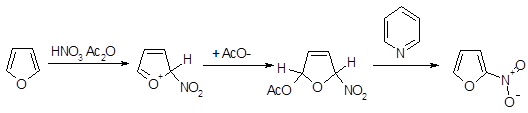
Сульфирование
Фуран и алкилфураны разлагаются под действием обычных сильных кислот, однако можно использовать комплекс пиридинсульфотриоксид, под действием которого происходит дизамещение фурана даже при комнатной температуре.
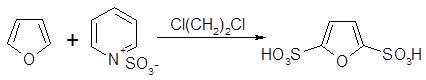
Галогенирование
Фуран энергично реагирует с хлором и бромом при комнатной температуре с образованием полигалогенированных соединений, но не реагирует с иодом. В более контролируемых условиях можно получить 2-бромфуран. реакция, по-видимому, протекает через образование 1,4-дибром-1,4-дигидроаддукта, поскольку такие частицы были действительно обнаружены при низкой температуре с использованием спектроскопии ПМР. В реакции с бромом в диметилформамиде при комнатной температуре гладко образуются 2-бром - и 2,5-дибромфураны.
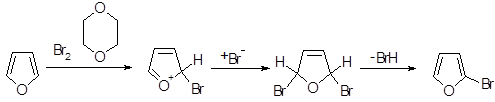
Ацилирование
Для ацилирования фуранов по Фриделю - Крафтсу ангидридами или галогенангидридами карбоновых кислот обычно необходимо присутствие кислоты Льюиса (часто трифторида бора), хотя реакция с ангидридом трифторуксусной кислоты не требует катализатора. Было показано, что при ацилировании фуранов в условиях катализа хлоридом алюминия α-положение проявляет реакционную способность, в 7 • 104 раз большую, чем реакционная способность β-положения. 3-Алкилфураны замещаются главным образом по положению 2; 2,5-диалкил фураны могут быть проацилированы по β-положению, хотя обычно большим трудом.
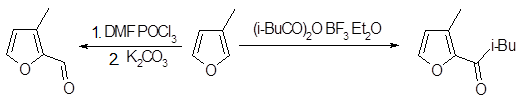
Формилирование фуранов по Вильсмейеру обеспечивает удобный подход к формилфуранам, хотя не меньшую роль играют легкая доступность фурфурола в качестве исходного материала, а также важны методы, включающие литиирование фуранов. Формилирование замещенных фуранов происходит согласно правилу предпочтительного образования α-замещенных производных, несмотря на все другие факторы; так, и 2-метилфуран, и метиловый эфир фуран-3-карбоновой кислоты дают 5-альдегид, а 3-метилфуран превращается главным образом в 2-альдегид.
2. Практическая часть
2.1 Пиримидин
Как известно, гетероароматические системы весьма отчетливо подразделяются на π-избыточные и π-дефицитные. Первым свойственны реакции электрофильного замещения, окисления, тогда как вторые реагируют главным образом с нуклеофилами, трудно окисляются, но сравнительно легко восстанавливаются. гетероароматическая система, обладающая одновременно свойствами π-избыточных и π-дефицитных соединений является перимидин, химическая амфотерность которого делает его интереснейшим объектом исследования.
2.1.1 Реакции электрофильного замещения
Перимидин является одним из наиболее активных по отношению к электрофильным агентам гетероциклов, что объясняется его высокой π-донорной способностью и большим отрицательным π-зарядом в орто-и пара-положениях нафталинового кольца. Именно по ним и протекают все реакции электрофильного замещения; до сих пор не известно случаев атаки электрофилами положений 5 и 8. Реакции электрофильного замещения в перимидинах очень чувствительны к стерическим помехам со стороны N-заместителя. Лишь небольшие по размерам частицы (D+, с большим трудом Сl+) могут вступать в положения 4 и 9 при наличии соседних N-метильных групп.
Ацилирование
Перимидин - единственная гетероароматическая система с пиридиновым атомом азота, подвергающаяся сравнительно легкому ацилированию по Фриделю — Крафтсу. Ацилирование лучше всего проводить с помощью карбоновых кислот в среде полифосфорной кислоты (ПФК). Для соединений с незамещенной группой NH реакция имеет ярко выраженный кинетический и термодинамический контроль. При 70—85° образуется главным образом 6(7)-ацилпроизводное (55—85%) наряду с небольшим количеством 9-изомера. При 120—150° единственным продуктом реакции становятся 4(9)-ацилперимидины. Одной из причин повышенной устойчивости последних является наличие в них прочной внутримолекулярной водородной связи.
Нитрование
В зависимости от количества и концентрации азотной кислоты перимидины нитруются (лучше всего в среде уксусной кислоты) до моно-, ди-, три- и тетранитропроизводиых, а ацеперимидины — до моно-и динитропроизводиых. Первое нитрование перимидинов со свободной группой NH сопровождается осмолением, что снижает выход. Так, перимидин нитруется действием 1 моля HNO3, образуя 4(9)- и 6(7)-нитропроизводные в соотношении 2,5 : 1 при общем выходе 30%.
Галогенирование
Хлорирование перимидинов, сульфурилхлоридом в уксусной кислоте и N-хлорбензотриазолом (ХБТ) в апротонной среде. Хлорирование перимидина действием моля SO2Сl2, приводит к образованию 6(7)- и 4(9)-хлорзамещенных в соотношении 8:1. При действии 2 молей SO2Сl2 образуется сложная смесь моно-, ди-и трихлорперимидинов, а 3 молей SO2Сl2 - 4,6,7-трихлорперимидии с высоким выходом. Получить с помощью SO2Сl2 тетрахлорперимидин не удалось, но 2-метилперимидин хлорируется избытком SO2Сl2 дотетра-хлорпроизводного.
