Биологическая функция нуклеиновых кислот
Явление, при котором последовательность оснований одной цепи однозначно определяет последовательность оснований другой цепи, получило название комплементарности. Таким образом, цепи молекул ДНК комплементарны по отношению друг к другу.
Сформулированный Уотсоном и Криком принцип комплементарности явился универсальным принципом в биологии. Он дал начало развитию новых научных направлений — молекулярной биологии, молекулярной генетике, генной инженерии. Водородные связи обеспечивают способ спаривания оснований, стабильность двухцепочечной системы. Основания плотно упакованы, причем расстояние между центрами оснований, лежащих друг над другом, равно 0,34 нм. На каждый полный виток двойной спирали приходится 10 нуклеотидных пар. Упакованные внутри двойной спирали основания гидрофобны и недоступны молекулам воды. Ионизированные фосфатные группы и гидрофильные остатки дезоксирибозы находятся на поверхности молекулы и контактируют с молекулами воды. Таким образом, двойная спираль стабилизирована не только водородными связями между комплементарными основаниями, но и гидрофобными взаимодействиями между основаниями, расположенными вдоль длинной оси молекулы ДНК. Из-за высокой степени упорядоченности макромолекул ДНК ее иногда называют апериодическим одномерным кристаллом.
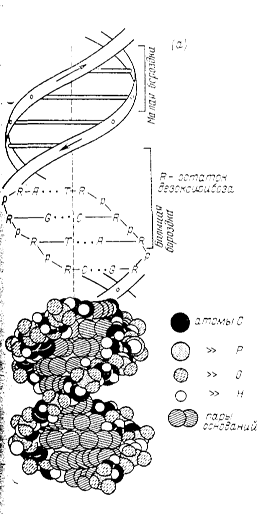
Рис.3 Макромолекулярная структура ДНК
При рентгенографическом исследовании головок сперматозоидов получается такая же дифракционная картина, что и для образцов ДНК, т.е. спираль Уотсона—Крика наблюдается непосредственно в живых клетках.
Модель строения ДНК в настоящее время является общепризнанной. За расшифровку структуры ДНК Дж. Уотсону, Ф. Крику и М. Уилкинсу в 1962 г. была присуждена Нобелевская премия.
Третичная структура ДНК образуется в результате дополнительного скручивания в пространстве двухцепочечной молекулы. Она имеет вид суперспирали или изогнутой (сломанной) двойной спирали.
В настоящее время описаны три формы структуры ДНК: А-, В- и Z-формы (рис.4). Параметры модели Уотсона—Крика соответствуют конформации ДНК в физиологических условиях (В-форме ДНК). Однако при изменении условий среды двойная спираль может принимать другие формы. Так при уменьшении влажности (в препарате образца для рентгеноструктурного анализа) ДНК переходит в А-форму. Этот переход связан с изменением конформации в остатках дезоксирибозы, уменьшением расстояния между фосфатными группами сахарофосфатного остова. Расстояние между парами нуклеотидов вдоль оси спирали, равное 0,34 нм в уотсон-криковской модели, уменьшается (примерно до 0,25 нм при 11 нуклеотидных остатках на один виток спирали). Диаметр спирали увеличивается; изменяются ширина и глубина бороздок; комплементарные пары азотистых оснований образуют с осью спирали угол 20° и, главное, они смещаются к периферии спирали. Поэтому двойная спираль похожа на пологую винтовую лестницу и внутри нее возникает полость диаметром 0,40 нм.
Переход молекулы ДНК из В- в А-форму можно осуществить при понижении активности воды в растворе (при внесении в него органического растворителя, например, этанола). Существует мнение, что В-форма представляет собой некую промежуточную форму двух или большего числа конформаций. Одной из особенностей В-формы, называемой В'-формой, является способность менять в молекуле ДНК положение двух цепей на обратное. Более того, В-форма может существовать в виде как правой, так и левой спирали.
Хотя более стабильными в А- и В-формах являются правозакрученные спирали, существуют довольно устойчивые и левозакрученные спирали ДНК. Одна из таких спиралей была получена в 1979 г. А. Ричем. Из-за нерегулярного зигзагообразного изгиба cахарофосфатного остова она была названа Z-формой (рис.4). Повторяющаяся единица в Z-форме ДНК включает две пары нуклеотидов, а не одну, как в В- и А-формах. Вследствие этого линия, соединяющая фосфатные группы, через каждые две пары нуклеотидов имеет излом и принимает зигзагообразный вид. По сравнению с В-формой в левой Z-форме резко изменен характер стэкинга оснований: сильные и слабые межплоскостные взаимодействия также чередуются. Z-форма может переходить в В-форму при снижении ионной силы раствора, добавлении этанола. Однако вопрос о существовании Z-формы ДНК in vivo и ее биологической роли до конца не выяснен. Высказывается мнение, что переход правозакрученной формы в левозакрученную может служить регуляторным сигналом, контролирующим экспрессию генов.
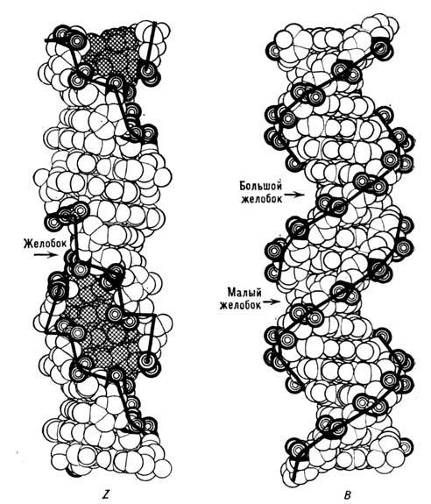
Рис.4. B- и Z-формы структуры ДНК
1.4. Физико-химические свойства ДНК
ДНК — довольно сильная многоосновная кислота, полностью ионизированная при рН 4,0. Фосфатные группы расположены по периферии. Они прочно связывают ионы Са![]() и Мg
и Мg![]() , амины, гистоны — положительно заряженные белки. Устойчивость комплементарных пар оснований зависит от величины рН. Пары оснований наиболее устойчивы в интервале рН 4,0—11,0. За его пределами двухцепочечная спираль ДНК теряет устойчивость и раскручивается.
, амины, гистоны — положительно заряженные белки. Устойчивость комплементарных пар оснований зависит от величины рН. Пары оснований наиболее устойчивы в интервале рН 4,0—11,0. За его пределами двухцепочечная спираль ДНК теряет устойчивость и раскручивается.
Молекулярная масса ДНК неодинакова и зависит от источника ее получения. К тому же даже при самых тщательных и щадящих процедурах выделения ДНК подвергается некоторой деградации. Препараты, полученные современными методами из тканей животных и растений, имеют молекулярную массу 6 10![]() —10 10
—10 10![]() . Однако истинная молекулярная масса ДНК животных и растений, определенная по вязкости и по длине молекул, значительно выше и достигает десятков миллиардов.
. Однако истинная молекулярная масса ДНК животных и растений, определенная по вязкости и по длине молекул, значительно выше и достигает десятков миллиардов.
У большинства вирусов ДНК представляет собой двойную спираль, линейную или замкнутую в кольцо. У некоторых вирусов она представляет собой одну полинуклеотидную цепь, замкнутую в кольцо и имеющую сравнительно небольшую молекулярную массу — 2 10![]() . ДНК сравнительно легко деполимеризуется под действием некоторых химических соединений, ультразвука, ионизирующей и ультрафиолетовой радиации. Нагревание растворов ДНК до температур 70—80 °С, а также их подщелачивание вызывают денатурацию ДНК, заключающуюся в плавлении двойной спирали (разрушение водородных связей и гидрофобных взаимодействий), и расхождение полинуклеотидных цепей. Денатурация сопровождается понижением вязкости раствора, повышением поглощения в ультрафиолетовой области, увеличением отрицательного удельного вращения плоскости поляризации света, увеличением плавучей плотности образцов ДНК. Возрастание светопоглощения света при 260 нм называется гипохромным эффектом; это важнейший критерий денатурации ДНК, по которому можно контролировать этот процесс.
. ДНК сравнительно легко деполимеризуется под действием некоторых химических соединений, ультразвука, ионизирующей и ультрафиолетовой радиации. Нагревание растворов ДНК до температур 70—80 °С, а также их подщелачивание вызывают денатурацию ДНК, заключающуюся в плавлении двойной спирали (разрушение водородных связей и гидрофобных взаимодействий), и расхождение полинуклеотидных цепей. Денатурация сопровождается понижением вязкости раствора, повышением поглощения в ультрафиолетовой области, увеличением отрицательного удельного вращения плоскости поляризации света, увеличением плавучей плотности образцов ДНК. Возрастание светопоглощения света при 260 нм называется гипохромным эффектом; это важнейший критерий денатурации ДНК, по которому можно контролировать этот процесс.
В отличие от многих глобулярных белков, денатурация которых происходит постепенно в широком температурном интервале, нативные ДНК денатурируют в узком интервале температур (~10 °С), поэтому тепловую денатурацию часто называют плавлением. Температура плавления тем выше, чем больше в молекуле ДНК GС-пар; этот показатель может использоваться для определения нуклеотидного состава ДНК. Установлено, что температура плавления линейно связана с составом ДНК: ее повышение на 1° соответствует 2,5 молярных % GС-пар. Гомогенные препараты ДНК характеризуются плавлением с резким переходом спираль—клубок, тогда как гетерогенные препараты дают сравнительно широкую зону плавления, что может служить мерой гетерогенности ДНК. При быстром охлаждении после тепловой денатурации ДНК не восстанавливает своих нативных свойств; однако, при медленном охлаждении полинуклеотидные цепи реассициируются по принципу комплементарности, т.е. происходит ренатурация молекул ДНК. Это продемонстрировано, в частности, на препаратах ДНК пневмококка с помощью методов электронной микроскопии и градиентного ультрацентрифугирования в СsСl.
