Исследование соотношения в мышцах С- и Х-белков в норме и при патологии
Результаты электронно-микроскопических исследований представлены на рис. 9–14. Мы показали, что в растворе, содержащем 30 мМ KCl, 10 мМ имидазола, рН 7.0 Х-белок образует спирально скрученные ленточные фибриллы с осевой периодичностью ~60–70 нм, шириной ~40 нм и длиной более 1 мкм (рис. 9 А). Мы обнаружили, что такие же структуры Х-белок образует и в растворе, содержащем 0.15 М глицин-КОН, рН 7.5 (рис. 9 Б). Кроме этого Х-белок, а также С-белок и Н-белок образуют аморфные агрегаты, протофибриллы, линейные фибриллы и пучки линейных фибрилл в растворах: 50 мM NaCl, 10 мM Hepes, pH 7.0; 25 мМ NaCI, 10 мМ Hepes, pH 7.0; 50 мM MgCl2, 10 мM имидазола, pH 7.0; 30 мМ MgCI2, 10 мМ имидазола, pH 7.0; 0.15 М глицин-KOH, рН 7.5 (рис. 10–13).
На рис. 14 представлены электронные микрофотографии пучка линейных фибрилл тайтина скелетных мышц кролика в растворе 0.15 М глицин-KOH, рН 7.5. В этих условиях тайтин образует плотные пучки линейных фибрилл длиной ~3 мкм, шириной до 500 нм и аморфные агрегаты. Мы наблюдали, что аморфные агрегаты, протофибриллы длиной 100–200 нм и диаметром ~3 нм, линейные фибриллы диаметром ~7 нм и пучки линейных фибрилл длиной более 3 мкм и шириной до 500 нм могут присутствовать в одном и том же образце. Это, по-видимому, отражает разные стадии фибриллогенеза, характерные для формирования амилоидов (Kelly, 1998; Chiti et al., 1999; Goldsbury et al., 2000).
Для подтверждения амилоидной природы фибрилл тайтина, Х-белка, С-белка и Н-белка наши дальнейшие исследования были направлены на сравнение агрегатов, образуемых белками семейства тайтина, с агрегатами известных амилоидогенных белков и, в частности, Аβ-пептида, играющего важную роль в патогенезе болезни Альцгеймера.
4.2. Электронно-микроскопическое изучение агрегационных свойств Аβ(25-35)-пептида в сравнении с агрегацией молекул Х-белка
Для сравнения спирально скрученных фибрилл Х-белка с другими амилоидными фибриллами мы изучили агрегационные свойства Аβ(25-35)-пептида. Мы показали, что Аβ(25-35)-пептид, инкубированный в течение 24 ч при 37˚С образует подобно Х-белку (рис. 15 А) спирально скрученные ленты несколько микрон длиной и диаметром 25–27 нм с вариабельным осевым периодом 170–250 нм (рис. 15 Б, В).
Ленты построены из нескольких длинных и узких фибрилл диаметром 3–5 нм. На микрофотографиях они лучше видны, если смотреть вдоль ленты. Обнаруживаются также листовые агрегаты (рис. 15 Г), сформированные за счет боковой агрегации более коротких узких фибрилл. Такие агрегаты достигают в ширину ~50 нм. Таким образом, с помощью электронной микроскопии нами было установлено морфологическое сходство фибрилл Х-белка с амилоидами Aβ-пептида, найденными в мозге при болезни Альцгеймера.
4.3. Подтверждение амилоидной природы агрегатов, образуемых белками семейства тайтина (тайтина, Х-белка, С-белка и Н-белка) при их взаимодействии со специфическими красителями на амилоиды
Конго красным и тиофлавином Т
Основным методом выявления амилоидной природы фибрилл, образуемых разными белками, является их способность взаимодействовать со специфическими красителями Конго красным и тиофлавином Т (Klunk et al., 1989; LeVine, 1993, 1995; Krebs et al., 2005). Именно эти красители используют в клинической практике для определения амилоидных отложений in vivo и для исследования амилоидогенеза in vitro разными белками.
При окрашивании Конго красным фибриллярных структур, формируемых исследуемыми белками, мы наблюдали двойное лучепреломление в поляризационном микроскопе, а при окрашивании их тиофлавином Т – желто-зеленую флуоресценцию в люминесцентном микроскопе. На рис. 16 представлены данные связывания Х-фибрилл, сформированных в растворе, содержащем 30 мМ KCl, 10 мМ имидазола, рН 7.0, с красителями Конго красным и тиофлавином Т.
При спектральных исследованиях интенсивность флуоресценции тиофлавина Т в присутствии фибрилл Х-, Н- и С-белков и тайтина возрастала в ~10, ~9, ~7 и ~5 раз соответственно по сравнению с интенсивностью флуоресценции красителя в присутствии этих белков в молекулярной форме (рис. 17). Незначительное увеличение интенсивности флуоресценции тиофлавина Т наблюдается и в присутствии молекулярных форм тайтина, Х-, С- и Н-белков, что согласуется с литературными данными для белков, содержащих β-складчатую структуру (LeVine, 1993; 1995).
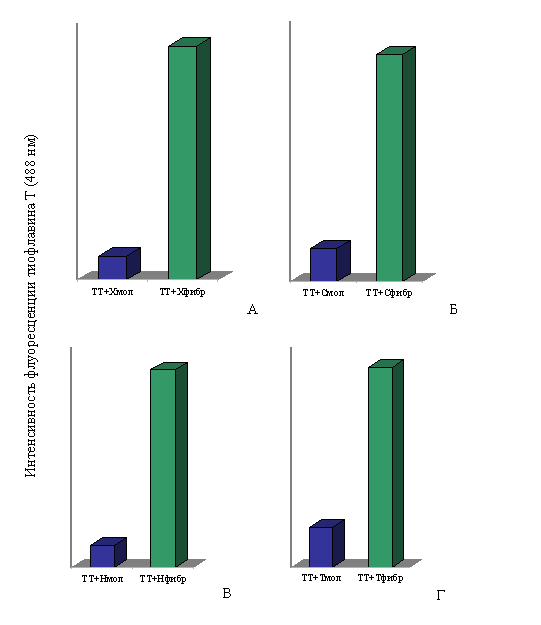
Рис. 17. Интенсивность флуоресценции тиофлавина Т (TT): А – в присутствии молекулярного X-белка (в растворе, содержащем 0.3 M KCl, 10 мМ К-фосфат, рН 7.0) и в присутствии фибрилл X-белка (0.15 М глицин-KOH, рН 7.5); Б – в присутствии молекулярного С-белка (0.3 M KCl, 10 мМ К-фосфат, рН 7.0) и в присутствии фибрилл С-белка (0.15 М глицин-KOH, рН 7.5); В – в присутствии молекулярного Н-белка (0.3 M KCl, 10 мМ К-фосфат, рН 7.0) и в присутствии фибрилл Н-белка (0.15 М глицин-KOH, рН 7.5); Г – в присутствии молекулярного тайтина (0.6 М KCl, 30 мМ KH2PO4, рН 7,0) и в присутствии фибрилл тайтина (0.15 М глицин-KOH, рН 7.5). Молярное соотношение красителя и белка 1:2.
При измерении спектральных характеристик раствора Конго красного в присутствии фибрилл тайтина, Х-, С- и Н-белков наблюдался сдвиг спектра поглощения красителя в длинноволновую область от ~490 нм к ~500 нм (рис. 18), что также является характерной чертой при связывании амилоидных фибрилл с Конго красным (Klunk et al., 1989).
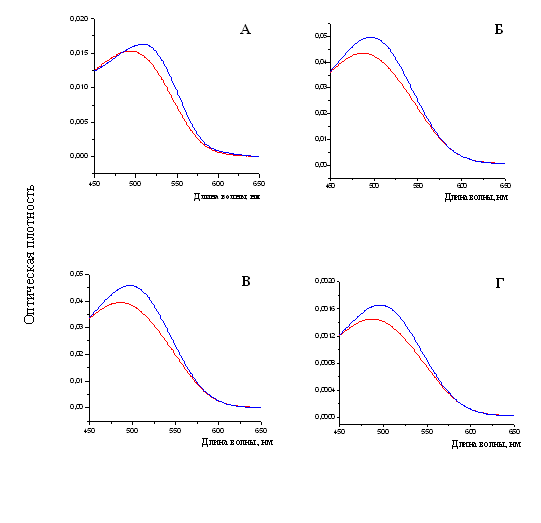
Рис. 18. Спектры поглощения свободного красителя показаны линиями красного цвета. Спектры поглощения красителя Конго красного (линия синего цвета): А – в присутствии фибрилл X-белка (в растворе, содержащем 0.15 М глицин-KOH, рН 7.5); Б – в присутствии фибрилл С-белка (0.15 М глицин-KOH, рН 7.5); В – в присутствии фибрилл Н-белка (0.15 М глицин-KOH, рН 7.5); Г – в присутствии фибрилл тайтина (0.15 М глицин-KOH, рН 7.5). Молярное соотношение красителя и белка 1:2.
Проведенные исследования указывают на специфичность связывания красителей с фибриллярными агрегатами, образуемыми белками семейства тайтина, подтверждая их амилоидную природу.
4.4. Изучение вторичной структуры тайтина и белков его семейства до и после образования амилоидных фибрилл
В работах по изучению образования амилоидных фибрилл белками in vitro используется длительная икубация и условия, несовместимые с условиями in vivo (денатурирующие вещества, низкие значения рН, высокие температуры, добавление ряда веществ, не присутствующих в клетке и т.п.) (Stine et al., 2003). Как известно, эти условия приводят к трансформации структуры молекулы белка с образованием β-складчатости, характерной для амилоидных фибрилл. (Juzczyk et al., 2005). Согласно литературным данным (Labeit & Kolmerer, 1995; Weber et al., 1993; Vaughan et al., 1993), молекулы белков семейства тайтина уже содержат β-складчатую структуру. Нами были проведены исследования вторичной структуры белков до и после образования ими амилоидных фибрилл. Как показано на рис. 20 молекулярные и фибриллярные формы Х-, С- и Н-белков характеризуются сходными спектрами кругового дихроизма (КД). Форма спектров фибрилл свидетельствует в пользу того, что в их составе практически отсутствуют α-спиральные участки, а преобладающими элементами являются β-складки. Молекулярная форма тайтина содержит ~10% α-спирали. После образования амилоидных фибрилл молекула тайтина содержит только β-структуру (рис. 19).
