Экспериментальные термометрические шкалы и методы измерения температур
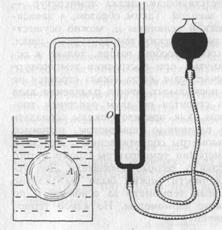
рис. 1
Газовый термометр представляет собой стеклянный, кварцевый или металлический баллон неизменного объема, заполненный реальным газом и соединённый с помощью капилляра с манометром. Уровень ртути в левом колене манометра доводится до отметки О, чтобы обеспечить постоянство объёма газа. В качестве рабочего раза раньше употреблялся водород. Сейчас же в основном употребляется гелий (для измерения низких и средних температур) и азот (для измерения высоких температур, где гелий не пригоден, т.к. он легко диффундирует сквозь стенки баллона). Давление газа измеряется по манометру, и затем, по этому давлению вычисляется температура с учётом поправок на изменение объёма баллона, неидеальность газа и пр.
Несмотря на кажущуюся простоту измерение температуры с помощью газового термометра – нелёгкая экспериментальная работа, требующая от экспериментатора особой тщательности. Поэтому в повседневной жизни пользуются другими типами термометров. Идеально – газовым термометром пользуются в исключительных случаях, когда нужна высокая точность измерения температуры.
Интервал, измеряемых газовым термометром, температур ограничен. Это связано с тем, что все реальные газы при очень низких температурах конденсируются и далее уже не подчиняются закону Бойля – Мариотта. Точно также при очень высоких температурах молекулы газа начинают диссоциировать (распадаться) на электроны и положительно заряженные ионы и также перестают подчиняться закону Бойля – Мариотта.
Но всё же там, где пригодна газовая шкала, она практически не отличается от шкалы Кельвина. Поэтому в интервале температур от 4 К до 1338 К абсолютная термодинамическая шкала осуществляется именно с помощью газового термометра.
Газовая шкала, хотя и слабо, но всё же зависит от природы рабочего газа. Рациональная температурная шкала не должна зависеть от свойств термометрического вещества. Этим требованиям удовлетворяет абсолютная термодинамическая шкала Кельвина. Хотя она и не относится к экспериментальным шкалам, но она так важна в физике, что я посчитал необходимым упомянуть и её.
Термодинамическая абсолютная шкала Кельвина.
В 1848 г. Вильям Томсон (лорд Кельвин) указал, что теоремой Карно можно воспользоваться для построения рациональной температурной шкалы, совершенно не зависящей от индивидуальных особенностей термометрического вещества и устройства термометра.
Из теоремы Карно следует, что КПД цикла Карно может зависеть только от температур нагревателя и холодильника. Обозначим буквами t1 и t2 эмпирические температуры нагревателя и холодильника, измеренные каким-либо термометром (например, газовым, ртутным, термометром сопротивления и т. п.). Тогда
![]()
где f(t1, t2) — универсальная функция выбранных эмпирических температур t1 и t2. Ее вид совершенно не зависит от устройства машины Карно и от рода используемого рабочего вещества. Этим обстоятельством и воспользовался Вильям Томсон, предложивший применить цикл Карно для построения температурной шкалы.
Чтобы построить термодинамическую шкалу температур, введем более простую универсальную функцию температур t1 и t2:
![]()
Эта функция легко выражается через прежнюю функцию f(t1,, t2). Определим общий вид функции φ(t1,, t2). С этой целью возьмем три тепловых резервуара, температуры которых поддерживаются постоянными. Эмпирические температуры этих резервуаров обозначим через t1, t2, t3 соответственно. Используя их в качестве нагревателей и холодильников, проведем три цикла Карно, изображенные на рис. 26.
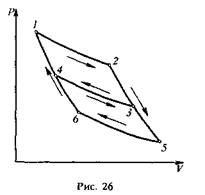
Предполагается, что t1, t2, t3 — температуры на изотермах 12, 43, 65. Для циклов Карно 1234 и 4356 можно написать
![]()
Исключив отсюда теплоту Q2, получим
![]()
Но эти два цикла, объединенные вместе по схеме рис. 26, эквивалентны одному циклу Карно 1256. Это
происходит потому, что по изотерме 43 мы проходим дважды в противоположных направлениях, и она может быть исключена из рассмотрения. Следовательно,
![]()
Сравнивая это соотношение с предыдущим, получим
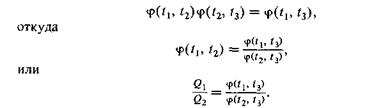
Такое соотношение справедливо при любом значении аргумента t3. Левая часть его не зависит от значения температуры t3. Поэтому и отношение в правой части не может меняться с изменением t3. Можно фиксировать t3 , не меняя значения самого отношения. Но тогда числитель в правой части формулы (31.5) будет функцией одного только аргумента t1. Обозначим эту функцию через Θ(t1). Знаменатель будет такой же функцией, но от аргумента t2.
Итак,
![]()
Таким образом, φ(t1,, t2) есть отношение значений одной и той же функции Θ (t). Так как величина Θ(t) зависит только от температуры, то она сама может быть принята за меру температуры тела. Величину Θ(t) и называют абсолютной термодинамической температурой. Отношение двух термодинамических температур Θ1 ≡ Θ1(t) и Θ2 ≡ Θ2(t) определяется соотношением
![]()
3. Отношение Θ1/ в принципе может быть найдено экспериментально. Для этого надо измерить теплоты Q1 и Q2. Однако значением этого отношения сами температуры Θ1, Θ2 и еще не определяются однозначно. Это видно также из того, что функция Θ(t) = φ( t1,, t2) зависит от параметра t3, которому можно придать произвольное значение. Отношение не зависит от параметра t3. Однако сами термодинамические температуры будут иметь разные значения при различном выборе этого параметра. Вместо функции Θ (t) можно было бы в качестве термодинамической температуры принять, например, величину Θ' (t) = ψ(t3)Θ(t), где ψ(t3) — произвольная функция. От этого значение отношения не изменилось бы. Но, придавая параметру t3 различные значения, мы получили бы бесконечное множество температурных шкал, отличающихся друг от друга масштабами единицы температуры. Чтобы однозначно определить термодинамическую температуру Θ, можно поступить двояко.
Во-первых, можно взять какие-либо две постоянные температурные точки, например нормальную точку плавления льда и нормальную точку кипения воды. Обозначим термодинамические температуры этих точек Θп и, а соответствующие им количества теплоты в цикле Карно — Qп и Qк. Фиксируем далее значение разности Θп - Θк , например примем, что она равна 100 градусам. Тогда температурный интервал между нормальными точками плавления льда и кипения воды разделится на 100 равных частей, каждая из которых ранее называлась градусом Кельвина, а теперь — просто Кельвином. Из двух уравнений
