Получение оксидов уранаРефераты >> Технология >> Получение оксидов урана
Диоксид урана UO2 (точнее, UO2±Х) – вещество темно-коричневого цвета с кристаллической структурой типа CaF2. Это нестехиометрическое соединение может иметь состав от UO1,6 до UO2,25, причем дополнительные (сверх стехиометрии) атомы кислорода удерживаются в промежутках кристаллической решетки в результате внедрения атомов кислорода в решетку UO2 типа флюорита.
Диоксид урана может быть получен восстановлением триоксида или U3O8 водородом или оксидом углерода при 500–600°С. Он образуется также при окислении урана на воздухе при 150 –170°С. Это – основной оксид, которому соответствует основной гидроксид U(OH)4. Диоксид урана термодинамически устойчив при нагревании в вакууме или в восстановительной атмосфере до 1600°С и возгоняется без разложения. При более высокой температуре он теряет кислород с образованием достехиометрического диоксида. В присутствии кислорода UO2 способен растворять его в себе с сохранением кубической структуры, образуя фазу UO2+x, где х зависит от температуры.
Диоксид урана не реагирует с водой и ее парами до 300°С, нерастворима в соляной кислоте, но растворима в азотной кислоте, царской водке и смеси HNO3 и HF. При растворении в азотной кислоте происходит образование уранил-ионов UO22+. Известен один кристаллогидрат диоксида урана UO2.2H2O – черный осадок, выпадающий при гидролизе растворов урана (IV). Диоксид урана входит в состав уранового минерала уранинита.
Оксиды U4O9 и U3O7 образуют самостоятельные фазы нестехиометрического состава. Для оксида U3O7 характерно наличие метастабильных тетрагональных фаз. Существует по крайней мере пять таких фаз, которые при температуре выше 600°С распадаются с образованием соответственно UO2 и U4O9 или U4O9 и UO2,6. При температуре выше 600°С в системе U–O в области от U4O9 до U3O8 исчезают все метастабильные тетрагональные оксиды, и в равновесии находятся фаза U4O9 и фаза с ромбической структурой закиси-окиси.
Закись-окись урана U3O8 – нестехиометрическое соединение, имеющее несколько модификаций в зависимости от условий приготовления. Цвет вещества – от зеленого до оливково-зеленого и черного. Закись-окись образуется при окислении на воздухе диоксида урана и при прокаливании на воздухе до красного каления (650–900°С) любого оксида урана, гидрата оксида или соли урана и летучего основания или кислоты.
Оксид U3O8 рассматривают иногда как UO2 . 2UO3 на основании того, что при растворении его в растворе присутствуют U4+ и 2UO22+. Однако доказано, что все атомы урана в U3O8 структурно эквивалентны и несут равный средний положительный заряд ![]() .
.
Закись-окись урана нерастворима в воде и разбавленных кислотах, но медленно растворяется в концентрированных минеральных кислотах с образованием смеси солей урана и уранила. В HCl и H2SO4 образуется смесь урана в степенях окисления четыре и шесть, а в HNO3 – только уранил-ион. При неполном растворении U3O8 в серной кислоте образуется U2O5, которая не получается при восстановлении оксидов урана водородом при нагревании. Закись-окись имеет гидрат U3O8 . xH2O, который не кристаллизуется и очень легко окисляется до гидрата триоксида урана. Значение триоксида велико и потому, что она входит в состав смоляной руды – настурана.
Триоксид урана UO3 – один из промежуточных продуктов в производстве чистых солей урана, встречающихся также в некоторых окисленных урановых рудах.
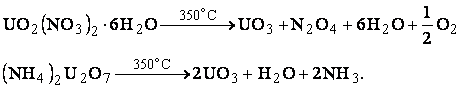 |
Триоксид урана амфотерен: с кислотами он образует соли уранила, например, UO2SO4, со щелочами – соли урановой кислоты, например, Na2U2O7. Известно несколько кристаллогидратов триоксида урана, которые можно рассматривать как кислоты.
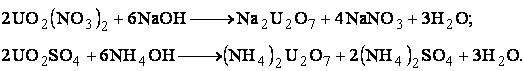 |
Пероксид урана UO4 . nH2O существует только в форме гидратов с 2, 3, 4 и 4,5 молекулами воды. Его можно представить как комплекс UO2(O2)x xnH2O. Он может быть получен действием пероксида водорода на соединения UVI и UIV в азотнокислом растворе. Пероксид урана – нерастворимое соединение, с помощью которого уран можно отделить от всех элементов, кроме тория, плутония, нептуния, циркония и гафния. Пероксид урана обладает кислотными свойствами. [1,2]
Технологическая характеристика оксидов урана
Оксиды урана имеют весьма важное значение в технологии производства ядерного горючего. В некоторых типах гетерогенных ядерных реакторов основой тепловыделяющих элементов (ТВЭЛов) является диоксид урана, который обладает высокой коррозионной и радиационной устойчивостью. Его огнеупорность дает возможность получать в ядерных реакторах очень высокие температуры и увеличивать тем самым коэффициент полезного действия. Кроме того, совместимость диоксида урана с различными материалами оболочки и его высокая плотность также с положительной стороны характеризуют этот вид ядерного горючего.
Из диоксида урана ТВЭЛы могут быть изготовлены в виде брусков, трубок, таблеток и т. д. обычными методами керамической технологии: холодным прессованием и выдавливанием с последующим спеканием изделий или горячим прессованием. В виде порошка диоксид урана диспергируется в металлических, графитовых или керамических матрицах.
Но, пожалуй, еще большее значение оксиды урана имеют как промежуточные продукты при производстве других соединений урана и главным образом фторидов. Наконец, нельзя не отметить, что оксиды урана как наиболее устойчивые его соединения могут быть использованы для целей хранения урана и послужить промежуточным звеном между урановорудным, аффинажно-металлургическим и фторидными производствами.
В связи с указанными выше областями применения оксидов урана к ним предъявляются совершенно определенные требования. Необходимо, чтобы оксиды урана были кондиционными по содержанию примесей. В том случае, если имеется в виду самостоятельное применение оксидов урана в гомогенных или гетерогенных ядерных реакторах, содержание примесей в них должно быть весьма малым, соответствующим требованию ядерной чистоты продуктов (табл. 2).
Таблица 2. Спецификация ядерно-чистого диоксида урана,
