Анализ азота и его соединений
Колориметрическое определение
с фенолдисульфоновой кислотой.
Определение основано на образовании желтого соединения в результате реакции нитратов с фенолдисульфоновой кислотой. Без разбавления этим методом можно определять от 0,5 до 50 мг ![]() в 1 л воды.
в 1 л воды.
При концентрации ![]() 2-50 мг1л и отсутствии мешающих влияний точность определения ±0,5 мг!л.
2-50 мг1л и отсутствии мешающих влияний точность определения ±0,5 мг!л.
Мешающие влияния. Определению мешают хлориды. Концентрация их в пробе не должна превышать 10 мг/л. Уменьшить их концентрацию можно соответствующим разбавлением. Мешающее влияние хлоридов можно также устранить добавлением сульфата серебра (см. ниже). Однако при анализе некоторых вод избыток ионов серебра вызывает окрашивание раствора или образование мути. Для подщелачивания пробы применяют едкое кали или аммиак.
Если для осаждения хлоридов был применен сульфат серебра, то подщелачивать раствор едким кали нельзя, так как этот реактив вызывает коричневое окрашивание; вместо него следует применять раствор аммиака.
При содержании нитритов, превышающем 0,7 мг/л, получаются повышенные результаты. Окрашенные соединения не должны присутствовать.
Удаление хлоридов. Определяют в пробе содержание хлоридов. К 100 мл пробы прибавляют эквивалентное количество раствора сульфата серебра (4,40 г Ag2SO4 ч. д. а., свободного от нитритов, растворяют в дистиллированной воде и доводят объем до 1 л, 1 мл раствора соответствует 1 мг ![]() ). Осадок хлорида серебра отфильтровывают или отделяют центрифугированном после предварительного нагревания смеси. Целесообразно оставить смесь на ночь в темноте.
). Осадок хлорида серебра отфильтровывают или отделяют центрифугированном после предварительного нагревания смеси. Целесообразно оставить смесь на ночь в темноте.
Удаление окраски. К 150 мл пробы прибавляют 3 мл суспензии гидроокиси алюминия (125 г сульфата алюминия и калия или сульфата алюминия и аммония растворяют в 1 л дистиллированной воды, нагревают до 60° С и постепенно прибавляют 55 мл концентрированного раствора аммиака при постоянном перемешивании. После отстаивания в течение 1 ч осадок переносят в большой стакан и промывают декантацией дистиллированной водой до исчезновения свободного аммиака, хлоридов, нитритов и нитратов), тщательно перемешивают, оставляют стоять несколько минут и фильтруют. Первые порции фильтрата отбрасывают.
Окисление нитритов. К 100 мл пробы прибавляют 1 мл 1 н. раствора H2SO4 и перемешивают. Затем по каплям прибавляют при перемешивании необходимое количество 0,1 н. раствора перманганата калия или 3%-нога раствора перекиси водорода. Перманганат добавляют в таком количестве, чтобы розовая окраска не исчезала в течение не менее 15 мин. Поскольку окисление нитритов приводит к образованию нитратов, надо из результата определения последних вычесть количество нитритов, присутствовавших в первоначальной пробе (в пересчете на нитраты). Содержание нитритов определяют в отдельной порции пробы соответствующим методом.
Аппаратура
Фотометр с фиолетовым (синим) светофильтром ( ![]() = 410 нм). Кюветы с толщиной слоя 1-5 см или набор цилиндров Несслера емкостью 50 или 100 мл. Для повышения верхнего предела определяемой концентрации можно производить измерения и при других длинах волн, например 480 нм.
= 410 нм). Кюветы с толщиной слоя 1-5 см или набор цилиндров Несслера емкостью 50 или 100 мл. Для повышения верхнего предела определяемой концентрации можно производить измерения и при других длинах волн, например 480 нм.
Реактивы
Фенолдисульфоновая кислота, раствор в серной кислоте. Растворяют 25 г фенола ч. д. а, (препарат не должен быть окрашен) в 150 мл концентрированной серной кислоты. Прибавляют 75 мл дымящей серной кислоты (олеум с 15% SO3), тщательно перемешивают и нагревают с обратным холодильником в течение 2 ч на кипящей водяной бане.
Аммиак ч. д. а., концентрированный раствор.
Едкое кали, приблизительно 12 н. раствор. Растворяют 673 г КОН ч. д. а. в дистиллированной воде и доводят до 1 л.
Комплексон III, аммиачный раствор. Растирают 50 г комплексона III с 20 мл дистиллированной воды до получения пасты, которую растворяют в 50 мл концентрированного раствора аммиака.
Нитрат калия, стандартный раствор. Растворяют 0,1631 г KNOз ч. д. а., высушенного при 105°С, в дистиллированной воде, прибавляют 1 мл хлороформа и доводят водой до 1 л; 1 л содержит 0,100 м ![]() .
.
Калибровочная кривая. На водяной бане выпаривают досуха 50,0 мл стандарт кого раствора. Сухой остаток растворяют в 2,0 мл кислого раствора фенолсульфоновой кислоты и доводят дистиллированной водой до 100 мл.
Для визуального колориметрирования, проводимого в цилиндрах Несслера, в несколько цилиндров емкостью по 50 мл отмеривают 0,1; 0,3; 0,5; 0,7; 1,0, 2,0. 5,0; 10, 15; 20 и 30 мл окрашенного стандартного раствора (что отвечает 0; 0,1; 0,3; . . .I 30 мг ![]() в 1 л), прибавляют 2,0 мл раствора фенолдисульфоновой кислоты и такое же количество раствора NH4OH или КОН, какое прибавлялось в пробе.
в 1 л), прибавляют 2,0 мл раствора фенолдисульфоновой кислоты и такое же количество раствора NH4OH или КОН, какое прибавлялось в пробе.
Объем раствора в цилиндрах доводят дистиллированной водой до метки и перемешивают Приготовленные таким способом окрашенные стандарты для сравнение могут сохраняться несколько недель без изменения окраски.
Для построения калибровочного графика используют оптические плотности. окрашенных стандартов, приготовленных, как указано выше при описании визуального колориметрирования. Из найденных значений вычитают оптическую плотности холостой пробы. Строят график зависимости оптической плотности от концентрации нитрат-ионов.
Ход определения. Прозрачную пробу объемом 100 мл или менее с содержанием не более 5 мг ![]() нейтрализуют до рН 7, переливают в фарфоровую чашку и выпаривают на кипящей водяной бане досуха. К сухому остатку прибавляют 2,0 мл раствора фенолдисульфоновой кислоты и размешивают стеклянной палочкой до полного растворения. Если потребуется, смесь слегка нагревают на водяной бане. Прибавляют 20 мл дистиллированной воды и приливают при помешивании 6-7 мл концентрированного раствора аммиака или 5-6 мл 12 н. раствора едкого кали. Если при этом выделяются гидроокиси присутствующих металлов, их удаляют фильтрованием через стеклянный фильтр или прибавляют по каплям аммиачный раствор комплексона III до полного растворения осадка. Фильтрат или прозрачный раствор переносят в мерную колбу емкостью 50 или 100 мл, доводят дистиллированной водой до метки и содержимое колбы перемешивают. Окрашенный раствор колориметрируют. Из найденного значения вычитают оптическую плотность холостого раствора (дистиллированная вода с реактивами) и по калибровочному графику находят содержание нитрат-ионов.
нейтрализуют до рН 7, переливают в фарфоровую чашку и выпаривают на кипящей водяной бане досуха. К сухому остатку прибавляют 2,0 мл раствора фенолдисульфоновой кислоты и размешивают стеклянной палочкой до полного растворения. Если потребуется, смесь слегка нагревают на водяной бане. Прибавляют 20 мл дистиллированной воды и приливают при помешивании 6-7 мл концентрированного раствора аммиака или 5-6 мл 12 н. раствора едкого кали. Если при этом выделяются гидроокиси присутствующих металлов, их удаляют фильтрованием через стеклянный фильтр или прибавляют по каплям аммиачный раствор комплексона III до полного растворения осадка. Фильтрат или прозрачный раствор переносят в мерную колбу емкостью 50 или 100 мл, доводят дистиллированной водой до метки и содержимое колбы перемешивают. Окрашенный раствор колориметрируют. Из найденного значения вычитают оптическую плотность холостого раствора (дистиллированная вода с реактивами) и по калибровочному графику находят содержание нитрат-ионов.
Расчет. Содержание нитрат-ионов в мг/л (х) или в мг-екв/л (у) вычисляют по формулам:
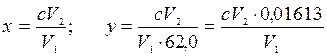
где с - концентрация нитрат-ионов, найденная по калибровочному графику или по шкале стандартов, мг/л; V1 - объем пробы, взятой для анализа, мл; V2 - объем окрашенной пробы, мл (50 или 100 мл); 62,0 - эквивалент ![]() .
.
