Изучение возможности применения магнитных жидкостей для синтеза магнитных сорбентов
Обычно получение устойчивых магнитных жидкостей ведется при совокупности методов конденсации, диспергирования и пептизации.
Эти методы широко используются в технике для получения красок, пигментов, магнитных лент и т.д. Использование этих методов для производства магнитных жидкостей будет обусловлено рядом дополнительных требований, таких как:
- возможность получения ферромагнетиков с размерами частиц 50-200Å;
- возможно больший выход частиц ферромагнетиков без загрязнения и разложения,
- простота технической реализации метода,
- высокие адсорбционные свойства частиц ферромагнетика и хорошо развитая поверхность;
- хорошая устойчивость получаемых коллоидов.
Среди этих методов нужно прежде всего выделить метод получения МЖ на основе магнетита путем соосаждения его избытком щелочи из растворов солей двух- и трехвалентного железа и последующей пептизации в жидкости-носителе.
Принципиальная схема процесса представлена на рис. 5. В реакторе I соли двух- и трехвалентного железа осаждаются избытком аммиака, затем в реакторе 2 к полученному осадку магнетита при постоянном перемешивании и нагревании до 70-90°С добавляют раствор олеиновой кислоты в керосине. В реакторах 3 и 4 происходит разделение полученной магнитной жидкости от воды и растворимых солей. Для более полного отделения магнитной жидкости от воды и примесей использован магнит 4.
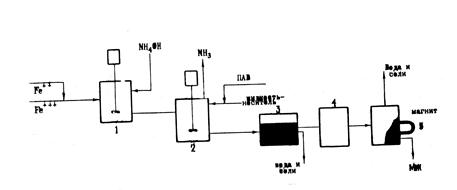
Рис.5. Технологическая схема процесса получения МЖ.
Описанный способ получения МЖ прост, производителен, позволяет получать магнетит размером 30-100Å, а магнитные жидкости - хорошей устойчивости и высокой намагниченности.
Выше рассмотрены наиболее изученные и отработанные методы получения МЖ. Но нужно отметить, что не всегда эти методы позволяют получить МЖ с широким диапазоном свойств на требуемой основе. Весьма перспективным в этом отношении является способ замены в МЖ одной жидкости-носителя другой, предложенный Р.Розенцвайгом [78] и основанный на методе пептизации. Суть этого способа состоит в том, что в МЖ вводят полярный флокулирующий агент или полимер, вызывающий флокуляцию частиц с адсорбированным на них ПАВом. В дальнейшем стабилизированные частицы выделяют из раствора и пептизируют в другой жидкости-носителе. Механизм действия флокулирующего агента приведен на рис. 6. Нa этом рисунке изображены две соседние частицы с адсорбированным на их поверхности ПАВом, взвешенные в неполярной жидкости-носителе. Когда две частицы сближаются, адсорбированные слои за счет стерического отталкивания препятствуют их укрупнению, и, естественно, и коагуляции. В силу этого частицы равномерно распределены в жидкости-носителе. При введении в систему полярного флокулирующего агента уменьшается взаимодействие ПАВ с жидкостью-носителем. Это приводит к вытеснению жидкости-носителя из зазоров между частицами и коагуляции последних с адсорбированным на них ПАВом. Скоагулировавшиеся частицы могут быть диспергированы в другой жидкости-носителе, имеющей средство к адсорбированному на них ПАВу.
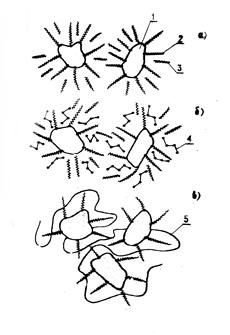
Рис.6. Механизм действия флокулирующего агента.
Флокуляция частиц полимером обусловлена большими размерами молекул полимера и их разветвленной структурой. Взаимодействуя с несколькими частицами сразу, молекула полимера обеспечивает укрупнение и коагуляцию частиц. В качестве полярного флокулирующего агента используют ацетон, этиловый спирт, этилацетат и др., а в качестве полимерных флокулянтов - полистирол, полиизобутилен, полимеры диметилсилоксана и др. Важными требованиями к полимерным флокулянтам являются их хорошая смешиваемость с жидкостью-носителем и чтобы длина молекулы в несколько раз превышала размер частиц феррофазы.
Описанный способ позволяет получать магнитные жидкости на других основах. Однако, нужно учесть, что таким образом можно производить замену сред только одного класса, например, один углеводород на другой. В дальнейшем этот способ был усовершенствован, что позволило производить замену различных по классу жидкостей-носителей [79]. Это достигается за счет подбора такого флокулирующего агента, который вызывает флокуляцию магнитных частиц без адсорбированного на них стабилизатора. Затем сфлокупировавшиеся магнитные частицы с помощью другого стабилизатора диспергируют в другой жидкости-носителе.
Замена жидкости-носителя в МЖ не только схожей с ней по свойствам, но и другими жидкостями, открывает возможность, получив предварительно МЖ наиболее простым и технологичным методом, в дальнейшем получать МЖ практически на любых основах и даже на таких, на которых прямым путем их получить очень трудно или вообще не удается. Например, можно, получив МЖ на воде, затем заменить воду углеводеродами, силиконовыми маслами, фторированными углеводородам или другими жидкостями-носителями. Кроме того, используя при повторном диспергировании другой стабилизатор, этим способом можно получить МЖ на той же основе, но с гораздо лучшими характеристиками и более широким спектром свойств.
В 80-90х гг в дипломных работах, выполненных на кафедре неорганической химии Белгосуниверситета им. В.И. Ленина дипломниками Витенчик Т.М, Омелюсик Л.С., Бурш В.В., Касперович Т.И. и др. были изучены закономерности процесса формирования пленок оксидов железа из стабильных коллоидных систем на основе магнитных оксидов железа с водной и неводной дисперсионной средой. Также было разработано несколько новых способов синтеза магнитных жидкостей. Так, например, в качестве стабилизатора были использованы олеат триэтаноламина (олеат ТЭА) и минеральные кислоты (HClO4, HNO3 и др.)
Из приведенного обзора видно, что наиболее простым и перспективным методом получения магнитных жидкостей является метод пептизации, хотя для получения МЖ с заранее заданными свойствами он требует усовершенствования.
2. Методика эксперимента
2.1. Синтез магнитного материала
2.1.1. Синтез магнетита
В данной работе был использован метод синтеза магнетита путем соосаждения солей двух- и трехвалентного железа избытком щелочи [80].
Готовилась смесь 25,5г FeSO4·7Н2О (марки чда) и 45г FeCl3·6Н2О, взятых в виде их 10%-ных водных растворов (т.о. отношение Fe(II):Fe(III) составляло 1,1:2, т.е. количество Fe(II) бралось в 10%-ном избытке по сравнению со стехиометрическим). Для предотвращения заметного окисления Fe(II) кислородом воздуха вода для приготовления раствора сульфата железа (II) подкислялась небольшим количеством (1-2 капли) концентрированной H2SO4.
Смесь растворов добавлялась быстро тонкой струей к 180-200мл 25%-ного раствора аммиака при интенсивном перемешивании механической мешалкой, которое продолжалось еще 20-25 мин после окончания реакции. Осаждение проводилось при рН=10.Образующийся черный осадок отмывался дистиллированной водой методом магнитной декантации до рН=8,5.
Из литературных данных известно, что целесообразно использовать 10%-е растворы солей (FeSO4·7H2O и FeCl3·6H2O)и их вливать в раствор щелочи или же проводить быструю нейтрализацию солей избытком щелочи, так как при медленном сливании разбавленных растворов образуются крупные частицы. Предотвратить образование гидрооксида железа и другие нежелательные побочные процессы можно используя предпочтительно хлорид и сульфат железа, а вместо едкого натра - водный раствор аммиака. Происходящая при этом химическая реакция может быть выражена следующим уравнением:
