Синтез, кинетика, термодимика
Сильные катиониты и аниониты, например, сульфокатиониты и аниониты типа четвертичных аммониевых оснований, не проявляют большой избирательности в отношении большинства ионов. Большая емкость смол такого типа, а также их способность функционировать в широком интервале рН могут быть использованы для концентрирования сильно разбавленных растворов, для обессоливания и в других случаях, когда необходимо полное извлечение всех катионов или анионов из раствора. Для выделения какого-либо одного элемента из смеси элементов бывает удобно подобрать такой сорбент, который избирательно поглощал бы ионы интересующего элемента.
В настоящее время известно большое количество селективных сорбентов. Синтез таких сорбентов сводится к задаче получения смолы с такой структурой, которая подобна структуре веществ, образующих прочные комплексы или нерастворимые соединения с данным ионом. Так была синтезирована смола (селективно сортирующая никель) путем введения в структуру смолы глиоксимовых группировок.
После выбора соответствующего сорбента необходимо определить область кислотности, в которой работает выбранный ионообменник, и его химическую устойчивость по отношению к тем рабочим средам и температурам, при которых должна проводиться очистка.
Процесс обмена ионов описывается уравнением изотермы, предложенным Б.П.Никольским:
![]()
где X1(2) и X2(2) -концентрации обменивающихся ионов в ионите (ммоль/г); X1(1)и X2(1) -концентрация обменивающихся ионов в равновесном растворе (ммоль/мл); γ1(2)и γ2(2) -коэффициенты активности обменивающихся ионов в фазе смолы; γ1(1) и γ2(1)- коэффициенты активности обменивающихся ионов в фазе раствора; Z1 и Z2 - заряды обменивающихся ионов; K -константа обмена.
Определение коэффициента активности в фазе смолы задача весьма сложная. Однако можно принять, что отношение коэффициентов активности ионов в поглощенном состоянии остается постоянным, и эту величину (можно ввести в константу. тогда, константа ионного обмена:
![]()
где a1(1) и а2(1) -активности обменивающихся ионов в равновесном растворе.
Если принять, что интересующий ион отмечен индексом 1, то для этого иона из уравнения никольскова имеем:
![]()
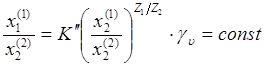
не ![]() -множитель, содержащий отношение коэффициентов активности обменивающихся ионов в растворе (в соответствующих степенях);
-множитель, содержащий отношение коэффициентов активности обменивающихся ионов в растворе (в соответствующих степенях); ![]()
Отношение количества вещества, поглощенного одним грамом сухой смолы, к его концентрации в равновесном растворе называется коэффициентам распределения данного иона. На практике для характеристики поглощения часто определяют именно эту величину, а не константу обмена, которая требует учёта не всегда известных коэффициентов активности.
По определению коэффициент распределения (α)
![]()
где q1(2) и q1(1) -содержание исследуемого иона соответственно фазе смолы и в растворе при равновесии, выраженное в любых единицах; V-объем раствора; m-навеска ионнта.
Коэффициент распределения являетcя величиной постоянной не зависит от концентрации интересующего иона в определенном интервале концентраций. Последнее означает, что поглощение ионов элемента -примеси прямо пропорционально его концентрации в растворе, и, следовательно, при очень малых концентрациях изотерма сорбции линейна. Величина коэффициента распределения зависит от природы второго обменивающегося иона, присутствия в растворе других ионов, в том числе мплексообразователей, кислотности раствора, температуры и давления.
Отношение коэффициентов распределения двух различных ионов в одних и тех же условиях называется коэффициентом разделения этих ионов в данных условиях.
Очистку соединений с помощью ионного обмена можно осуществлять разными способами. Если вещества-примеси содержат ионы с величиной заряда, отличающейся от величины заряда очищаемого элемента, то отделение основывается на том, что многозарядные ионы из разбавленных и умеренно концентрированных растворов поглощаются намного сильнее, чем ионы с меньшей величиной заряда. Так, если на сульфокатионитетипа КУ -2 или дауэкс -50 поглотить смесь щелочных, щелочноземельных и редкоземельных элементов, то при элюировании разбавленными растворами хлорной или соляной кислоты в первую очередь будут вымываться ионы щелочных металлов.
В более сложных случаях, когда необходимо разделить элементы, коэффициенты разделения которых близки к единице, чаще всего используют метод комплексообразовательной хроматографии. В этом случае весьма существенными становятся данные о составе, условиях образования и константах устойчивости различных комплексов разделяемых элементов.
В первом варианте все разделяемые ионы сначала поглощаются смолой. Затем производят их (разделение, пропуская (через колонку со смолой раствор комплексообразоаателя., который раздвигает -первоначально образовавшиеся близко расположенные зоны и последовательно вымывает их. При этом подбирают условия, наиболее благоприятные для комплексообравования (рН, температура, концентрация, скорость.пропускания раствора и т. п.). Все ионы вымываются в строго определенном порядке, который задается соотношением прочности связи данного иона со смолой с прочностью образующихся в фильтрате комплексов. Первыми вымываются те ионы, которые образуют наиболее прочные комплексы и слабее всего удержшваютоя смолой.
Во втором варианте комплексообразователь, добавляют к раствору, содержащему смесь разделяемых элементов, и в этом растворе создают условия, благоприятствующие комплексообразованию. Затем производят сорбцию этой смеси комплексов на соответствующем ионите, например, на анионите, если были получены анионные комплексы. При этом лучше всего сорбируютоя наиболее прочные комплексы, которые имеют наибольшее сродство к смоле.
Чем больше различие констант устойчивости, использованных для разделения комплексов, тем полнее и эффективнее достигаемое разделение в обоих вариантах.
Знание констант устойчивости различного вида комплексов очень полезно также при выборе сорбентов, селективно поглощающих определенные ионы. Известно, что во многих случаях сорбированные ионы образуют комплексные соединения со структурными элементами смолы. Очевидно, что чем более
прочные комплексы образуются в фазе смолы, тем большей (избирательностью в отношении данного иона будет обладать смола. В литературе имеется немного работ, посвященных изучению прочности комплексов с функциональными группами :молы. Поэтому, на практике при выборе селективного сорбента пользуются данными об устойчивости аналогичных комплексов в растворах.
Комплексообразование в фазе смолы объясняет, например, высокую избирательность карбоксильных и фосфатных катионов в отношении некоторых катионов. Установлен следующий порядок селективности фосфорнокислых смол в отношении катионов: Th4+ >U 4+ >UO22+ ![]() Fe3+> редкоземельные элементы > Н+ > Сu2+ >Со2+ >Вa2+ >Na+.
Fe3+> редкоземельные элементы > Н+ > Сu2+ >Со2+ >Вa2+ >Na+.
