Увеличение степени защиты стали от коррозии в нейтральных и кислых средах
Неравномерная коррозия значительно более опасна, чем равномерная. Неравномерная коррозия, при сравнительно небольшом количестве окисленного металла, вызывает большое уменьшение сечения в отдельных местах. Язвенная или точечная коррозия могут привести к образованию сквозных отверстий, например в листовом материале, при малой потере металла [31].
Приведенная классификация, конечно, условна. Возможны многочисленные формы разрушения, лежащие между характерными типами, показанными на рисунок 1.2.
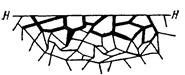
Рисунок 1.2 – Межкристаллитная коррозия.
Некоторые сплавы подвержены своеобразному виду коррозии, протекающей только по границам кристаллитов, которые оказываются отделенными друг от друга тонким слоем продуктов коррозии (межкристаллитная коррозия). Здесь потери металла очень малы, но сплав теряет прочность. Это очень опасный вид коррозии, который нельзя обнаружить при наружном осмотре изделия.
1.4 Термодинамическая оценка процесса электрохимической коррозии
Процесс электрохимической коррозии совокупность двух сопряженно протекающих реакций:
![]() (анодный процесс),
(анодный процесс),
![]() (катодный процесс),
(катодный процесс),
где D – деполяризатор (окислитель).
Причина коррозии – термодинамическая неустойчивость металлов, сплавов и сталей в агрессивной среде. Определить вероятность протекания коррозионного процесса, как и любого электрохимического процесса, можно по изменению энергии Гиббса:
![]() (1.3)
(1.3)
Известно, что любая реакция протекает в данном направлении, если при этом уменьшается энергия Гиббса ΔG <0. Энергия Гиббса ΔG связана с ЭДС электрохимической реакции следующим соотношением.
![]() , (1.4)
, (1.4)
где ![]() .
.
Таким образом, ![]()
Из последнего уравнения видно, что коррозия металла протекает самопроизвольно при условии, что равновесный потенциал окислителя ![]() более положителен, чем равновесный потенциал металла
более положителен, чем равновесный потенциал металла ![]() [28, 31].
[28, 31].
1.5 Кинетическое обоснование процесса коррозии
В настоящее время считается достаточно строго обоснованной кинетическая теория. Она пришла на смену устаревшей теории микрогальванических (локальных) элементов.
Коррозионные процессы являются гетерогенными химическими реакциями и к ним применили почти все положения формальной кинетики. Так, рассматривая этот процесс в виде последовательных стадий: 1) доставка вещества к поверхности; 2) адсорбция; 3) собственно реакция; 4) образование (или исчезновение) новой фазы; 5)отвод продуктов.
Любая из этих пяти стадий электрохимического процесса может протекать затрудненно по сравнению с остальными. Поскольку в стационарных условиях скорость всего процесса определяется самой медленной стадией, то для того, чтобы эту стадию ускорить требуется определенные энергетические затраты, вызывающие перенапряжение [5, 6].
Если замедлена доставка ионов к поверхности или отвод продуктов реакция (транспортная стадия), а все остальные стадии (разряд ионов, ионизация металла, образование или разрушение кристаллической решетки) протекают без затруднений, быстро, то возникает концентрационное перенапряжение.
Если замедлена только собственно электрохимическая реакция, то есть разряд ионов или окисление металла с отдачей электронов (эту стадия часто называют переносом заряда), то возникает химическое или активационное перенапряжение.
Если эта стадия не требует ускорения, но затруднена стадия образования новой фазы, возникает фазовое перенапряжение [6].
1.5.1 Поляризация электродных процессов
Скорость электрохимической коррозии металлов в агрессивных средах ограничивается явлением поляризации.
Причина поляризации электрода, возникновение перенапряжения состоит в том, что при протекании на электроде электрохимической реакции (окисления или восстановления) могут возникнуть того или иного рода затруднения. Поскольку в стационарных условиях скорость процесса определяется самой медленной стадией, то для ее ускорения требуется определенные энергетические затраты, вызывающие перенапряжение.
Экспериментально было установлено, что при протекании постоянного тока падение напряжения на металлических электродах значительно выше, чем рассчитанное по закону Ома.
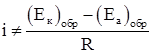 (1.5)
(1.5)
При постоянной величине сопротивления электролита причина настоящего неравенства обусловлена изменением величины числителя. При этом потенциал анода, как показано на рисунке 1.3, становится положительнее, а потенциал катода – отрицательнее:
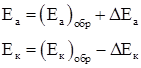 (1.6)
(1.6)
где Еа и Ек – достигнутые при данном значении тока электродные потенциалы, называемые эффективными; ΔЕа и ΔЕк – смещение потенциалов анода и катода.
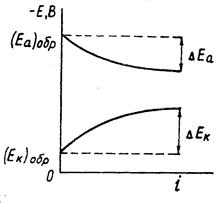
Рисунок 1.3 – Поляризация электродов
Явление электродной поляризации тормозит протекание коррозионного процесса; Уравнение, позволяющее оценить скорость электрохимического коррозионного процесса, величину коррозионного тока, в общем виде записывается следующим образом
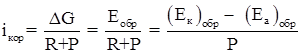 (1.7)
(1.7)
где R – омическое сопротивление корродирующей системы; Р – поляризационное сопротивление (сопротивление протеканию электродных процессов) системы [31].
1.5.2 Концентрационная поляризация
В тех случаях, когда скорость электродной реакции настолько велика, что ее начинает ограничивать доставка к электроду разряжающихся частиц, происходит изменение концентрации раствора в слое, прилегающем к электроду, за пределами двойного электрического слоя. При этом имеет место концентрационная поляризация электрода из-за обеднения раствора у металла разряжающимися частицами. Величина ее, следовательно, зависит от массопереноса.
Перенос реагирующих веществ в условиях электрохимической реакции может осуществляться по трем механизмам. Основным механизмом является молекулярная диффузия, т.е. перемещение частиц вещества под действием градиента концентрации. Второй механизм массопереноса – миграция, т.е. перемещение заряженных частиц под действием электрического поля. При протекании катодных процессов миграция ускоряет доставку к поверхности электрода катионов и замедляет подвод анионов, создавая избыток постороннего индифферентного электролита (фона), можно резко уменьшить омическое падение потенциала в растворе и тем самым элиминировать миграцию. Третий механизм – конвекция, т.е. перенос вещества вместе с потоком движущейся жидкости [6]. Неравновесным в условиях лимитирующей стадии переноса оказывается некоторый слой раствора вблизи поверхности электрода, в котором концентрация реагирующих веществ изменяется от значения С0 в объеме до Сэ – у поверхности.
